Clear Sky Science · tr
CRMP2, meme kanserinde CXCL10 mRNA’sının ILF3’e bağlı stabilizasyonunu bozarak metastaz oluşumunu engelliyor
Neden kanserin yayılmasını durdurmak önemli
Meme kanserinden kaynaklanan ölümlerin çoğu, birincil tümörden değil, kanser hücrelerinin akciğerler gibi hayati organlara gidip buralarda yeni büyümeler oluşturmasından kaynaklanır. Bu çalışma, uzak organların göç eden kanser hücreleri için serdiği “hoş geldin paspasını” değiştirerek bu yayılmayı yavaşlatabilen ya da engelleyebilen, meme kanseri hücrelerinde bulunan yerleşik bir koruyucu proteini ortaya çıkarıyor. Bu gizli güvenlik düğmesini anlamak, kanserin vücudun başka yerlerine tutunmasını engelleyen yeni tedavilere kapı açabilir.
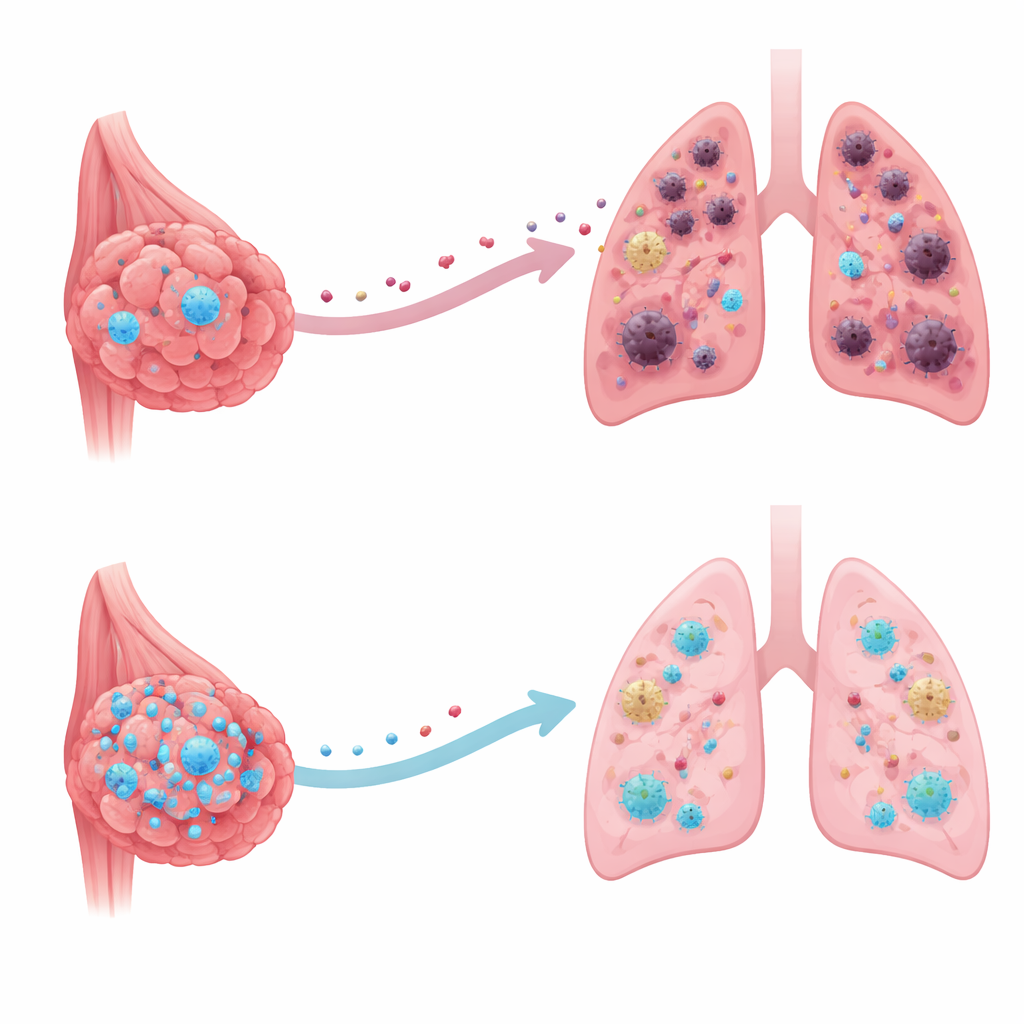
Kanser hücrelerinin içindeki sessiz bir savunmacı
Araştırmacılar, sinir hücrelerinin büyümesine ve iç iskeletinin korunmasına yardımcı olmasıyla bilinen CRMP2 adlı proteine odaklandı. Büyük kamuya açık kanser veritabanları ve hasta tümör örnekleri incelendiğinde, CRMP2 seviyelerinin özellikle yayılmış kanserlerde meme tümörlerinde olağandışı derecede düşük olduğu görüldü. Tümörlerinde hâlâ daha yüksek CRMP2 miktarına sahip hastalar daha uzun yaşama eğilimindeydi ve uzak metastaz geliştirme olasılıkları daha düşüktü. Bu desen, CRMP2’nin meme kanserinde hızlandırıcı değil, fren gibi davrandığını; hastalığın sürücüsünden ziyade içsel bir savunmacı olduğunu düşündürdü.
Akciğerlerin istila için nasıl hazırlanması
Kanser hücreleri nadiren uzak bir organa sürpriz bir şekilde ulaşır. Orijinal tümör oraya varmadan çok önce, o organı bilim insanlarının “pre‑metastatik niş” dediği—kanserin hayatta kalmasını kolaylaştıran bir mikroçevre—hale getiren moleküller salar. İnsan meme kanserini yakından taklit eden iyi kurulmuş bir fare modelini kullanarak ekip, meme tümörü hücreleri ekstra CRMP2 üretmesi için modifiye edildiğinde birincil tümörlerin aynı hızda büyüdüğünü, ancak akciğerlerin çok daha az elverişli hale geldiğini gösterdi. Akciğerlerdeki iltihap ve doku yeniden yapılanması belirteçleri azaldı ve normalde anti‑tümör savunmaları baskılayan immün hücrelerden daha az çekildiler. Sonuç olarak, ana tümör alındıktan sonra akciğerlerde çok daha az metastatik nodül oluştu.
Sorun çıkaran bir sinyal zinciri
Daha derine indiklerinde, bilim insanları akciğerleri hazırlamaktan hangi tümör kaynaklı sinyallerin sorumlu olduğunu sordular. Belirledikleri hedef CXCL10 oldu: belirli immün hücreleri çeken ve uykudaki kanser hücrelerini uyandıran küçük bir haberci protein (kemokin). Hem laboratuvarda yetiştirilen insan hem de fare meme kanseri hücrelerinde CRMP2’yi artırmak, üretilen ve salgılanan CXCL10 miktarını keskin şekilde azalttı. Farelerde, CRMP2 bakımından zengin tümör materyaline maruz kalan akciğerlerde CXCL10 ve normalde koruyucu T hücre aktivitesini zayıflatan gelen immün hücrelerde belirgin düşüş görüldü. Araştırmacılar CXCL10’u bir antikorla bloke ettiklerinde akciğer kolonizasyonu azaldı; fazladan CXCL10 eklediklerinde ise CRMP2’nin koruyucu etkisi ortadan kalktı. Bu, CXCL10’u metastaz‑dostu nişin tetikleyicisi olarak CRMP2’nin hemen altında konumlandırdı.
Kötü sinyalleri stabil hale getiren gizli aracı
CRMP2 hücre içinde yaşarken CXCL10 salgılandığı için ekip moleküler bir aracıdan şüphelendi. CRMP2’nin doğrudan bir ortağı olarak ILF3 adlı bir RNA‑bağlayıcı proteini tanımladılar. ILF3, CXCL10’un RNA şemasına tutunur ve normalde bunun parçalanmasını engelleyerek daha fazla CXCL10 protein üretimine izin verir. CRMP2, ILF3’e belirli temas noktalarından bağlanır ve onu hücrenin protein geri dönüşüm mekanizması aracılığıyla yok edilmek üzere etiketler; böylece ILF3’ün ömrünü kısaltır ve CXCL10 RNA’sı üzerindeki kontrolünü bozar. CRMP2 seviyeleri yüksek olduğunda ILF3 daha hızlı parçalanır, CXCL10 RNA’sı kararsız hale gelir ve daha az iltihaplı kemokin salgılanır. ILF3 yapay olarak geri getirildiğinde, CXCL10 üzerindeki CRMP2 baskısını aşabildi ve bu zincirdeki kritik bağlantı olduğunu doğruladı.
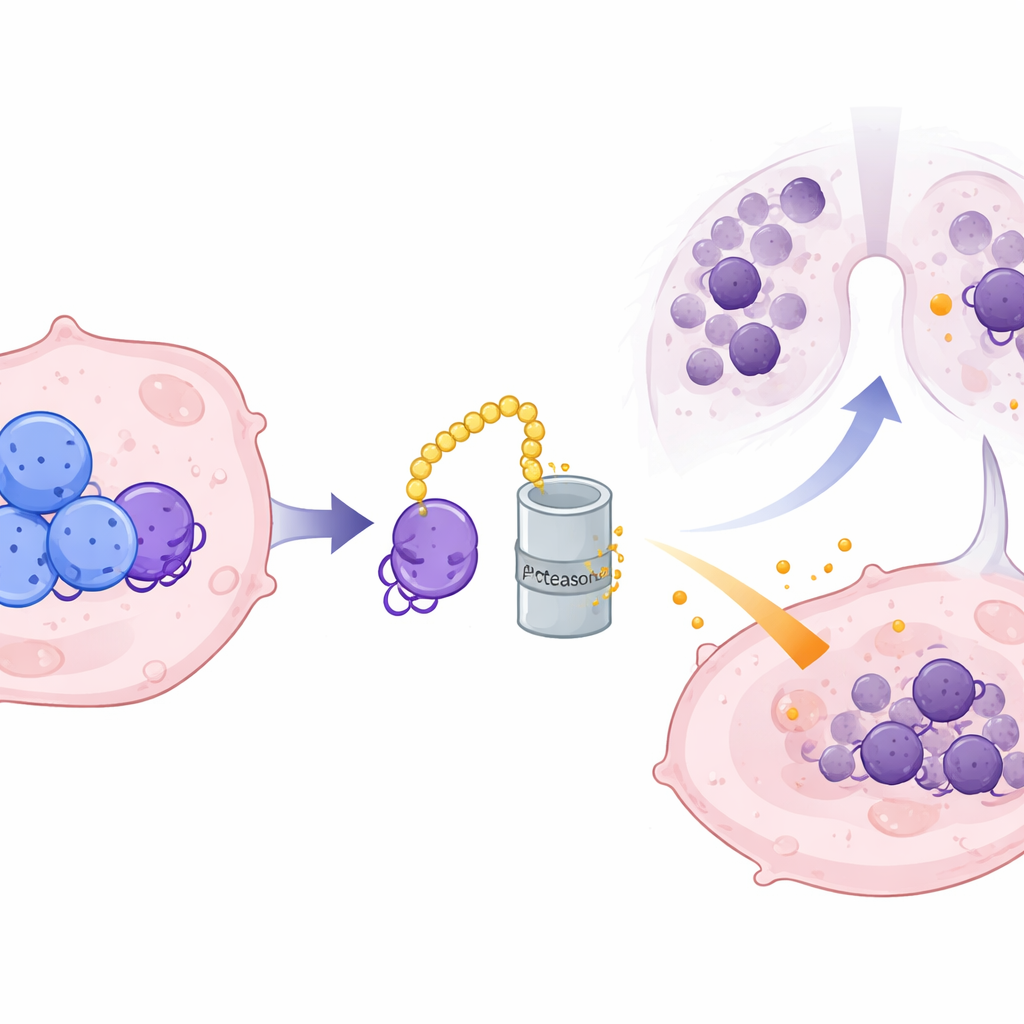
Bitki bileşiğini potansiyel bir müttefik haline getirmek
Bu yolun terapötik olarak kullanılıp kullanılamayacağını test etmek için araştırmacılar doğal bileşik kitaplığını taradılar ve uzun süredir cilt tedavilerinde kullanılan bitki kaynaklı bir molekül olan psoralen’in doğrudan CRMP2’ye bağlandığını ve onu daha kararlı hale getirdiğini buldular. Hücre deneylerinde psoralen CRMP2 seviyelerini yükseltti, ILF3 ve CXCL10’u düşürdü ve meme kanseri hücrelerinin invaziv davranışını genel canlılıklarını bozmayarak azalttı. Birden fazla fare modelinde psoralen birincil meme tümörlerini küçültmedi, ancak akciğer metastazlarını güçlü şekilde azalttı ve pre‑metastatik niş oluşumunu törpüledi; yine bu etki CRMP2’ye bağlıydı. Psoralen’in kendisi karaciğer toksisitesi yapabileceği için iyileştirme gerektirse de, bu sonuçlar küçük moleküllerin CRMP2’nin koruyucu rolunu güçlendirebileceğini gösteriyor.
Hastalar için bunun anlamı
Bir arada ele alındığında, bu çalışma CRMP2’nin ILF3’ü destabilize ettiği, bunun da CXCL10’u düşürerek akciğerlerin metastaz için verimli bir zemin olmasını engellediği meme kanseri hücreleri içinde koruyucu bir ekseni açığa çıkarıyor. Bu strateji kanser hücrelerine doğrudan saldırmaktan ziyade, onların dayandığı uzak nişleri etkisizleştirerek vücudun kendi savunmalarının lehine dengeyi değiştirmeyi amaçlıyor. Klinik uygulamaya ulaşmadan önce yapılması gereken çok şey olsa da, CRMP2–ILF3–CXCL10 yolunu hedeflemek —muhtemelen daha güvenli psoralen benzeri ilaçlarla— meme kanserinin yayılmasını önlemek için umut verici yeni bir yaklaşım sunuyor.
Atıf: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Anahtar kelimeler: meme kanseri metastazı, pre‑metastatik niş, kemokin sinyalleşmesi, RNA-bağlayıcı proteinler, doğal ürün terapileri