Clear Sky Science · tr
CCL11, cerrahiden sonra immünsüpresif CCR5+ CD206+ M2-benzeri makrofajları güçlendirerek ve tümör invazivitesini artırarak hepatosellüler karsinomun nüksünü teşvik eder
Karaciğer kanserinin cerrahiden sonra neden yeniden ortaya çıkabildiği
Karaciğer cerrahisi, erken evre karaciğer kanseri olan hastalar için sıklıkla en iyi umut olsa da birçok hastada kanser birkaç yıl içinde tekrar görülebiliyor. Bu çalışma basit ama kritik bir soruyu ele alıyor: Cerrahinin tetiklediği vücudun kendi iltihabi yanıtı kazara kalan kanser hücrelerinin büyümesine ve yayılmasına yardımcı oluyor mu? Araştırmacılar CCL11 adlı bir sinyal molekülüne odaklanıyor ve cerrahiden sonra bu molekülün ani artışının hem anti-kanser bağışıklığı zayıflattığını hem de hayatta kalan tümör hücrelerini daha agresif hale getirdiğini gösteriyor.
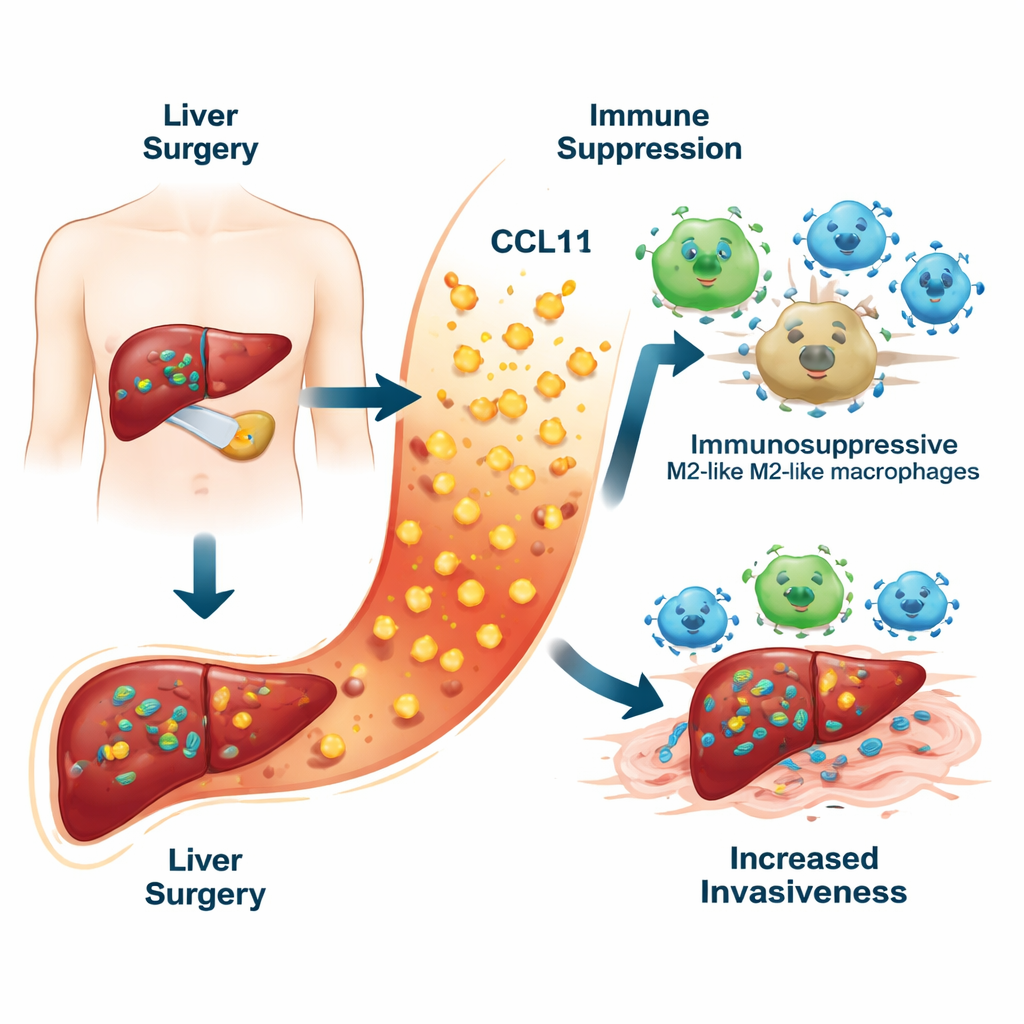
İyileşme yanıtında gizli bir tehlike
Cerrahlar bir karaciğer tümörünü çıkardıklarında kan damarlarını klemplamak ve çevre dokuyu yaralamak zorundadırlar. Bu hasar, karaciğerin iyileşmesine yardımcı olan bir inflamasyon dalgasını tetikler. Hastaların ameliyattan bir hafta sonra kanlarında on farklı inflamatuar molekülü ölçerek, ekip bir kemokin olan CCL11’in öne çıktığını buldu. Daha sonra karaciğer kanseri nükseden hastaların CCL11 düzeyleri, kanserden uzak kalanlara göre anlamlı derecede daha yüksekti. Yüksek CCL11 seviyeleri ayrıca daha kötü sağkalımla ilişkilendirildi. Araştırmacılar CCL11’i rutin klinik verilerle —kan testleri ve tümör özellikleri gibi— birleştirdiklerinde, beş yıllık nüksü geleneksel modellerden daha doğru tahmin eden bir risk “skor kartı” oluşturabildiler.
Normal görünen karaciğer dokusu hâlâ önem taşıyor
Kanser araştırmalarında çoğunlukla dikkat tümörün kendisine yönelir, ancak bu çalışma çevredeki “normal” karaciğer dokusunun da en az tümör kadar önemli olabileceğini gösteriyor. 100’den fazla hastadan alınan örneklerde CCL11 aslında tümör düğümlerinden veya sağlıklı verici karaciğerlerinden daha yüksek düzeydeydi. Yakın çevredeki karaciğer dokusunda daha fazla CCL11 üreten hastalar, daha ileri evre hastalık, uzak yayılım ve cerrahi sonrası nüks ile daha fazla ilişkiliydi. Bir operasyon sırasında kısa süreli kan akımı kesilip yeniden sağlanmasını taklit eden fare modellerinde karaciğer yaralanması hızla CCL11 düzeylerini yükseltti. Laboratuvarda düşük oksijen koşullarında, miyofibroblastlar ve kan damarı döşeyen hücreler gibi karaciğeri destekleyen hücreler de daha fazla CCL11 üretti; bu da cerrahi stresin geride kalan karaciğer dokusunu tümörü destekleyen bir ortama hazırladığını düşündürüyor.
CCL11 nasıl bağışıklık savunucularını kenara çeker
CCL11’in bağışıklığı nasıl şekillendirdiğini görmek için yazarlar, tümörleri ya saldırabilecek ya da koruyabilecek çok yönlü beyaz kan hücreleri olan makrofajlara odaklandı. Tümör dışı karaciğer dokusunda daha yüksek CCL11, CCR5 işaretçisini taşıyan ve M2-benzeri, tümör dostu bir profil gösteren bir makrofaj alt tipinin artışıyla el ele gitti. Hastalarda CCR5+ M2-benzeri makrofajlarla zengin karaciğerler daha kötü sağkalım ile ilişkiliydi. Hücre kültüründe CCL11 eklemek, monositleri bu immünsüpresif makrofaj tipine dönüştürdü; PD‑L1 ve IL‑10 gibi moleküllerin üretimini artırdı ve daha fazla bağışıklık hücresini çeken ve yönlendiren diğer sinyalleri saldı. Bu CCL11 ile koşullandırılmış makrofajlar daha sonra naïf yardımcı T hücrelerini, anti-tümör yanıtları baskılayan düzenleyici T hücrelere dönüşmeye teşvik etti. Mekanistik deneyler CCL11’in makrofajların içinde NF‑κB yolunu ve PD‑L1 üretimini sonlandıran bir sinyal zincirini aktive ettiğini gösterdi; bu da kanser hücrelerini bağışıklık saldırısından korumaya yardımcı oluyor.
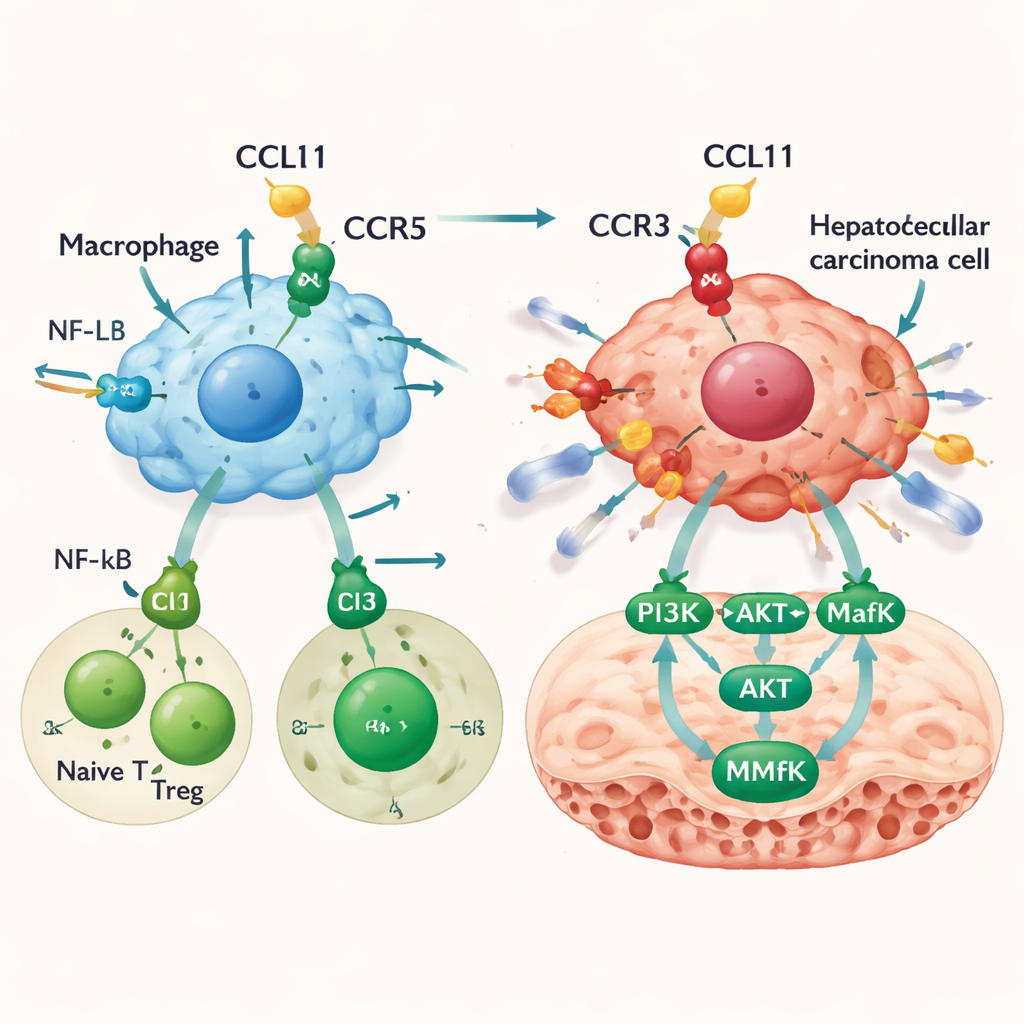
CCL11 nasıl kalan kanser hücrelerini daha invaziv hale getiriyor
CCL11 yalnızca immün manzarayı yeniden şekillendirmekle kalmıyor; aynı zamanda karaciğer kanseri hücreleri üzerinde doğrudan etkili oluyor. Kanser hücreleri kendileri çok az CCL11 üretse de CCR3 adlı reseptörlerden birini taşıyorlar. Laboratuvar deneylerinde CCL11, karaciğer kanseri hücrelerinin büyümesini hızlandırmadı ama onların bariyerler boyunca göç etmelerini ve invaze etmelerini kolaylaştırdı; bu, metastatik potansiyelin bir işaretidir. CCR3 reseptörünün bloke edilmesi bu etkiyi büyük ölçüde ortadan kaldırdı. Gen analizi, CCL11–CCR3 sinyalinin PI3K ve AKT’i devreye soktuğu, bunun da MafK adlı bir transkripsiyon faktörünü aktive ettiği bir yol gösterdi. MafK ise çevre dokuyu parçalayan ve kanser yayılımı için yollar açan bir enzim olan MMP13 üretimini artırıyor. Fare modellerinde karaciğere CCL11 verilmesi tümör yükünü artırdı ve PI3K–AKT–MafK–MMP13 yolunun tümörler içinde daha yüksek düzeyde aktivitesine eşlik ederek daha fazla metastaza yol açtı.
Riskli bir sinyali tedavi fırsatına çevirmek
CCL11 hem bağışıklık savunmalarını susturuyor hem de kalıntı kanser hücrelerini güçlendiriyor gibi göründüğünden araştırmacılar, cerrahiden sonra bunu engellemenin sonuçları değiştirip değiştiremeyeceğini test ettiler. Cerrahi olarak çıkarılan karaciğer tümörleri olan farelerde, CCL11’i nötralize eden bir antikorla tedavi, karaciğerin tekrar kanserle tutulma oranını dramatik şekilde azalttı ve belirgin kilo kaybı gibi yan etkiler olmadan sağkalımı iyileştirdi. Bir araya getirildiğinde bulgular, CCL11’i cerrahi yaralanmayı immünsüpresif ve invazyon-dostu bir karaciğer ortamına bağlayan anahtar bir anahtar olarak sunuyor. Hastalar için bu çalışma, ameliyat sonrası CCL11 düzeyinin ölçülmesinin en yüksek nüks riski taşıyanları belirlemeye yardımcı olabileceğini ve CCL11–CCR5/CCR3 eksenini hedef alan ilaçların bir gün karaciğer kanserinin geri gelmesini önleme stratejilerinin parçası haline gelebileceğini öne sürüyor.
Atıf: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Anahtar kelimeler: karaciğer kanseri nüksü, CCL11 kemokin, tümör mikroçevresi, immün baskılama, kanser metastazı