Clear Sky Science · tr
Kanserle ilişkili fibroblastlar METTL1 aracılı NET1 m7G modifikasyonu yoluyla non-small hücreli akciğer kanseri hücrelerinde osimertinib direncini teşvik eder
Bazı akciğer kanserlerinin “akıllı” bir ilaca neden yanıt vermeyi kesmesi
Osimertinib gibi hedefe yönelik ilaçlar, sık görülen bir akciğer kanseri türünde birçok hasta için tedaviyi dönüştürdü; geleneksel kemoterapiden daha az yan etkilerle daha uzun yaşam süresi sağlıyorlar. Yine de çoğu hasta için bu yararlar geçici oluyor: tümörler sonunda ilacı alt etmenin yollarını buluyor. Bu çalışma, önemi büyük ama göründüğü kadar basit bir soruyu araştırıyor: tümörün destekleyici dokusu—özellikle kanserle ilişkili fibroblastlar olarak adlandırılan hücreler—osimertinib’in etkilerinden kaçmasına sessizce yardımcı oluyor mu?
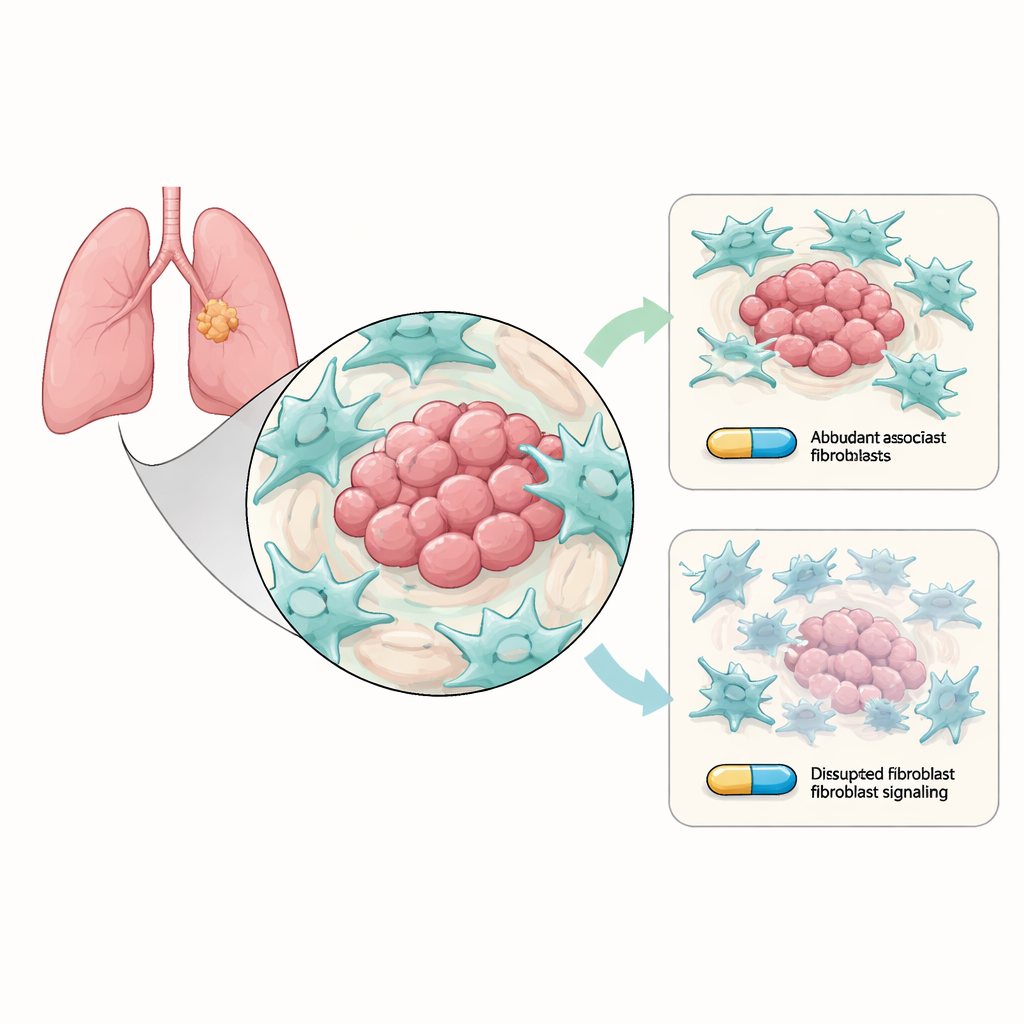
Tümörü gizlice koruyan yardımcı hücreler
Non-small hücreli akciğer kanseri, tümör mikroçevresi olarak bilinen kanser dışı hücrelerin yoğun olduğu bir mahallede büyür. En bol bulunan sakinlerden biri kanserle ilişkili fibroblastlardır (CAFlar); bunlar tümör çevresini yeniden düzenleyen bağ doku hücreleridir. Araştırmacılar, lab ortamında olağan osimertinib’e duyarlı EGFR mutasyonlarını taşıyan akciğer kanseri hücrelerini CAFlarla birlikte büyüttüler. CAFlar var olduğunda, kanser hücrelerinin osimertinib ile öldürülmesinin daha zor olduğunu buldular: daha fazla koloni oluşturdular, daha az kendi kendini yok etme gösterdiler ve uzun vadeli hayatta kalma ve nüksle bağlantılı daha güçlü “kök-benzeri” özellikler sergilediler. Başka bir deyişle, ilaç hâlâ kanser hücrelerini hedeflese bile, çevredeki fibroblastlar onların dayanmasına sessizce yardım etti.
Kuralları değiştiren RNA üzerindeki kimyasal etiket
Takım daha sonra genlerin ötesine, hücre içindeki genetik bilginin çalışan kopyaları olan RNA’yı süsleyen kimyasal etiketlere baktı. m7G olarak adlandırılan bu etiketlerden biri, bir RNA molekülünün ne kadar kararlı olduğunu ve ne kadar verimli proteine çevrildiğini etkileyebilir. Biyokimyasal testler ve genoma yayılmış haritalama kullanarak araştırmacılar, CAFların akciğer kanseri hücrelerindeki RNA’lar üzerinde genel m7G işaretlemesini artırdığını gösterdiler. Bu artış esas olarak m7G işaretlerini haberci RNA’lara yerleştiren bir metiltransferaz enzimi olan METTL1 tarafından sağlandı. METTL1 düzeyleri akciğer tümörlerinde çevredeki normal dokuya göre daha yüksekti ve daha ileri hastalık ile daha kötü hasta sağkalımıyla ilişkilendiriliyordu; bu da bu enzimin yalnızca rutin hücresel işlevleri ince ayarlamaktan daha fazlasını yaptığını ima ediyor.
Salınan bir sinyal ve zayıf bir moleküler zincir
CAFlar METTL1’i kanser hücrelerinde nasıl artırıyor? Çalışma, CAFların çevrelerine salgıladığı HMGB1 adlı bir proteine işaret ediyor. CAFlar kanser hücrelerine kıyasla çok daha fazla HMGB1 salgıladı. Araştırmacılar HMGB1’i akciğer kanseri hücrelerine eklediklerinde METTL1 düzeyleri ve m7G işaretleri arttı; CAFlardan elde edilen ortamda HMGB1 bloke edildiğinde bu etki zayıfladı. Daha da yakından baktıklarında METTL1’in bir ana RNA hedefini tanımladılar: hücre büyümesini ve hareketini destekleyen NET1 geni. CAFlar hem NET1 RNA ve protein bolluğunu hem de NET1 üzerindeki m7G etiketlemesini artırdı ve METTL1 NET1 RNA’sına fiziksel olarak bağlanarak onu stabilize etti. METTL1 azaldığında modifiye NET1 daha az oldu, kanser hücrelerinin hayatta kalma sinyalleri zayıfladı ve osimertinib’e duyarlılık arttı.
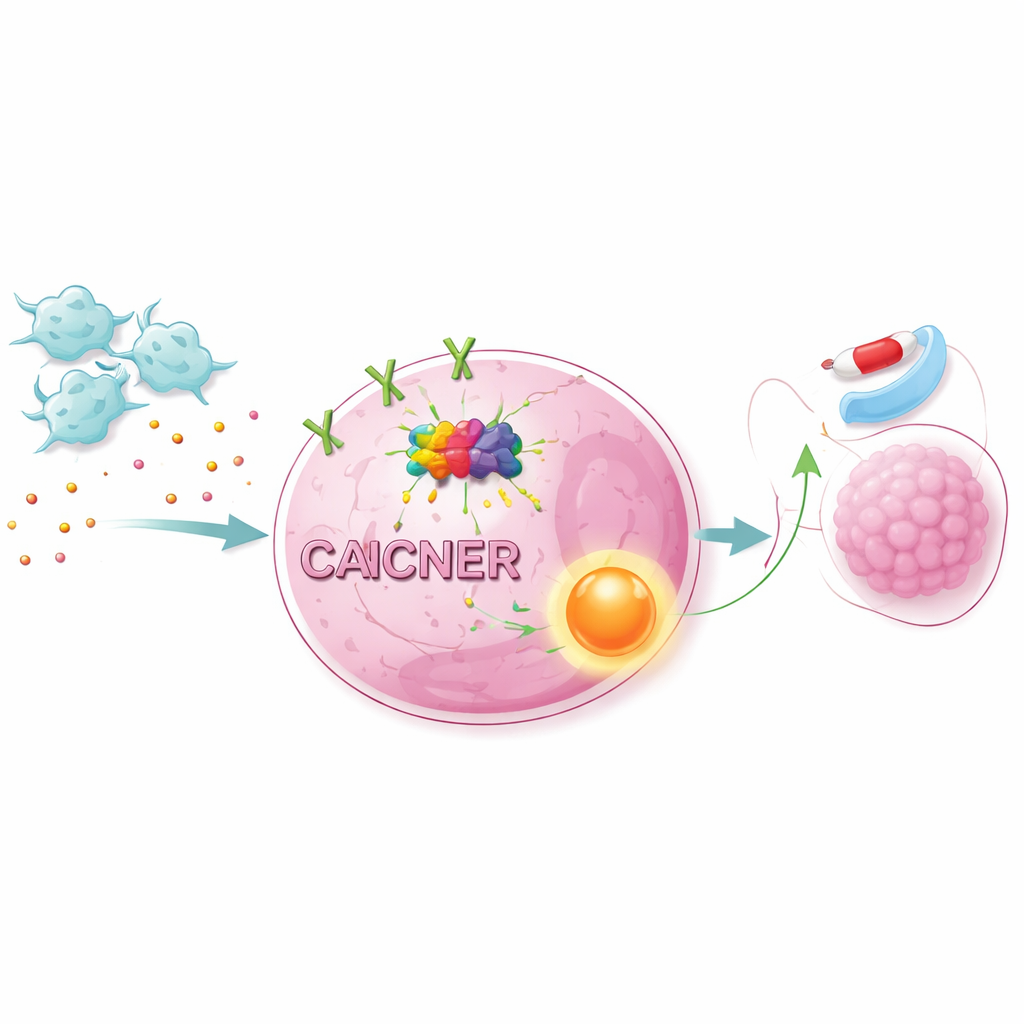
Kanser hücreleri içinde hayatta kalma yollarını açmak
Güçlenen NET1 sinyali tek başına hareket etmedi. Büyük ölçekli RNA verilerini yol analiziyle birleştirerek bilim insanları CAFların AKT/NF-κB olarak bilinen hücre içi ana büyüme ve hayatta kalma yolunu aktive ettiğini gösterdiler. AKT veya NF-κB’yi spesifik inhibitörlerle bloke etmek, CAFların varlığında bile akciğer kanseri hücrelerini osimertinib’e karşı daha savunmasız hale getirdi. NET1 düzeylerini değiştirmek benzer etkiler yarattı: NET1’i azaltmak CAFların korumasını zayıflatırken, NET1’i artırmak direnci güçlendirdi. İnsan akciğer kanseri hücreleri farelere nakledildiğinde CAFlar eklemek tümörlerin daha hızlı büyümesine ve osimertinib’e daha az yanıt vermesine yol açtı. Kanser hücrelerinde METTL1’i baskılamak m7G işaretlerini azalttı, NET1 ve yol aktivasyonunu düşürdü ve CAFlardan kaynaklanan tümör büyümesini keskin biçimde azalttı.
Gelecekteki akciğer kanseri tedavisi için çıkarımlar
EGFR-mutasyonlu akciğer kanseriyle karşı karşıya olan kişiler için bu çalışma, güçlü ilaçlar olan osimertinib’in neden zamanla başarısız olduğunu düşünmenin yeni bir yolunu sunuyor. Sorumluluğu yalnızca kanser hücrelerindeki yeni mutasyonlara yüklemek yerine, tümör hücresi dışında başlayan moleküler bir zinciri vurguluyor—CAFların HMGB1 salgılamasıyla başlayan—METTL1 aracılığı, NET1 üzerindeki m7G işaretleri ve ilacın etkisini azaltan hayatta kalma yolaklarının aktivasyonu. Bu zinciri herhangi bir noktada kesmek teorik olarak duyarlılığı geri getirebilir veya uzatabilir. METTL1, HMGB1 veya belirli m7G ile işaretlenmiş RNA’ları doğrudan hedefleyen ilaçlar hâlâ erken aşamalarda olsa da, çalışma osimertinib’i tümörün destekleyici hücrelerine veya onların RNA-değiştiren sinyallerine yönelik tedavilerle birleştirmenin bu akciğer kanseri formunu daha uzun süre kontrol altında tutmaya yardımcı olabileceğini öne sürüyor.
Atıf: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Anahtar kelimeler: osimertinib direnci, non-small hücreli akciğer kanseri, kanserle ilişkili fibroblastlar, RNA metilasyonu, METTL1 NET1 yolu