Clear Sky Science · tr
Onkogenik BCS1L izoformunun ekson tercihinin değiştirilmesi, mitokondriyal işlevi bozarak over kanseri ilerlemesini baskılar
Kanser Hücrelerinin İçindeki Enerji Santralleri
Vücudumuzdaki her hücre, mitokondri adı verilen küçük enerji santrallerine dayanır. Hızla büyüyüp yayılan kanser hücreleri enerjiye özellikle çok ihtiyaç duyar. Bu çalışma, over kanserinin mitokondrilerden birini destekleyen temel yardımcısını nasıl yeniden düzenlediğini ortaya koyuyor ve bu yardımcı üzerinde moleküler bir “anahtarı” nazikçe çevirmenin, sağlıklı dokuları büyük oranda korurken tümörleri nasıl açlığa sürükleyebileceğini gösteriyor.
Neden Tümörler Motorlarına Güvenir?
Over kanseri hücreleri, pek çok kanserde olduğu gibi, farklı enerji kaynaklarına esnek biçimde yönelebilir. Araştırmacılar büyük hasta veri tabanlarını ve tek hücre profillerini tarayarak birçok over tümörünün mitokondrilerini oksidatif fosforilasyon (OXPHOS) olarak bilinen yüksek devrede çalıştırdığını saptadı. Bu artırılmış mitokondriyal aktiviteye sahip tümörler daha agresifti ve ileri evre hastalıkta daha yaygındı. Mitokondri enerji makinesini kuran birçok proteinden biri öne çıktı: Kompleks III’ün montajını yardım eden şaperon BCS1L. Yüksek OXPHOS gösteren tümörler ve belirli tümör hücre alt tipleri özellikle güçlü BCS1L aktivitesi sergiliyordu; bu da kanser hücrelerinin motorlarını çalıştırmak için bu yardımcıya yoğun biçimde dayandığını düşündürdü.
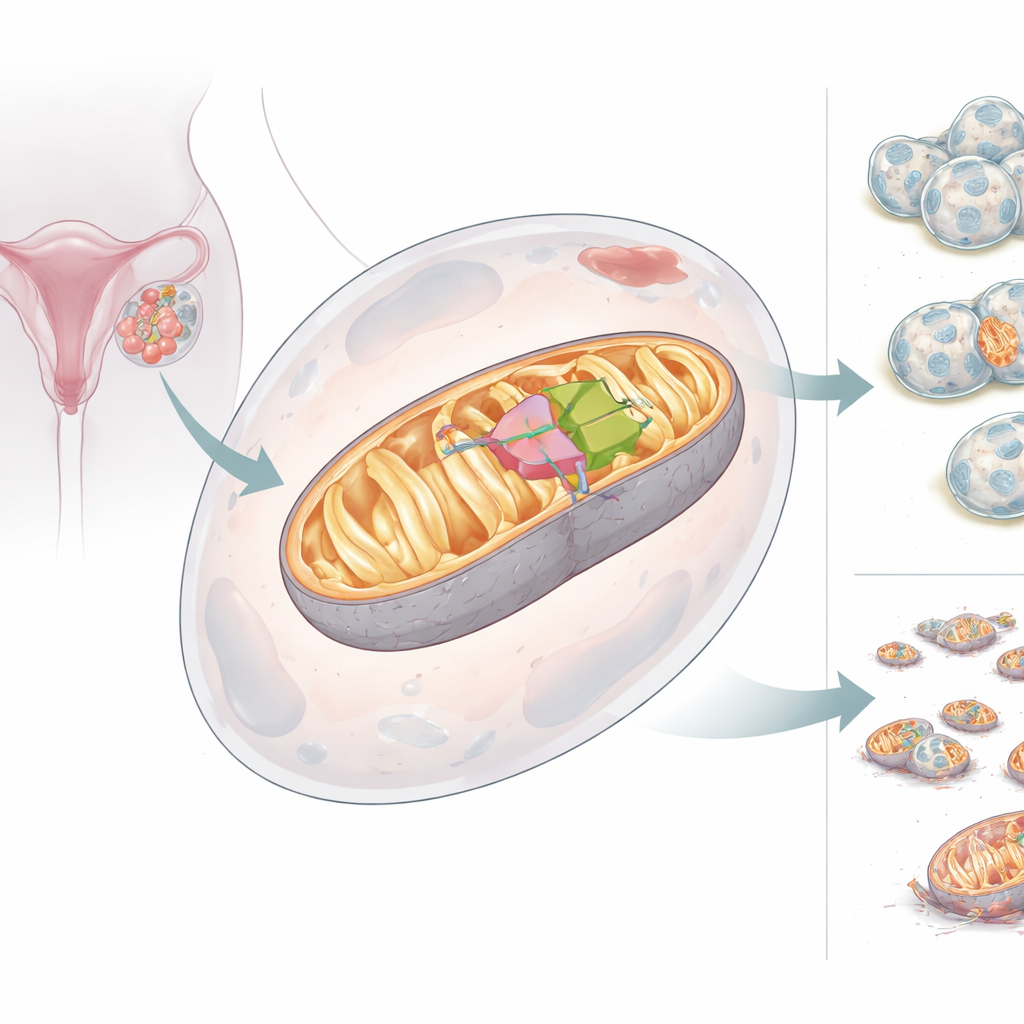
Mitokondriyal Bir Yardımcının İki Yüzü
Ekibin bulgularına göre BCS1L geni, proteinin iki versiyonunu ya da izoformunu üretebiliyor. Tam uzunluklu form olan BCS1L-L, içine mitokondriye gönderilmesini sağlayan bir adres etiketi taşır; burada Kompleks III montajını destekleyerek güçlü enerji çıktısı sağlar. Daha kısa olan BCS1L-S ise önemli bir segmentten yoksundur ve mitokondriye ulaşamaz; bunun yerine hücre özsuyunda ve çekirdekte kalır ve enerji üretimini desteklemez. Sağlıklı dokularda kısa form yaygındır, ancak over kanserlerinde denge tersine döner: uzun ve mitokondriye bağlı form baskındır. Hücreler daha fazla BCS1L-L üretmeye zorlandığında, mitokondrileri daha fazla enerji üretti, zar potansiyellerini daha iyi korudu, zararlı oksijen yan ürünleri azaldı ve hücre ölümü karşısında direnç gösterdi. BCS1L azaltıldığında ise mitokondriler parçalandı, enerji üretimi düştü, zararlı oksijen molekülleri arttı ve kanser hücreleri ölme eğilimi gösterdi.
Kanser Mesajı Nasıl Yeniden Düzenliyor?
BCS1L’in uzun ya da kısa versiyonunu üretmek, hücrenin RNA mesajını düzenleme biçimine—splicing—bağlıdır. Araştırmacılar BCS1L RNA’sına dokunan ve bu tercihi etkileyen proteinleri aradılar. Birden USP39 adlı, daha önce çeşitli kanserlerle ilişkilendirilmiş bir splicing faktörüne odaklandılar. Over kanseri hücrelerinde USP39, BCS1L’in ekson 2’si haline gelen RNA segmentinin yakınında bağlanıyor ve bu segmentin dahil edilmesini teşvik ederek uzun, mitokondri hedefli formun oluşumunu destekliyordu. USP39 susturulduğunda, hücreler bu segmenti daha sık atladı ve BCS1L-S kısa formuna kaydı. Bu kayma Kompleks III’ü zayıflattı, mitokondriyal solunumu ve ATP üretimini azalttı, oksidatif stresi artırdı ve kanser hücresi ölümünü tetikledi. Bu hücrelerde BCS1L-L’in yeniden sağlanması, mitokondriyal işlevin ve hücre sağkalımının büyük kısmını kurtardı; bu da USP39’un kritik bir mitokondriyal anahtarı büyük ölçüde BCS1L aracılığıyla yönlendirdiğini gösterdi.
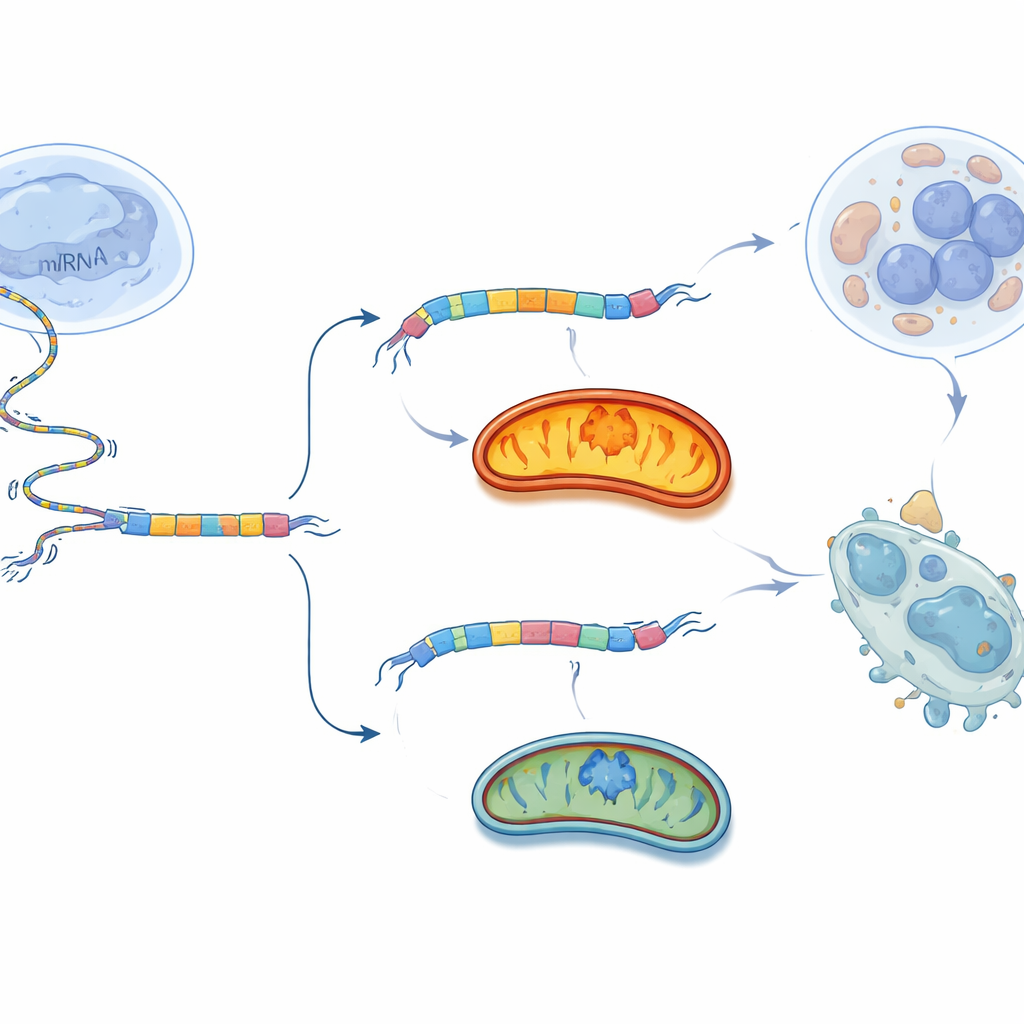
Anahtarı Tümöre Karşı Çevirmek
Mitokondrileri geniş ölçüde engellemek birçok dokuda zarar verebileceğinden, ekip daha cerrahi bir taktik denedi: doğrudan BCS1L’in ekson tercihine müdahale etmek. BCS1L RNA’sının ekson 2’sinin çevresine bağlanan antisense oligonükleotidler (ASO’lar) adı verilen kısa genetik parçacıklar tasarladılar. Bu ASO’lar, küçük mandallar gibi davranarak splicing makinesinin mesajı okuma biçimini değiştiriyor ve hücreyi ekson 2’yi atmaya teşvik ediyordu. Laboratuvarda yetiştirilen over kanseri hücrelerinde en etkili ASO, uzun BCS1L-L formunu güçlü biçimde azaltıp kısa BCS1L-S formunu artırdı. Sonuç olarak mitokondriyal solunum ve ATP üretimi düştü, zararlı oksijen seviyeleri yükseldi ve çok daha fazla hücre programlı ölüm geçirdi. Aynı ASO farelerdeki over kanseri tümörlerine enjekte edildiğinde tümör büyümesi yavaşladı ve tümörler daha hafif oldu; etki kanser hücreleri üzerinde normal fibroblastlara kıyasla çok daha belirgindi.
Bu Hastalar İçin Ne Anlama Gelebilir?
Basitçe söylemek gerekirse, bu çalışma birçok over kanserinin büyümelerini desteklemek için mitokondriyal bir yardımcı proteinin “turbo” versiyonuna dayandığını gösteriyor. Bir splicing faktörü olan USP39, hücrenin RNA düzenleme mekanizmasını bu turbo versiyonun daha fazla üretilmesine doğru eğiyor ve tümörün enerji santrallerini üst düzeyde tutuyor. Hassas biçimde tasarlanmış ASO’lar kullanılarak ekson tercihinin daha zayıf versiyona çevrilmesiyle araştırmacılar kanser hücresi mitokondrilerini seçici şekilde çökertip hücre ölümünü tetikleyebiliyor; bu sırada çoğu normal hücre daha az etkileniyor. Bu tür ASO ilaçlarının tümörlere teslimi hâlâ büyük bir zorluk olsa da, çalışma BCS1L ekson tercihi anahtarını over kanserini tedavi etmek için umut verici ve yüksek özgüllüğe sahip yeni bir hedef olarak işaret ediyor.
Atıf: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Anahtar kelimeler: over kanseri, mitokondri, RNA ekson tercihi (splicing), BCS1L, antisense oligonükleotidler