Clear Sky Science · tr
NSD2, oksidatif fosforilasyon aracılığıyla PD-L1 ifadesini baskılayarak hepatoselüler karsinomda bağışıklık gözetimini kontrol eder
Bu karaciğer kanseri öyküsü neden önemli
Hepatoselüler karsinom, karaciğer kanserinin en yaygın biçimi, çoğunlukla geç evrede teşhis ediliyor ve birçok tedaviye direnç gösteriyor. Tümör hücrelerindeki PD-L1 “görünmezlik pelerini”ni engelleyen immünoterapi ilaçları bazı hastalara yardımcı oluyor, ama çoğuna değil. Bu çalışma, karaciğer kanseri hücrelerinin enerji üretimini bağışıklık sistemi tarafından ne kadar görünür olduklarıyla ilişkilendiren beklenmedik bir oyuncu olan NSD2 adlı bir proteini ortaya koyuyor. Bu bağlantının anlaşılması, mevcut tedavileri güçlendirecek yeni yaklaşımlara ve hangi hastaların fayda görme olasılığının yüksek olduğunun belirlenmesine işaret edebilir.
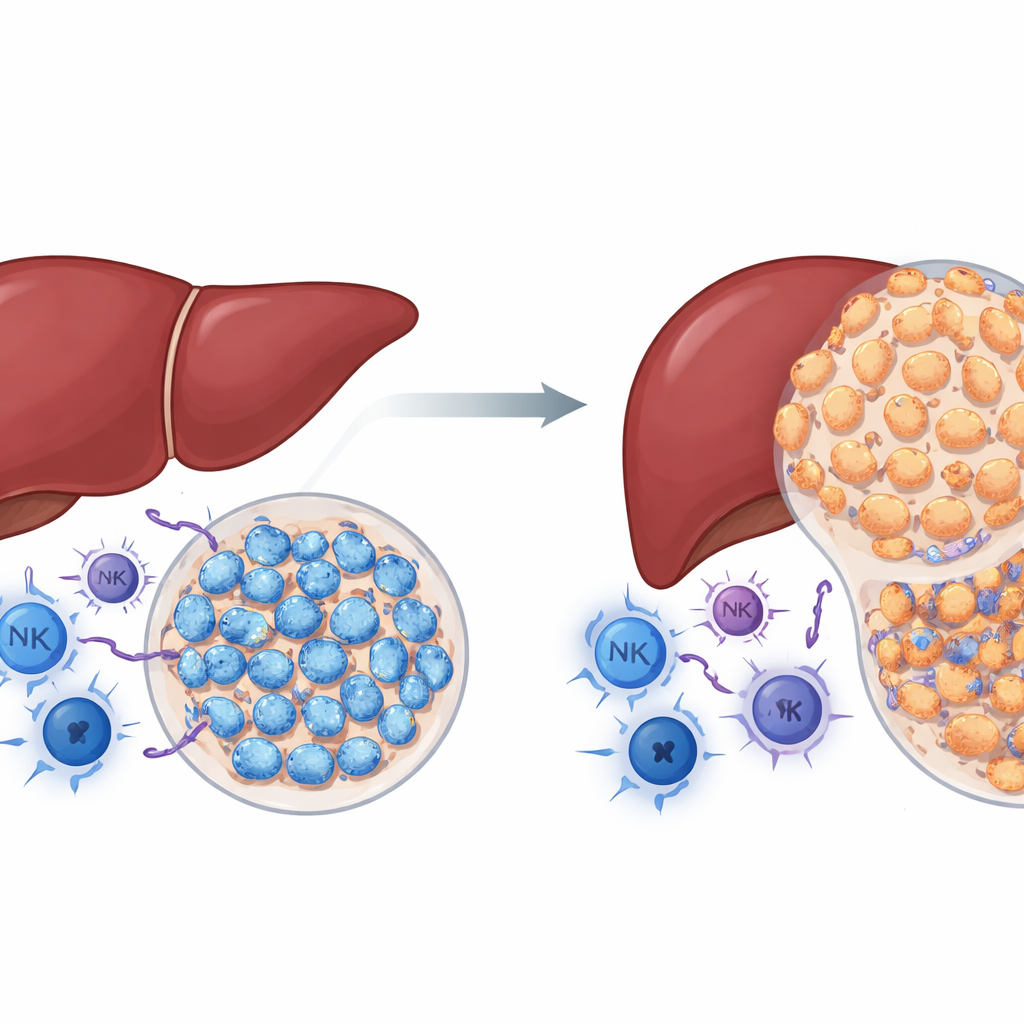
Bilinen bir kanser proteini için şaşırtıcı bir rol
NSD2, DNA’nın sarılı olduğu histonları değiştiren bir enzimdir. Pek çok kanserde NSD2, tümör büyümesini destekleyen bir etken olarak değerlendirilmiştir. Yazarlar, aynı şeyin karaciğer kanseri için de geçerli olup olmadığını sordular. NSD2’nin sadece karaciğer hücrelerinde aktif hale getirildiği genetik olarak tasarlanmış fareleri kullanarak, hayvanlara güvenilir şekilde karaciğer tümörleri oluşturan bir kimyasal verdiler. Beklentilerin aksine, fazla NSD2’ye sahip farelerde normal farelere göre çok daha az ve daha küçük tümörler gelişti; ayrıca karaciğerlerinde daha az hasar, skarlaşma ve hücre proliferasyonu gözlendi. Aynı zamanda, NSD2 fazla ifade edilen karaciğerlerden kaynaklanan tümörler, yardımcı ve katil T hücreleri ile doğal öldürücü hücreler de dahil olmak üzere daha fazla kanserle savaşan bağışıklık hücresi içeriyordu. Bu bulgular, sağlam bir bağışıklık sistemi varlığında NSD2’nin karaciğer kanserinde hızlandırıcıdan çok fren gibi davrandığını düşündürdü.
Tümör hücrelerinde enerji fabrikaları ve yakıt kullanımı
NSD2’nin tümörleri nasıl kısıtladığını anlamak için ekip, karaciğer dokusunda gen aktivitesi profillemesi yaptı. NSD2 fazla ifadesinin, mitokondrilerin—hücrenin “enerji santralleri”—oksijen kullanarak enerji ürettiği süreç olan oksidatif fosforilasyonla ilgili genleri güçlü şekilde baskıladığını buldular. Fare ve insan karaciğer kanseri hücre hatlarında yapılan takip deneyleri, NSD2 arttırıldığında birçok oksidatif fosforilasyon geninin ifadesinin düştüğünü, oksijen tüketiminin ve ATP üretiminin azaldığını ve mitokondriyal zar potansiyelinin düştüğünü (zayıf mitokondriyal aktivitenin bir göstergesi) gösterdi. Aynı zamanda bu hücreler daha az glikoz tüketti fakat enerji ihtiyaçlarını glikolize kaydırmadılar; bu da net bir enerji çıktısı azalması olduğunu gösteriyor. NSD2 kaybı ise ters etkiyi yaparak mitokondriyal gücü ve yakıt kullanımını güçlendirdi.
NSD2 enerji ve bağışıklık görünürlüğünü nasıl yeniden düzenliyor
Daha derine inerek, araştırmacılar genom çapında kromatin haritalama ile gen ifade verilerini birleştirdiler ve NSD2 varlığında doğrudan aktive edilen bir gen seti belirlediler. Bunlardan ikisi, Camk2d ve Prkce, mitokondriyal aktiviteyi kısıtladıkları bilinen genlerdi. NSD2, bu genlerin promotörlerinde belirli bir histon işaretini (H3K36me2) artırdı ve bunların ifadesini yükseltti. Bu genleri NSD2 eksikliği olan karaciğer kanseri hücrelerine yeniden sokmak, mitokondriyal oksijen kullanımını ve ATP üretimini azalttı; bu, bunların NSD2’nin oksidatif fosforilasyon üzerindeki aşağı akış frenleri olarak işlev gördüğünü doğruladı. Önemli olarak, önceki çalışmalar yüksek mitokondriyal aktivitenin tümör hücrelerinde yüksek PD-L1’i desteklediğini öne sürmüştü. Buna uygun olarak, yazarlar NSD2’nin aşırı ifadesinin PD-L1 düzeylerini azalttığını, NSD2 kaybının ise karaciğer kanseri hücrelerinde ve tümör dokusunda PD-L1’i artırdığını buldular.
Kalkanı kısmak ve bağışıklık saldırısını uyandırmak
Bu moleküler değişimlerin işlevsel etkisi, NSD2’yi kazanacak veya kaybedecek şekilde genetik olarak değiştirilmiş kanser hücrelerinin karaciğere enjekte edildiği farelerde test edildi. NSD2 eksik hücreler hızla daha büyük tümörler oluşturdu, daha fazla PD-L1 ifade etti ve özellikle etkin katil T hücreleri olmak üzere daha az T hücresi ve doğal öldürücü hücre ile infiltre oldu. Araştırmacılar mitokondriyal oksidatif fosforilasyonun önemli bir bileşeni olan kompleks V’yi kimyasal olarak bloke ettiğinde, NSD2 eksik hücrelerde PD-L1 düzeyleri normale doğru düştü ve bağışıklık hücreleri tümör hücresi ölümünü daha iyi indükleyebildi. Benzer şekilde, NSD2 eksik hücrelerde Camk2d veya Prkce’nin aşırı ifade edilmesi ya da tümörlerin PD-L1’i engelleyen bir antikorla tedavi edilmesi, tümör boyutunu azalttı ve bağışıklık hücresi infiltrasyonunu geri getirdi. Hasta veri setlerinde düşük NSD2 ifadesi daha kötü sağkalım ile ilişkilendirildi, ancak ilginç bir şekilde PD-L1 hedefli tedaviye daha iyi yanıtla da bağlantılıydı; bu da NSD2 durumunun hangi hastaların bu tür ilaçlardan fayda görebileceğini tahmin etmeye yardımcı olabileceğini düşündürüyor.
Gelecekteki karaciğer kanseri bakımına ne anlama geliyor
Genel okuyucu için temel mesaj, bu çalışmanın NSD2’yi, en azından çalışan bir bağışıklık sistemi varlığında, karaciğer kanserinde tümör baskılayıcı bir faktör olarak yeniden tanımladığıdır. Hücrenin oksijen tabanlı enerji üretimini düşürerek NSD2, dolaylı yoldan tümör hücrelerindeki PD-L1’i azaltır; böylece onların görünmezlik pelerinlerinden bir kısmını kaldırır ve bağışıklık hücrelerinin onları tanıyıp saldırmasına izin verir. Yeni tanımlanan bu NSD2–enerji–PD-L1 zinciri iki pratik fikri öneriyor: birincisi, tümörleri NSD2 eksik olan hastaların PD-L1’i bloke eden ilaçlar için özellikle iyi adaylar olabileceği; ikincisi, mitokondriyal enerji üretimini engelleyen ilaçların immünoterapi ile birleştirilmesinin karaciğer kanserine karşı güçlü bir kombinasyon sağlayabileceğidir.
Atıf: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Anahtar kelimeler: hepatoselüler karsinom, NSD2, oksidatif fosforilasyon, PD-L1, tümör immünoterapisi