Clear Sky Science · tr
DNMT2, 5’tiRNAGly-GCC üretimini düşürerek anaplastik tiroid kanseri ilerlemesini engelliyor
Bu gizli RNA kimyası neden önemli
Anaplastik tiroid kanseri, cerrahi, radyasyon ve kemoterapiye rağmen hastaları aylar içinde öldürebilen en ölümcül insan kanserlerinden biridir. Bu çalışma, kanser hücrelerinin derinliklerinde beklenmedik bir suçlu ortaya koyuyor: protein yapımına yardımcı olan transfer RNA’ların üzerine konan küçük kimyasal işaretler. Yazarlar, belirli bir enzim olan DNMT2 kaybolduğunda veya azaldığında tiroid tümörlerinin daha hızlı büyüdüğünü, daha kolay yayıldığını ve yaygın kemoterapi ilacı doksorubisine karşı daha dirençli hâle geldiğini gösteriyor. Daha da ilginci, DNMT2 düşük olduğunda ortaya çıkan küçük bir RNA fragmanını saptıyorlar ve bu fragmanı engellemenin yeni bir tedavi stratejisi olabileceğini gösteriyorlar.
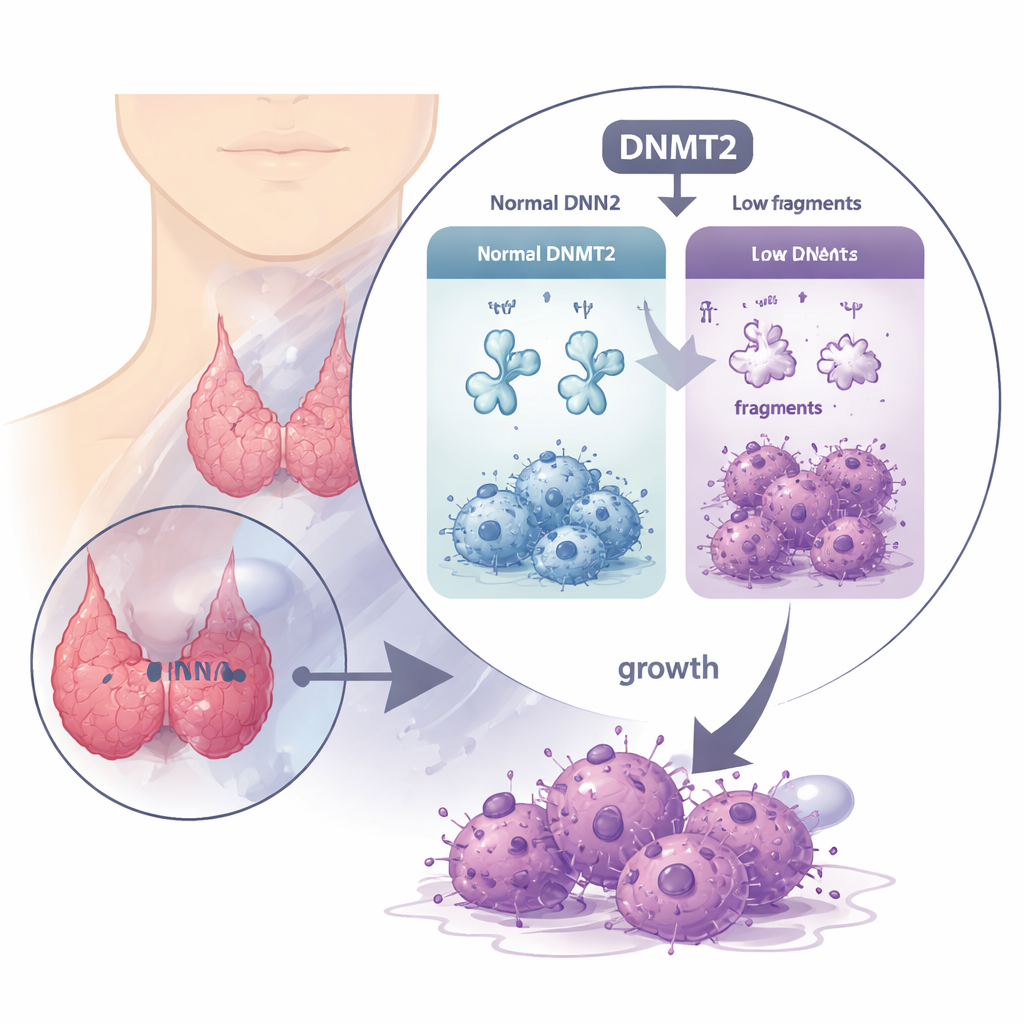
Kayıp olan koruyucu enzim
Transfer RNA’lar (tRNA’lar) normalde amino asitleri hücrenin protein yapım makinesine taşır ve kararlılıkları hassas kimyasal süslemelere bağlıdır. DNMT2, tRNA’nın belirli bölgelerine metil adı verilen bir işaret ekleyen bir enzimdir. Pek çok kanserde DNMT2 seviyeleri yükselmiş ve tümörlere yardımcı olduğu düşünülmüş olsa da burada durum tersine dönüyor. Geniş hasta veri kümeleri ve tümör örneklerini analiz ederek, araştırmacılar DNMT2 seviyelerinin anaplastik tiroid kanseri dokusunda normal tiroide göre anlamlı şekilde daha düşük olduğunu buldular. Tümörlerinde daha yüksek DNMT2 olan hastalar, kanserlerinin kötüleşmeden daha uzun süre yaşama eğilimindeydi; bu da DNMT2’nin bu hastalıkta hızlandırıcıdan çok fren gibi davrandığını düşündürüyor.
Düşük DNMT2’nin agresif davranışı nasıl beslediği
DNMT2’nin kanser hücrelerinde gerçekte ne yaptığını görmek için ekip, anaplastik tiroid kanseri hücre hatlarında ve fare modellerinde DNMT2 düzeylerini değiştirdi. DNMT2 azaldığında hücreler daha hızlı çoğaldı, zarları daha kolay delebildi ve daha fazla koloni oluşturdu; bunların hepsi agresif bir tümörün ayırt edici özellikleri. Bu hücreler ayrıca standart bir ilaç olan doksorubisine karşı daha az duyarlı hâle geldi. Farelerde DNMT2’si azaltılmış şekilde tasarlanmış tümörler daha büyük büyüdü ve akciğere daha kolay yayıldı; tersine DNMT2 ifadesini artırmak tam tersine etki yaptı. Araştırmacılar bu değişiklikleri kısmen epitel–mezenkimal geçiş (EMT) olarak bilinen ve kanser hücrelerini daha hareketli ve invaziv yapan bir hücresel programın aktivasyonuna bağladılar.
Hasarlı tRNA’dan zararlı küçük parçacıklara
Daha derine inildiğinde çalışma, DNMT2’nin yalnızca üç tRNA türünde belirli bir pozisyonda (C38 olarak adlandırılan) metil işareti koyduğunu gösteriyor. Bu koruma olmadan, tRNA’lar diğer bir enzim olan angiogenin tarafından kesilmeye daha açık hâle geliyor. Bu kesim, tRNA-Gly-GCC’den türeyen kısa bir RNA parçası olan 5’tiRNAGly-GCC’yi üretiyor. Dizileme ve biyokimyasal testlerle yazarlar, DNMT2 düşük olduğunda özellikle glisin taşıyan tRNA’dan gelen bu fragmanın biriktiğini buldular. Test tüpü deneylerinde metil işaretinin eklenmesi, tRNA’nın dilimlenmesinden güçlü şekilde korudu; bu da DNMT2’nin normalde bu molekülleri daha küçük, potansiyel olarak zararlı parçalara ayrılmaktan koruduğunu doğruluyor.
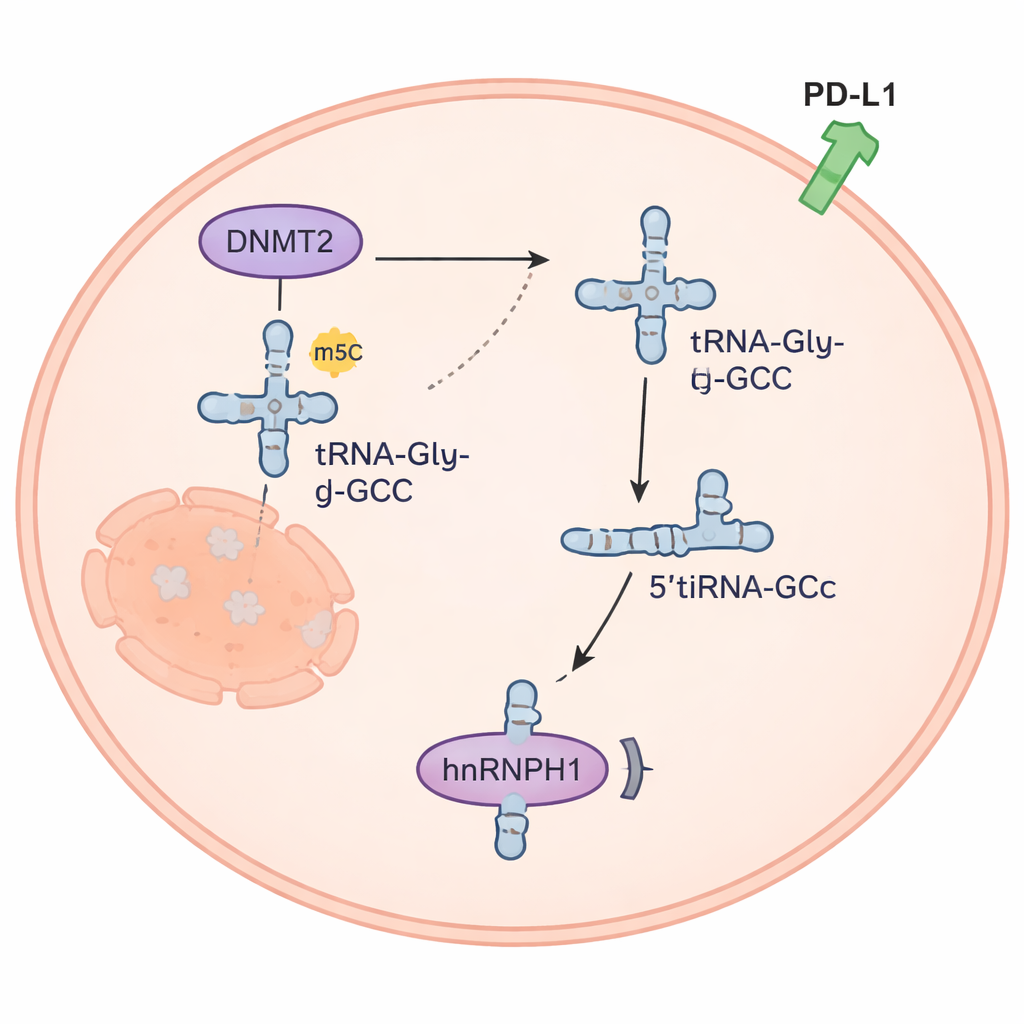
Çok küçük bir RNA fragmanı kanser sinyallerini yeniden düzenliyor
5’tiRNAGly-GCC fragmanı moleküler bir artık olmanın ötesine geçti. Anaplastik tiroid kanseri hücrelerinde bol bulunurken normal tiroid hücrelerinde nadirdi. Araştırmacılar seviyesini yapay olarak artırdıklarında, kanser hücreleri daha hızlı çoğaldı, daha fazla invaze oldu ve doksorubisine daha dirençli hâle geldi; fragmanı düşürmek ters etkiyi gösterdi. Farelerde 5’tiRNAGly-GCC’ye yönelik kimyasal olarak tasarlanmış bir inhibitör tümör büyümesini yavaşlattı ve bu inhibitör ile doksorubinin kombinasyonu tek başına uygulanan her iki tedaviden daha iyi sonuç verdi. Ekip, 5’tiRNAGly-GCC’nin hnRNPH1 adlı bir proteine bağlandığını ve hücre içindeki miktarını azalttığını keşfetti. hnRNPH1 normalde bağışıklıkla ilgili PD-L1 proteininin seviyelerini kontrol altında tutmaya yardımcı olduğundan, hnRNPH1 kaybı PD-L1’in yükselmesine izin veriyor; bu değişiklik tümörlerin bağışıklıktan kaçmasına yardımcı olabilir ve tümör çevresinde düzenleyici T hücre birikimiyle ilişkilendiriliyor.
Gelecek tedaviler için anlamı
Basitçe ifade etmek gerekirse, çalışma şu zincirleme reaksiyonu ortaya koyuyor: DNMT2 düşük olduğunda, belirli tRNA’lar koruyucu bir işareti kaybediyor, küçük parçalara kesiliyor ve bu parçalardan biri (5’tiRNAGly-GCC) PD-L1’i sınırlayan bir proteini devre dışı bırakıyor. Sonuç daha agresif, ilaç direncine sahip ve bağışıklıktan kaçan bir kanser. DNMT2’yi doğrudan artırmaya çalışmak—ki bu diğer dokularda riskli olabilir—yerine yazarlar zararlı RNA fragmanını hedeflemenin daha uygun olabileceğini öneriyor. Fare deneyleri, özellikle 5’tiRNAGly-GCC inhibitörünün doksorubin ile birlikte kullanıldığında, bu mikroskobik RNA devrelerini kesmenin tiroid kanserinin en ölümcül biçimlerinden birini kontrol altına almaya yardımcı olabileceğine dair erken kanıt sağlıyor.
Atıf: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Anahtar kelimeler: anaplastik tiroid kanseri, DNMT2, tRNA parçacıkları, kemorezistans, PD-L1