Clear Sky Science · tr
Mitozom fosfatazı PGAM5’i hedeflemek, NRF2 aracılı FSP1 ifadesini yukarı çekerek ferroptozu ve akut pankreatiti hafifletir
Neden stres altındaki hücreler ve ağrılı pankreaslar önemli?
Hücreler aşırı zorlandığında, tüm vücuda zarar veren biçimlerde ölebilirler. Ferroptoz adı verilen bu hücre ölümü türü, demir ve hücre zarlarındaki yağların “paslanmasına” yol açan kontrolsüz kimyasal reaksiyonlarla yönlendirilir. Bu süreç, ağrılı ve bazen ölümcül olabilen akut pankreatit de dahil olmak üzere organ hasarlarıyla ilişkilendirilmiştir. Bu makalenin dayandığı çalışma, hücrelerin enerji santralleri olan mitokondriler içinde ferroptozu artırıp azaltabilen kilit bir kontrol düğmesini ortaya çıkarıyor ve bu düğmeyi engellemenin fare modelinde pankreası nasıl koruyabildiğini gösteriyor.
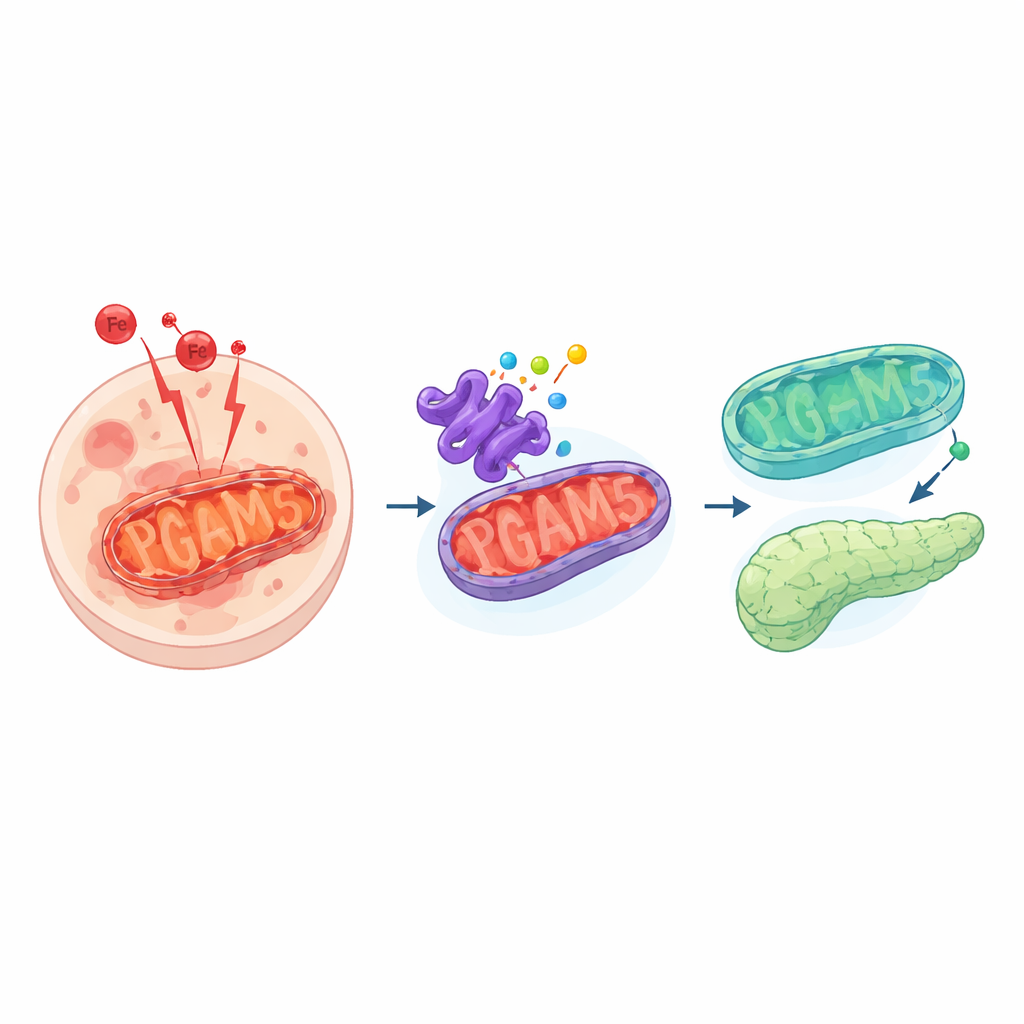
Tehlikeli bir hücre ölümü biçimi
Ferroptoz, apopitoz gibi daha tanıdık hücre ölümü biçimlerinden farklıdır. Düzenli bir kendi kendine yıkım yerine, ferroptoz geçiren hücreler zarlarındaki hassas yağların bozulmasına yol açan demir kaynaklı bir reaksiyon fırtınası yaşarlar. Bu durum toksik yan ürünler ve zamanla hücreyi öldüren zar delinmeleri oluşturur. Genellikle hücreler, bu reaktif molekülleri detoksifiye eden koruyucu sistemlerle bunu kontrol altında tutar. Bu sistemler başarısız olduğunda veya baskılandığında, ferroptoz dokulara yayılarak kanserden organ yetmezliğine kadar çeşitli hastalıklara katkıda bulunabilir.
Hedefte bir mitokondri anahtarı
Araştırmacılar, mitokondrinin iç yüzünde bulunan ve bir sinyal merkezi gibi davranan PGAM5 adlı bir proteine odaklandı. PGAM5, mitokondri şeklinin kontrolüne yardımcı olur, strese yanıt verir ve hücrelerin oksidasyonla nasıl başa çıktığını etkiler. İlginç bir şekilde, ekip PGAM5’i ya azaltınca ya da fazla üretimini zorlayınca hücreler ferroptozla öldürülmeye daha dirençli hâle geldi. PGAM5’in kimyasal olarak inhibe edilmesi, genetik baskılanması ve aşırı eksprese edilmesi, zararlı lipid yan ürünlerinin birikimini azalttı ve ferroptozu tetikleyen bir ilaçla tetiklenen hücre ölümünü düşürdü. Bu bulgu, sistemin hassas bir dengede olduğunu gösteriyor: hem çok az hem de çok fazla PGAM5, hücreleri daha korunaklı bir duruma itiyor.
İçsel bir kalkanın devreye girmesi
Daha derine inildiğinde, PGAM5’in etkisinin NRF2 ve FSP1 adında iki diğer oyuncuyu içeren koruyucu bir eksen aracılığıyla gerçekleştiği keşfedildi. NRF2, nükleusta aktif olduğunda geniş bir antioksidan savunma programını açan ana düzenleyicidir. FSP1, membrandaki lipid hasarını engelleyen yağda çözünebilen bir antioksidantı yenileyen aşağı akım savunucularından biridir. PGAM5 düzeyleri değiştirildiğinde hücreler NRF2’nin hem mesaj hem de protein düzeylerini artırdı ve NRF2 sitoplazmadan nükleusa daha kolay taşındı. Orada FSP1 üretimini yükseltti. FSP1 ya da NRF2 engellendiğinde koruma ortadan kalktı ve ferroptoz hassasiyeti geri geldi; bu da PGAM5–NRF2–FSP1 zincirinin gözlemlenen direnci için elzem olduğunu gösteriyor.
Gizli habercinin enerji stresi olması
Çalışma ayrıca mitokondri stresinin bu koruyucu yanıta nasıl dönüştüğünü ortaya koydu. PGAM5’in bozulması mitokondri dengesini bozdu ve hücrenin enerji parası olan moleküllerin oranını değiştirdi: düşük enerjili moleküller (AMP ve ADP) ile yüksek enerjili ATP arasındaki oran yükselerek enerji stresini işaret etti. Bu da enerji algılayıcı enzim AMPK’yi aktive etti. Aktifleşmiş AMPK, NRF2’yi nükleusa girişini teşvik edecek şekilde doğrudan modifiye etti ve böylece FSP1 üretimini daha da artırdı. AMPK sistemden çıkarıldığında NRF2 artık nükleusta birikmedi, FSP1 seviyeleri düştü ve hücreler yeniden ferroptoza yenildi. Böylece PGAM5, mitokondri durumunu enerji ve antioksidan yanıtına bağlayarak hücreleri demir kaynaklı ölümlerden koruyan bir köprü oluşturuyor.
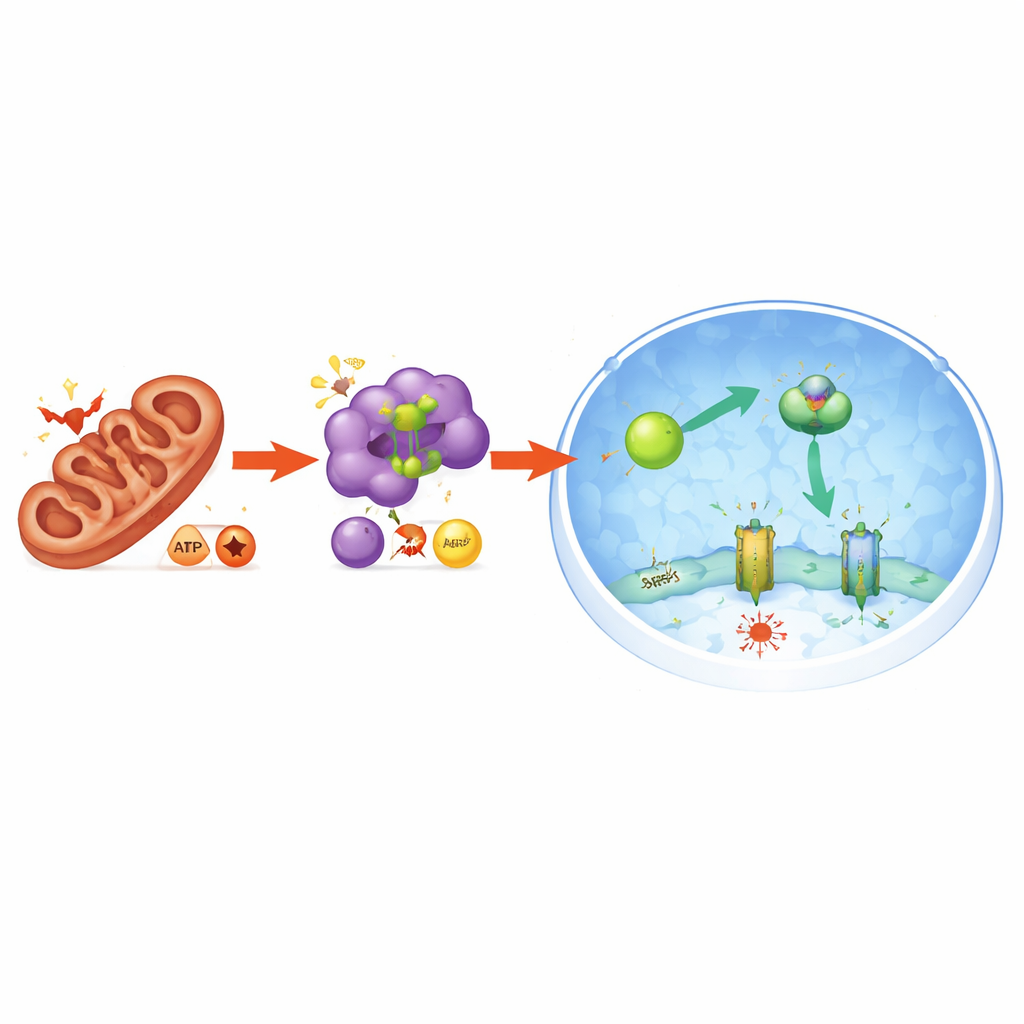
Canlı hayvanlarda pankreası korumak
Bu mekanizmanın bütün bir organ için anlamlı olup olmadığını test etmek üzere bilim insanları, yüksek doz arginin amino asidi ile tetiklenen akut pankreatit fare modeline yöneldi. Bu modelde pankreas yaygın hasar, doku yaralanmasını gösteren yükselmiş kan enzimleri ve artan iltihap belirteçleri sergiliyor. Lipid peroksidasyon belirteçleri—ferroptozun bir imzası—pankreasta keskin biçimde yükseldi. Farelere PGAM5’i inhibe eden bir bileşik verildiğinde bu belirtiler hafifledi: kan hasar belirteçleri düştü, pankreas dokusu mikroskop altında daha sağlıklı görünmeye başladı ve iltihap sinyalleri azaldı. Aynı zamanda ferroptoz belirteçleri geriledi, AMPK aktivitesi ile NRF2 ve FSP1 seviyeleri pankreasta arttı; bu da hücre kültüründe görülen koruyucu yolakla örtüştü.
Gelecekteki tedaviler için ne anlama geliyor?
Toplu olarak ele alındığında bu çalışma, mitokondri stresi, hücresel enerji durumu ve ferroptozu engelleyen güçlü bir antioksidan program arasında bağlantı kuran merkezi bir kontrol noktası olarak PGAM5’i tanımlıyor. PGAM5 aktivitesini azaltarak hücreler AMPK ve NRF2’yi etkinleştiriyor, FSP1’i artırıyor ve demir kaynaklı lipid hasarına karşı daha iyi dayanıyor. Farelerde bu strateji akut pankreatitte pankreatik hasarı hafifletiyor. Halka yönelik bir özetle, araştırmacıların yıkıcı bir hücre ölüm biçimini önleyebilecek yeni bir iç “devre kesici” bulduklarını söyleyebiliriz. Klinik uygulamaya geçmeden önce yapılması gereken çok iş olsa da, PGAM5’i veya onun aşağı akım ortaklarını hedeflemek ferroptoz ve mitokondri yetmezliğinin zararlı rol oynadığı durumların tedavisinde yeni yollar açabilir.
Atıf: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Anahtar kelimeler: ferroptoz, mitokondri, akut pankreatit, oksidatif stres, hücre ölümü