Clear Sky Science · tr
UBE3A aracılı mH2A1 Ubiquitinasyonu, TERT transkripsiyonunu aktive ederek pankreas kanserinde yaşlanmaya direnç sağlar
Bu araştırma hastalar için neden önemli
Pankreas kanseri, kısmen tümör hücrelerinin vücudun doğal yaşlanma frenlerinden alışılmadık derecede iyi kaçabilmesi nedeniyle en ölümcül kanserler arasında yer alır. Bu çalışma, pankreas kanseri hücrelerinin genç kalmasına, bölünmeye devam etmesine ve tedaviye direnç göstermesine yardımcı olan gizli bir moleküler “sabotaj devresini” ortaya koyuyor. Araştırmacılar bu devreyi anlayarak, bu hücreleri yaşlanmaya itmenin ve ardından selektif olarak temizlemenin yeni bir yolunu işaret ediyor; bu da daha akıllı, kombinasyonel tedavilere kapı açıyor.
Vücudun doğal tümör freni olarak yaşlanma
Tüm hücreler sonunda bölünmeyi durduran bir iç saate sahiptir; bu sürece senesans denir. Erken pankreatik lezyonlarda bu saat, prekansere hücreleri kalıcı emekliliğe göndererek tümör gelişimini yavaşlatabilir. Birçok anticancer tedavi de kısmen tümör hücrelerini bu yaşlı duruma zorlayarak etki gösterir. Ancak bu senescent hücreler temizlenmezse iltihabı körükleyebilir ve kanserin geri gelmesine katkıda bulunabilir. Bu da yeni bir tedavi fikrini doğurdu: önce kanser hücrelerini senesansa it, sonra bu yaşlanmış hücreleri onlara özel toksik etkiye sahip “senolitik” ilaçlarla ortadan kaldır.
Odakta kanseri destekleyen bir enzim
Pankreas kanseri hücrelerinin senesansı yenmesine yardımcı olan genleri bulmak için ekip büyük hasta veri setlerini taradı ve bulgularını tümör örnekleri ve hücre hatlarında doğruladı. UBE3A adlı, diğer proteinleri yok edilmek üzere işaretleyen bir enzimde yoğunlaştılar. UBE3A düzeyleri pankreas tümörlerinde çevre normal dokuya kıyasla çok daha yüksekti ve daha fazla UBE3A’ya sahip hastalar genellikle daha büyük, daha ileri evre kanserlere ve daha kötü sağkalıma sahipti. Laboratuvarda UBE3A’yı arttırmak büyümeyi hızlandırdı, hücresel yaşlanmanın klasik belirteçlerini azalttı ve senescent hücrelere özgü inflamatuar salgıları kesti. UBE3A’nın susturulması ise ters etki yaptı ve fare modellerinde tümör büyümesini ve karaciğer metastazını keskin biçimde azalttı. 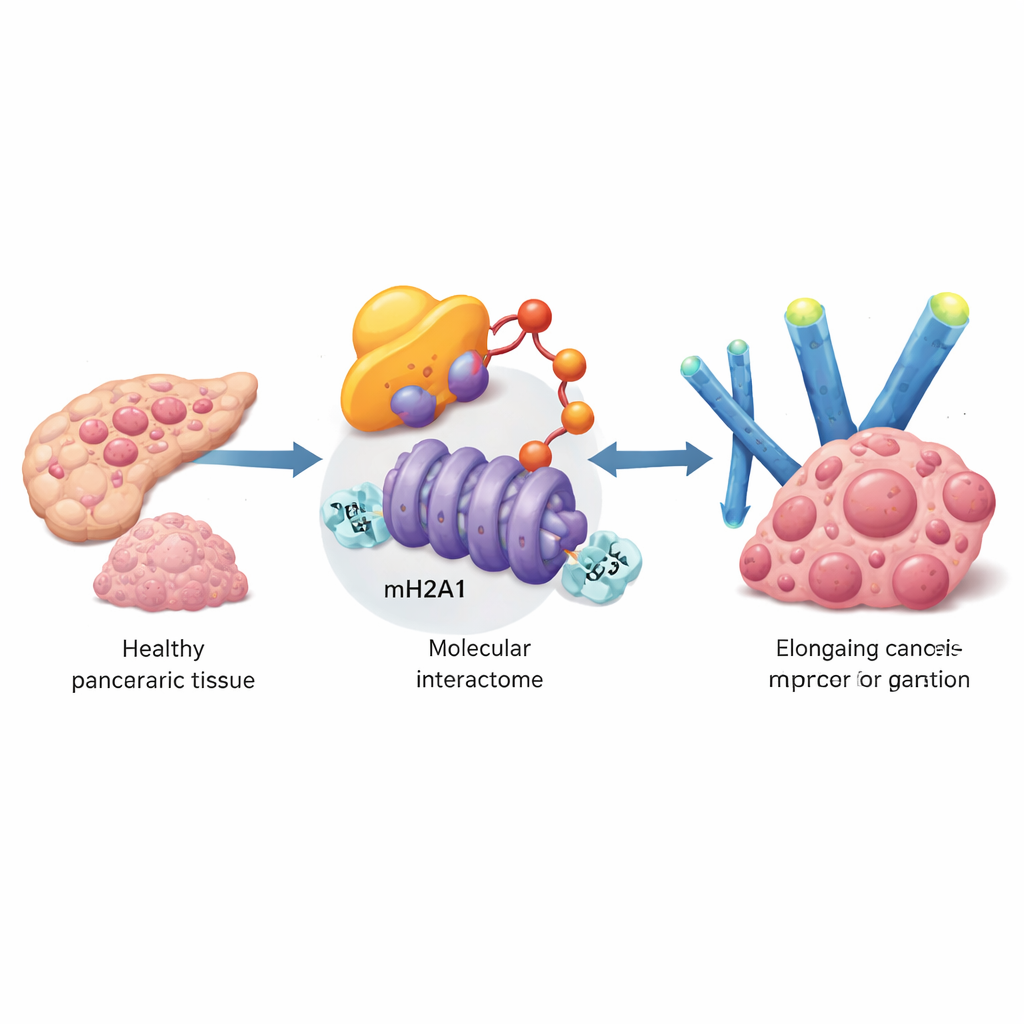
Kanser hücrelerinin kromatin frenini nasıl sildiği
Daha derine indiklerinde, UBE3A’nın hangi moleküller üzerinde etkili olduğunu sordular. İleri kütle spektrometrisi taramaları kullanarak UBE3A’nın makroH2A1 (mH2A1) adlı özel bir histon varyantına bağlandığını ve onu kimyasal olarak işaretlediğini buldular. mH2A1 DNA’yı sıkıştırmaya yardımcı olur ve gen aktivitesi üzerinde genellikle bir fren görevi görür. UBE3A, mH2A1’e belirli bir konumda “beni yok et” zincirleri takar ve bunun sonucunda hücrenin protein imha mekanizması tarafından parçalanır. Pankreas tümörlerinde UBE3A yüksek olduğunda mH2A1 düzeyleri daha düşük bulundu ve mH2A1’i geri vermek UBE3A’nın senesansı engelleme ve tümör büyümesini teşvik etme kabiliyetini karşı koydu. Bu, önemli bir adımı ortaya koyuyor: pankreas kanseri hücreleri, mH2A1’i ortadan kaldırmak için UBE3A’yı kullanarak koruyucu bir kromatin işaretini silerler.
Hücreleri genç tutmak için telomerazı açmak
Sıradaki soru, mH2A1 kaldırıldığında hangi genlerin serbest kaldığıydı. RNA dizileme ve DNA-bağlanma haritalarını birleştirerek ekip, telomeraz geni TERT’i merkezi bir hedef olarak tanımladı. Telomeraz, kromozom uçlarındaki koruyucu kapakları (telomerleri) korur; bu sayede hücreler senesansa girmek yerine bölünmeye devam edebilir. Çalışma, mH2A1’in normalde TERT geninin içinde bir güçlendirici bölgede bulunduğunu ve burada başka bir enzim olan EZH2’yi yakın histonlara baskıcı bir kimyasal işaret koyması için işe aldığını gösteriyor. Bu kombinasyon TERT’i düşük tutar ve telomerlerin kısalmasına izin verir. UBE3A mH2A1’i yok ettiğinde, baskıcı kompleks çözülür, güçlendirici aktif hale gelir, TERT açılır, telomerler korunur ve pankreas kanseri hücreleri yaşlanmaya karşı direnç kazanır. Protein etiketleyemeyen UBE3A mutantları veya etiketlenemeyen mH2A1 mutantları bu devreyi bozar ve senesans frenini geri getirir.
Senesansın başlatılması ile senolitik temizliğin eşleştirilmesi
Son olarak, araştırmacılar bu yolun terapötik olarak kullanılabileceğini test ettiler. UBE3A’yı kapatmak pankreas kanseri hücrelerini senesansa itti ve onların BCL‑2 ailesine ait anti‑ölüm proteinlerine bağımlılığını artırdı—bu, senescent hücrelerin bilinen bir zaafıdır. Ekip daha sonra UBE3A inhibisyonunu, bu hayatta kalma proteinlerini hedef alan bir senolitik ilaç olan ABT‑263 ile birleştirdi. Kültürde, kombinasyon her iki tedaviden tek başına olandan daha fazla kanser hücresinin programlı hücre ölümüne gitmesine neden oldu. Fare modellerinde ise UBE3A azaltılmış tümörler, hayvanlara ABT‑263 verildiğinde daha da küçüldü ve tümör içindeki hücre çoğalması belirteçleri keskin şekilde düştü. 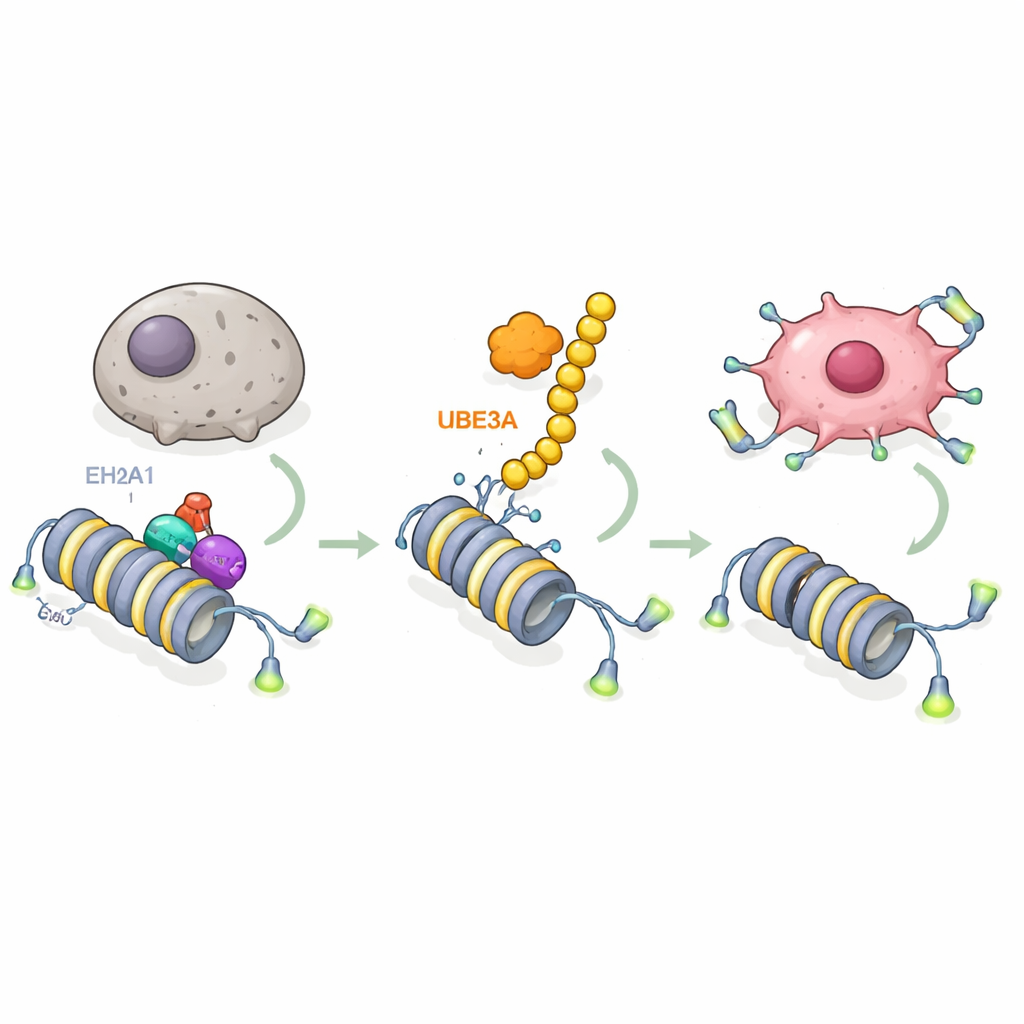
Gelecek tedaviler için bunun anlamı
Bu çalışma, pankreas kanseri hücrelerinin yaşlanmaktan kaçınmasını sağlayan ayrıntılı bir olay zincirini ortaya koyuyor: UBE3A, kromatin fren mH2A1’i yok ediyor; bu da telomeraz geni TERT’in baskısının kalkmasına ve telomerlerin korunmasına yol açarak hücrelerin bölünmeye devam etmesini sağlıyor. UBE3A’yı hedefleyerek doktorlar hücrenin doğal yaşlanma programını yeniden devreye sokabilir ve ardından ABT‑263 gibi senolitik ilaçlarla bu savunmasız, yaşlanmış kanser hücrelerini seçici olarak ortadan kaldırabilir. Bu mekanizmanın hasta tedavilerine çevrilmesi için daha fazla çalışma gerekmekle birlikte, UBE3A–mH2A1–TERT ekseni, en dirençli kanserlerden birine yönelik umut verici yeni bir müdahale noktası sunuyor.
Atıf: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Anahtar kelimeler: pankreas kanseri, hücresel yaşlanma, telomeraz, ubiquitin ligaz, senolitik tedavi