Clear Sky Science · tr
ARF GTPaz proteini 1’in küçük moleküllü bir inhibitörünün karaciğer ve kolon kanseri hücre büyümesi ile metastazını sınırlaması
Bu araştırma neden önemli
Karaciğer ve kolon kanserleri en ölümcül tümörler arasında yer alır ve mevcut tedaviler genellikle tümörleri küçültürken ağır yan etkilere yol açar. Bu çalışma, hızla çoğalan hücreleri zehirlemek yerine kanser hücrelerinin içine girip büyümek ve yayılmak için güvendikleri bir protein “kontrol merkezini” söküp ayıran yeni bir ilaç türünü araştırıyor. Bu merkeze odaklanarak deneysel bileşik, sağlıklı dokuyu korurken tümör büyümesini yavaşlatmayı hedefliyor.
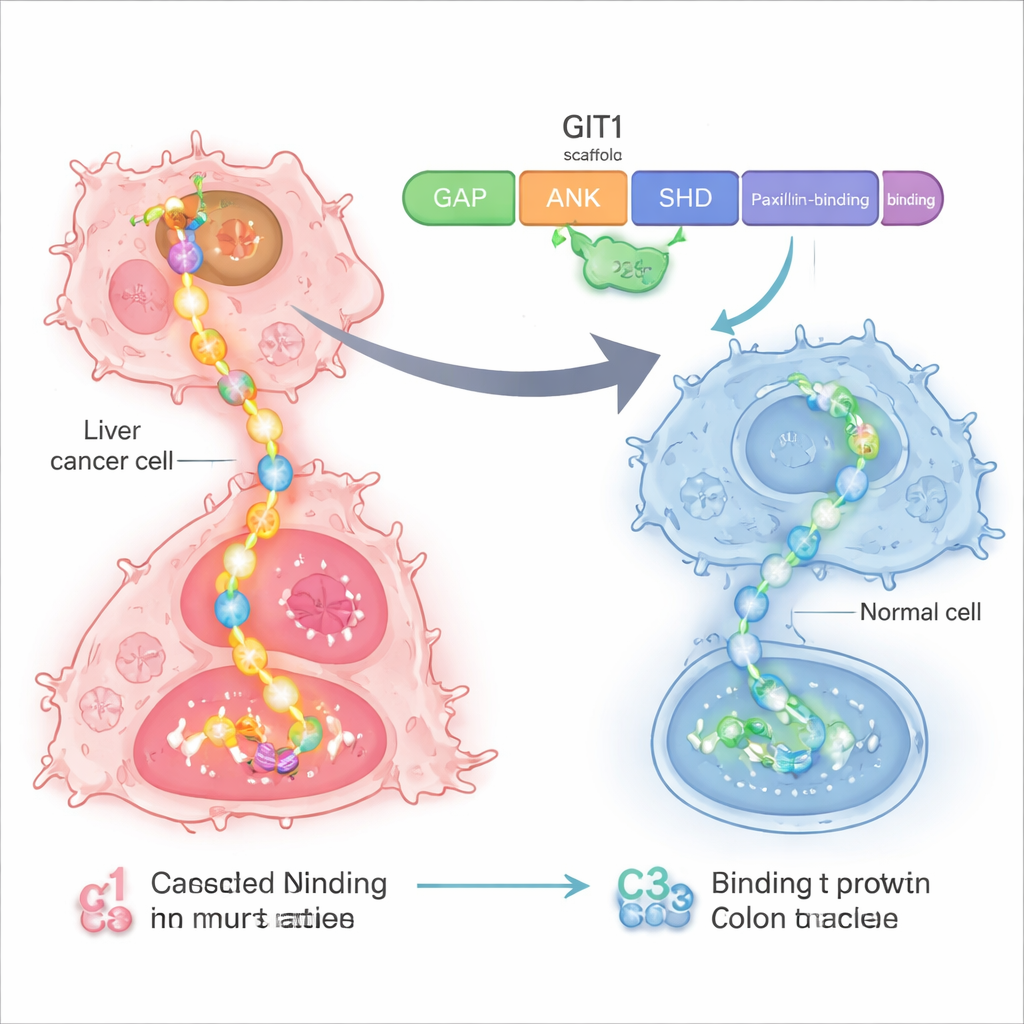
Kanser hücreleri içinde savunmasız bir kontrol merkezi
Araştırmacılar, hücre içinde bir iskelet veya güç dağıtım noktası gibi davranan GIT1 adlı bir proteine odaklandı. Karaciğer ve kolon kanserlerinde GIT1 ve onun eşlik eden proteini MAT2B aşırı üretilir. Birlikte, hücrelere bölünme ve göç sinyali veren RAS–RAF–MEK–ERK olarak bilinen büyük bir büyüme yolunun birkaç bileşenini bir araya getirirler. Önceki çalışmalar, GIT1 ve MAT2B bol olduğunda karaciğer ve kolon tümörlerinin daha hızlı büyüdüğünü ve daha kolay yayıldığını, bu proteinler azaltıldığında ise kanser büyümesinin yavaşladığını gösterdi. Bu da GIT1–MAT2B iskeletini daha hedefli bir tedavi için cazip bir hedef haline getirdi.
Plan olmadan küçük bir molekül tasarlamak
Ana zorluk, GIT1’in üç boyutlu kristal yapısının mevcut olmamasıydı; bu nedenle ekip proteinin şeklini “doğrudan bakarak” belirleyemedi. Bunun yerine, MAT2B ve diğer sinyal proteinlerinin bağlandığı bölgeye yakın olan ankyrin tekrarlarından oluşan GIT1’in bir bölgesinin yapısını bilgisayar modellemesiyle öngördüler. Sonra bu modele karşı büyük bir küçük molekül kütüphanesini sanal olarak tarayarak hangi bileşiklerin o bölgeye bağlanabileceğini test ettiler. Hücrelerde test edilen dokuz adayın arasından bileşik 3 (C3) öne çıktı. C3, yakından ilişkili GIT2’ye değil yalnızca GIT1’e özgü olarak bağlandı ve birden çok kanser hücre hattında ERK büyüme sinyalinin aktivitesini azalttı.
Kanser hücrelerinin bölünmesini ve yayılmasını durdurmak
Karaciğer ve kolon kanseri hücreleri C3 ile muamele edildiğinde büyümeleri yavaşladı ve daha yüksek dozlarda birçok hücre öldü; buna karşın kanser dışı karaciğer ve böbrek hücreleri büyük ölçüde etkilenmedi. C3, kanser hücrelerini hücre döngüsünün G2 ile M fazları arasındaki sınırda, yani hücrenin ikiye bölünmeden hemen önce ve mitoz sırasında duraklattı. Bileşik ayrıca kanser hücrelerinin koloni oluşturma ve bir yüzey boyunca göç etme yeteneğini keskin biçimde azalttı—bunlar tümör yeniden büyümesi ve metastaz ile ilişkili laboratuvar ölçümleridir. Moleküler düzeyde C3, GIT1, MAT2B ve RAF–MEK–ERK sinyal proteinleri arasındaki etkileşimleri zayıflattı; bunun sonucu olarak MEK ve ERK aktivitesi ile hücre döngüsü sürücüsü siklin D1 düzeyleri azaldı.
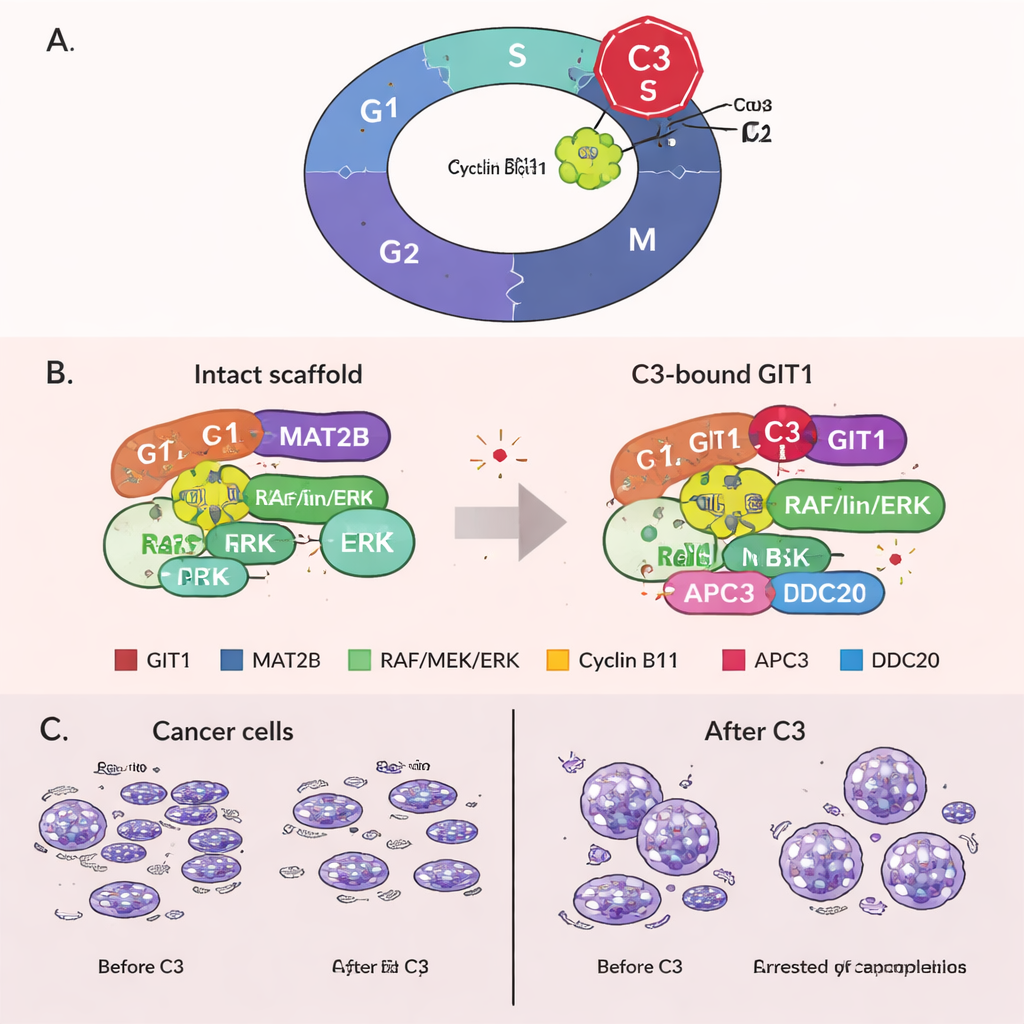
GIT1’in yeni keşfedilen rolüyle hücreleri mitozda kilitlemek
Beklenmedik şekilde ekip, GIT1’in hücre bölünmesinin son adımlarında yeni bir rolünü ortaya çıkardı. GIT1’in hücreleri mitoza iten bir protein olan siklin B1’e bağlandığını ve ayrıca siklin B1’i normalde yıkarak hücrelerin mitozdan çıkmasına izin veren anafaz-promoting kompleks (APC/C) adlı protein makinesinin parçalarına bağlandığını buldular. C3 tedavisi GIT1 ile siklin B1 arasındaki bağı güçlendirdi, ancak GIT1, siklin B1 ve APC/C bileşenleri arasındaki bağlantıları zayıflattı. Sonuç olarak siklin B1 etkin biçimde parçalanamadı, düzeyleri yüksek kaldı ve hücreler mitozda takıldı. Bu uzun süreli duraklama hücre ölümünü tetiklediği bilinen bir olaydır ve C3’ün kanser hücrelerini öldürmesinin ikinci bir yolunu sunar. Önemli olarak, GIT1 deneysel olarak azaltıldığında C3’ün siklin B1’i yükseltme, hücre döngüsünü engelleme ve büyümeyi baskılama yeteneğinin büyük bölümünü kaybettiği görüldü; bu da C3 etkilerinin gerçekten GIT1’e bağımlı olduğunu gösterir.
Hayvan modellerinde ümit verici sonuçlar
Araştırmacılar daha sonra C3’ün canlı organizmalarda işe yarayıp yaramadığını görmek için fare modellerine geçti. İmmun yetkin farelere eklenen kolorektal tümörlere doğrudan enjekte edilen C3, ana organlarda belirgin toksisite olmadan tümör büyümesini keskin şekilde yavaşlattı. İki ek modelde—immun yetmez farelerin karaciğerinde büyüyen insan kolon kanseri hücreleri ve immun yetkin farelerde karaciğere yayılmış fare kolon kanseri hücreleri—intraperitoneal enjeksiyonla verilen C3 tümör yükünü ve yayılma işaretlerini azalttı. Kan testleri ve doku incelemeleri uygulamaların iyi tolere edildiğini gösterdi ve farmakokinetik çalışmalar dozlamadan sonra birkaç saat boyunca kanda yeterince yüksek ilaç düzeyleri olduğunu ortaya koydu.
Gelecekteki kanser tedavileri için olası anlamı
Uzman olmayan bir dinleyici için temel mesaj şu: araştırmacılar kanseri tek bir mutasyona uğramış enzimi hedeflemek yerine, kanser hücrelerinin büyüme sinyalleri ve düzgün hücre bölünmesi için dayandıkları çoklu protein birleşimini bozarak saldırmanın bir yolunu buldular. Küçük molekülleri C3, GIT1’e özgü şekilde bağlanıyor, onun ortakları ağını yeniden şekillendiriyor, büyük bir büyüme yolunu kısıyor ve kanser hücrelerini mitoz sırasında ölümcül bir trafik sıkışıklığına sokuyor. C3 hâlâ deneysel bir araç olup henüz hasta tedavisi için bir ilaç olmasa da çalışma, GIT1 gibi iskelet proteinlerini hedeflemenin karaciğer ve kolon kanserlerini daha yüksek hassasiyetle ve potansiyel olarak daha az yan etkiyle tedavi etme yolunu açabileceğini gösteriyor.
Atıf: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Anahtar kelimeler: karaciğer kanseri, kolon kanseri, hedefe yönelik tedavi, hücre döngüsü durması, iskelet (scaffold) proteini