Clear Sky Science · tr
Melanom hücre kaderini yeniden yönlendirmek: TRPM8 modülatörleri apoptozu tetikliyor ve NK hücre sitotoksisitesini artırıyor
“Soğuk sensör”ü cilt kanserine karşı kullanmanın önemi
Melanom, sıklıkla ilaçlardan ve bağışıklık sisteminden kaçmayı öğrenen tehlikeli bir cilt kanseri türüdür. Bu çalışma, melanom hücrelerinde beklenmedik bir zayıflığı araştırıyor: sinir hücrelerinin soğuğu veya mentolu algılamasını sağlayan sensör olarak bilinen TRPM8 proteini. Araştırmacılar, TRPM8’i bloke eden özenle tasarlanmış ilaçların melanom hücrelerini kendi kendini yok etmeye itebileceğini ve aynı zamanda bunları doğal öldürücü (NK) bağışıklık hücreleri için daha kolay hedef haline getirebileceğini gösteriyor. Bu çift etkili yaklaşım, inatçı ve ileri evre melanom için yeni bir tedavi yoluna işaret ediyor.
Melanom hücrelerinde gizli bir anahtar
Büyük kanser veritabanlarını tarayarak ve hastadan türetilmiş melanom hücrelerini laboratuvarda inceleyerek ekip, TRPM8’in metastatik melanomda normal cilde, sağlıklı melanositlere ve dermal fibroblastlara kıyasla çok daha bol bulunduğunu saptadı. Görüntülemeyle TRPM8’in hem hücre yüzeyinde hem de iç membranlarda yer aldığını gösterdiler; bu da kanalın hücre davranışını etkileyecek stratejik noktalarda konumlandığını düşündürüyor. Yeni TRPM8 hedefli moleküllerden oluşan bir panel uygulandığında, iki bileşik (4 ve 9 adlandırılmış) tutarlı biçimde öne çıktı: zaman içinde melanom hücrelerinin hayatta kalmasını keskin biçimde azalttılar, normal cilt hücrelerini ise büyük ölçüde sağ bırakttılar. Genetik testler, TRPM8 ortadan kaldırıldığında bu ilaçların öldürücü etkisini kaybettiğini, TRPM8 arttığında melanom hücrelerinin daha hassas hale geldiğini doğrulayarak etkinin bu özel kanala bağlı olduğunu kanıtladı. 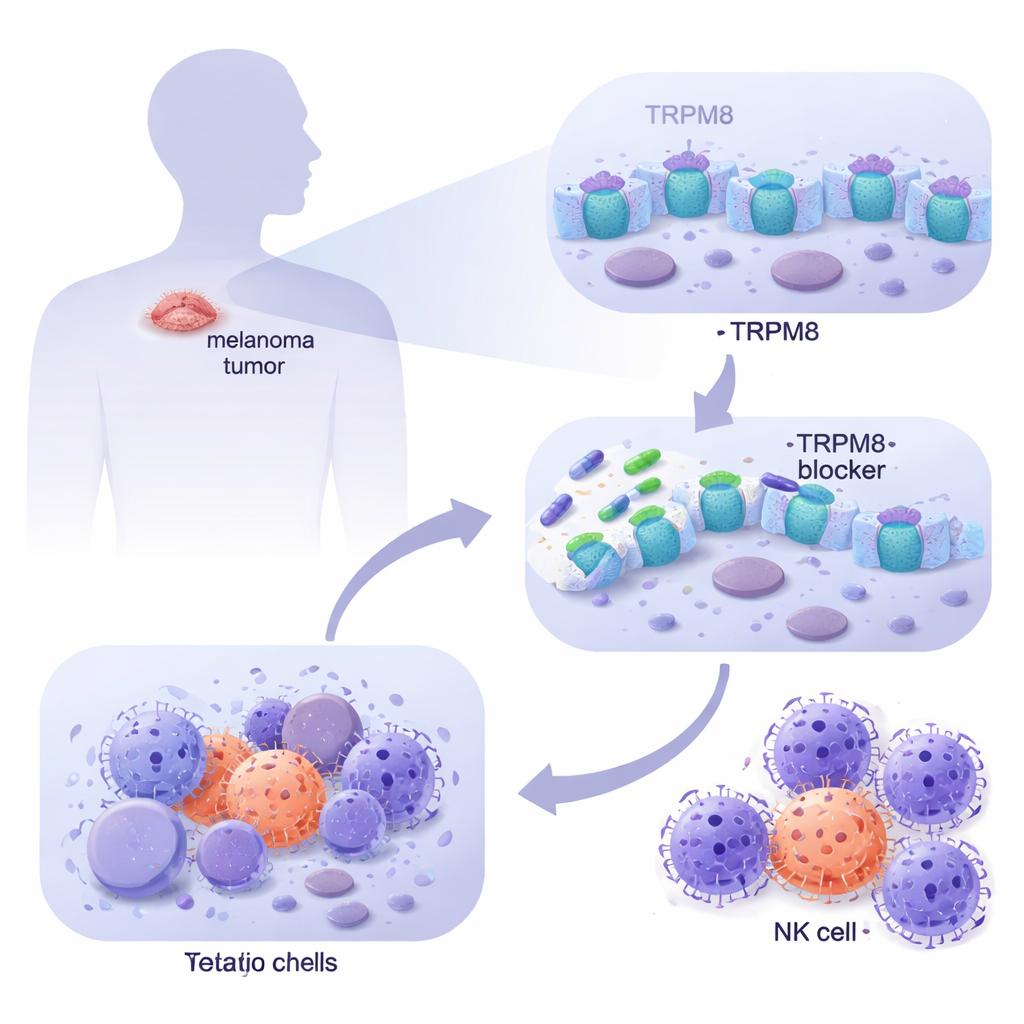
Kanser hücrelerini enerji krizine zorlamak
Mentol gibi klasik TRPM8 aktive edicilerinin hücreye kalsiyum girişini hızla artırmasının aksine, bu yeni bloke ediciler kalsiyum değişiklikleri tetiklemedi. Bunun yerine, melanom hücrelerinde bir oksidatif stres dalgası başlattılar. Bileşikler, özellikle hücrenin enerji fabrikaları olan mitokondriler içinde olmak üzere, reaktif oksijen türlerini hızlıca artırdı. Bu oksidatif patlama mitokondrilerin elektriksel yükünü kaybetmesine, parçalanmasına ve sitokrom c kaçışına yol açtı; bu da hücrenin iç “intihar” programını açmanın kilit bir adımıdır. Bu reaktif molekülleri temizleyen antioksidanlar hücreleri büyük ölçüde kurtararak redoks dengesizliğinin yan etki olmadığını, hücre ölümünün motoru olduğunu gösterdi. Aşağı akışta, kaspaz-3 aktivasyonu ve PARP parçalanması gibi klasik ölüm belirteçleri, hücrelerin rastgele bir hasar şekli yerine programlı apoptoz geçirdiğini doğruladı.
Hayatta kalma sinyallerini etkisizleştirmek ve bir koruyucuyu uyandırmak
Oksidatif darbe daha geniş bir stres yanıtını tetikledi. İlaçlar DNA hasarının sensörü ATM’yi aktive etti ve hasarlı bir hücrenin kendini onarıp onarmamaya karar veren ünlü tümör susturucu protein p53’ün birikimine ve aktivasyonuna yol açtı. Aynı zamanda, bileşikler melanomun ana hayatta kalma yollarından biri olan PI3K–AKT yolunu zayıflattı. Normalde TRPM8, AKT’ı aktif, büyümeyi teşvik edici formunda tutmaya yardımcı olmak için PI3K bileşenleriyle fiziksel etkileşim içindedir. Tedavi sonrasında bu ortaklık bozuldu ve AKT aktivitesi düştü; bu da dengeyi hücre ölümüne doğru daha da eğdi. Önemli olarak, bu değişiklikler melanom hücrelerinde belirginken kansersiz hücrelerde görülmedi; bu da tümörün sert şekilde hedeflendiği ancak sağlıklı dokunun korunduğu bir tedavi penceresini işaret ediyor.
Tümörleri bağışıklık “atak timleri”ne daha görünür kılmak
Melanomun tehlikesi bağışıklık gözetiminden kaçma yeteneğinde de yatıyor. Araştırmacılar bu nedenle düşük doz TRPM8 bloke edicilere uzun süre maruz kalan ve hayatta kalan tümör hücrelerinde ne olduğunu sordular. Bu kalıntı hücrelerin yüzeylerinde NKG2D reseptörleri tarafından tanınan bir alarm işareti işlevi gören ULBP1 adlı bir yüzey belirtecini daha fazla sergilemeye başladıklarını keşfettiler. Diğer ilgili belirteçler değişmedi; bu da seçici bir etkiyi gösteriyor. Gerçek tümörleri daha iyi taklit eden üç boyutlu melanom sferoidlerinde, TRPM8 bloke edicilerle ön işlem sadece yapıları küçültmek ve hücre ölümünü artırmakla kalmadı, aynı zamanda bunları NK hücre saldırısına çok daha duyarlı kıldı. ULBP1 veya NKG2D antikorlarla bloke edildiğinde bu ek öldürme büyük ölçüde ortadan kalktı; bu da geliştirilmiş bağışıklık temizliğinin tümör ile NK hücreleri arasındaki bu özgül etkileşim yoluyla gerçekleştiğini gösteriyor. 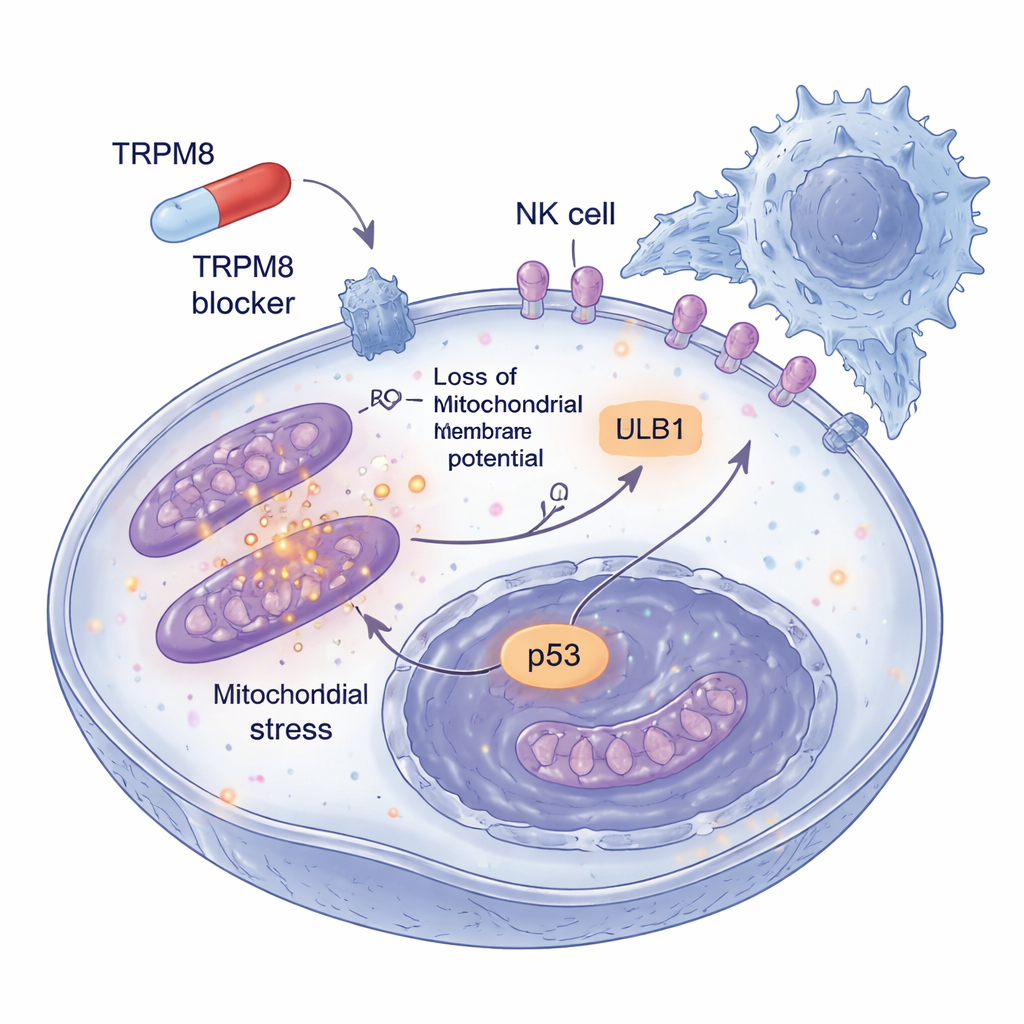
Gelecekteki melanom bakımına olası etkileri
Basitçe söylemek gerekirse, TRPM8 “soğuk sensörü”nü bloke etmek onu terapötik bir kaldıraç haline getiriyor: melanom hücrelerini ölümcül bir mitokondri ve DNA krizine sürüklüyor ve aynı zamanda NK hücreleri tarafından yok edilmek üzere işaretliyor. İlaçlar normal cilt hücrelerini büyük ölçüde koruyor ve NK hücrelerine zarar vermiyor; bu da yeni tedaviler için umut verici bir temel sunuyor. Yazarlar, TRPM8 bloke edicilerin mevcut immünoterapilerle birleştirilebileceğini; böylece ileri, ilaçlara dirençli melanomu iki cepheden: tümör hücrelerini doğrudan öldürerek ve hayatta kalanları bağışıklık sistemi için daha görünür kılarak hedefleyebileceğini öneriyorlar.
Atıf: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Anahtar kelimeler: melanom, TRPM8, mitokondri, oksidatif stres, doğal öldürücü hücreler