Clear Sky Science · tr
Laktillasyon kaynaklı TRIM29, hnRNPA1 aracılı Wnt/β-katenin yolu üzerinden mide kanserinde invaziv davranış ve lenf nodu metastazı oluşturur
Bu araştırma neden önemli
Mide (gastrik) kanseri, yakın lenf düğümlerine erken yayılma eğilimi nedeniyle cerrahiyle kür olmasını zorlaştıran, dünya çapında en ölümcül kanserlerden biridir. Bu çalışma, tümör metabolizmasına bağlı bir kimyasal değişikliğin TRIM29 adındaki bir proteini nasıl güçlendirdiğini ortaya koyuyor; bu durum kanser hücrelerinin çevre dokuya invaze olmasını, yeni lenf damarları oluşturmasını ve kemoterapiye direnç kazanmasını sağlıyor. Bu olay zincirinin anlaşılması, mide kanserinin yayılımını yavaşlatmaya veya engellemeye yönelik yeni yaklaşımlara işaret ediyor.
Midedeki tümörlerde tehlikeli bir ortaklık
Araştırmacılar işe 100 hastadan alınan mide kanseri örneklerini çevre sağlıklı doku ile ve ayrıca büyük kamuya açık gen veri tabanlarıyla karşılaştırarak başladı. TRIM29’un, bağışıklık düzenlemesi ve diğer kanserlerle daha önce ilişkilendirilmiş bir protein olmasına karşın, tümör hücrelerinde tutarlı şekilde yüksek olduğunu buldular. Tümörlerinde daha fazla TRIM29 bulunan hastalarda lenf nodu ve damar içi yayılım daha sık görüldü ve genel sağkalım daha kötüydü. Bu desenler TRIM29’un sadece bulunmakla kalmayıp mide kanserinin daha agresif davranmasında aktif rol oynadığını düşündürdü.
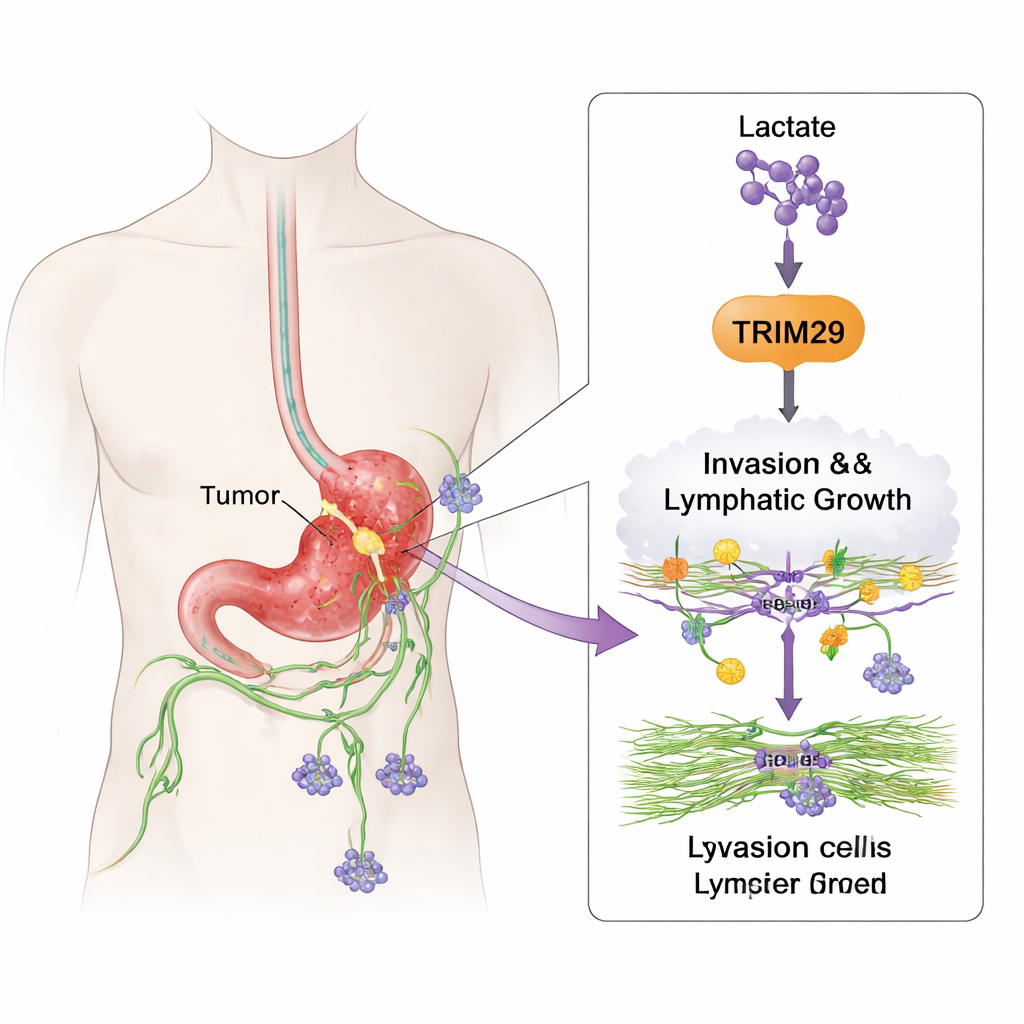
Kanser hücreleri nasıl seyahat etmeyi öğrenir
TRIM29’un gerçekte ne yaptığını görmek için ekip, mide kanseri hücre hatlarında bu proteinin düzeylerini değiştirdi. TRIM29’u azalttıklarında hücreler belirgin şekilde daha az hareketli ve vücut dokusunu taklit eden 3B jelleri geçmede daha az yetenekli oldu. TRIM29’u artırmak ters etki göstererek hücreleri daha invaziv hâle getirdi. Araştırmacılar ayrıca lenf damarlarını döşeyen hücreler olan lenfatik endotel hücrelerini inceledi. TRIM29 bakımından zengin kanser hücreleri bu damar hücrelerini filizlenmeye ve tüp benzeri yapılar oluşturmaya teşvik etti; bu yeni lenf damarı oluşumunun (lenfanjiyogenez) bir göstergesiydi. Fare modellerinde yüksek TRIM29’lu tümörler daha fazla karaciğer ve lenf nodu metastazı oluştururken, TRIM29 baskılanmış olanlar daha az yayıldı ve daha az lenfatik damar oluşturdu.
Moleküler röle: önemli bir düzenleyiciyi korumak
Daha derine indiklerinde bilim insanları TRIM29’un, genlerin işlenmesini etkilediği ve kanser yayılımıyla ilişkilendirildiği bilinen hnRNPA1 adlı başka bir proteinle fiziksel olarak bağlandığını keşfettiler. Normalde hnRNPA1 hücrenin atık imha sistemi aracılığıyla başka bir enzim olan ZFP91 tarafından tahrip edilmek üzere işaretlenebilir. TRIM29 bu süreçle, hnRNPA1’e bağlanmak için ZFP91 ile rekabet ederek müdahale eder. TRIM29 bol olduğunda hnRNPA1’in işaretlenip parçalanmasını engeller. Sonuç olarak hnRNPA1 daha stabil hale gelir ve kanser hücrelerinde birikir; bu da Wnt/β-katenin yolunun aktivasyonuyla sonuçlanan bir sinyal zincirini başlatır—tümör büyümesi ve hareketini bilinen bir şekilde tetikler. Bu da VEGF‑C üretimini artırır; VEGF‑C yeni lenf damarlarını uyarır ve kanser hücrelerine kaçmaları için daha fazla “yol” sağlar.
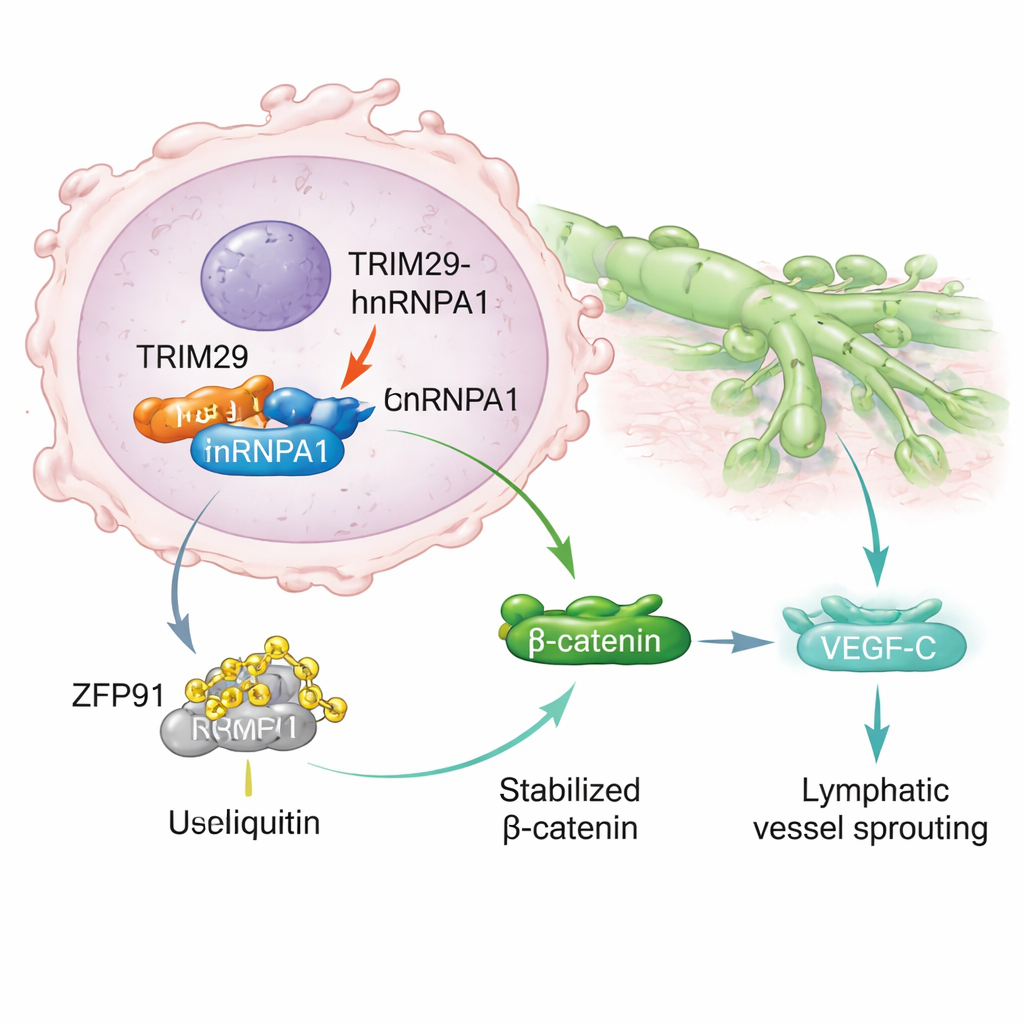
Kanseri laktatla beslemek
Çalışma bu invaziv davranışı tümörlerin şeker işleme biçimiyle de ilişkilendiriyor. Hızla büyüyen kanserler sıklıkla yüksek miktarda laktat üreten bir metabolizma biçimine dayanır; laktat bir zamanlar sadece atık kabul ediliyordu. Burada yazarlar, laktatın DNA’yı paketlemeye yardımcı olan histon proteinlerini, özellikle H3K9 adlı bir bölgede kimyasal olarak değiştirebildiğini gösteriyor. Bu “laktillasyon” TRIM29 geninin bir açma anahtarı gibi davranarak onun aktivitesini yükseltiyor. Metabolik ilaçlarla laktat üretimini düşürdüklerinde TRIM29 düzeyleri azaldı; laktatı yükselttiklerinde TRIM29 arttı. Hastalardan elde edilen mide kanseri dokuları, daha yüksek H3K9 laktillasyon düzeyleri sergiledi; bu da daha yüksek TRIM29, daha fazla lenf nodu yayılımı ve daha kötü sağkalımla koreleydi. Özetle, tümörün değişmiş metabolizması daha agresif bir genetik programın yazılmasına yardımcı oluyor.
Kemoterapiyi güçlendirmenin yeni yolları
Lenf damarları sadece kanser hücrelerini taşımakla kalmaz; aynı zamanda kemoterapi ilaçlarını tümörlerden uzaklaştırabilirler. Farelerde büyütülen hasta kaynaklı tümör greftlerini kullanarak araştırmacılar, TRIM29’u ve lenf damar oluşumunu engellemenin 5‑florourasil (5‑FU) adlı standart mide kanseri ilacının etkisini artırıp artırmayacağını test ettiler. TRIM29’un inhibisyonu veya lenfanjiyogenezin engellenmesi, her biri 5‑FU’nun tümörleri küçültme ve hücre bölünmesini azaltma etkinliğini artırdı. Her iki stratejinin birleştirilmesi en güçlü yanıtı verdi; bu, ileri hastalıkta bazı ilaç direnç biçimlerinin üstesinden gelmeye yönelik potansiyel bir yol öneriyor.
Bu hastalar için ne anlama geliyor
Bu çalışma adım adım bir tablo çiziyor: mide tümörleri fazla laktat üretiyor, bu TRIM29’u açıyor; TRIM29 sonra hnRNPA1’i koruyor, bir büyüme yolunu stabilize ediyor ve lenf damar oluşumunu ve lenf nodlarına yayılımı artırıyor. Klinik olarak yüksek TRIM29 ve ilişkili laktillasyon işaretleri, daha agresif hastalık riski taşıyan hastaları tanımlıyor. Gelecekte, laktat sinyallemesini azaltan, TRIM29’u engelleyen veya lenf damar oluşumunu önleyen ilaçlar mevcut kemoterapiyle birleştirilerek mide kanserinin yayılmasını engellemeye ve tedavilerin etkinliğini artırmaya yardımcı olabilir.
Atıf: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Anahtar kelimeler: mide kanseri metastazı, TRIM29, laktat ve laktillasyon, lenfanjiyogenez, Wnt beta-katenin yolu