Clear Sky Science · tr
Selenometiyonin: çift mekanizmalı bir ferroptozis inhibitörü olarak — transsülfürasyonun ötesinde selenyum teminiyle GPX4 biyosentezi ve GPX4 aktivitesinden bağımsız, indirgenmiş kapasiteyle ROS süpürülmesi
Hücrelerimizi “paslanma benzeri” bir ölümden korumanın önemi
Vücudumuzdaki hücreler birçok farklı yolla ölebilir; en yeni ve ilginç olanlardan biri ferroptozis adı verilen, demir kaynaklı ve hücre zarı üzerinde “paslanma” benzeri bir hasar sürecidir. Bu mekanizma şimdi böbrek hasarından nörodejenerasyona kadar çeşitli hastalıklarla ilişkilendiriliyor. Pek çok kişinin takviye olarak bildiği eser element selenyum, bu tehlikeli hücre ölümü biçimini durdurmada kilit bir rol oynuyor. Bu çalışma, yaygın bir selenyum içeren amino asit olan selenometiyoninin, hücreleri ferroptozisten yalnızca tek bir yolla değil, iki ayrı koruyucu stratejiyle nasıl koruyabildiğini inceliyor.
Devasa bir ilaç taramasında bulunan yeni bir savunmacı
Araştırmacılar ferroptozisi engelleyebilecek küçük molekülleri bulmak için FDA onaylı ilaçlar ve doğal ürünler arasından binlerce bileşiği taradılar. İnsan kanser hücre hatlarında ferroptozisi tetiklemek için RSL3 adlı kimyasalı kullandılar ve hücre ölümünü ile hücre zarlarında biriken okside yağların düzeyini izlediler. Tüm adaylar arasında selenometiyonin güçlü bir koruyucu olarak öne çıktı: farklı hücre tiplerinde ve iki ana ferroptozis modelinde —biri doğrudan GPX4 inhibisyonu (RSL3 ile) diğeriyse hücreleri antioksidan glutatyonun yapı taşı olan sistinden yoksun bırakma— hem lipid hasarını hem de hücre ölümünü azalttı. Bu sonuçlar selenometiyonini geniş kapsamlı ve dayanıklı bir ferroptozis inhibitörü olarak konumlandırdı. 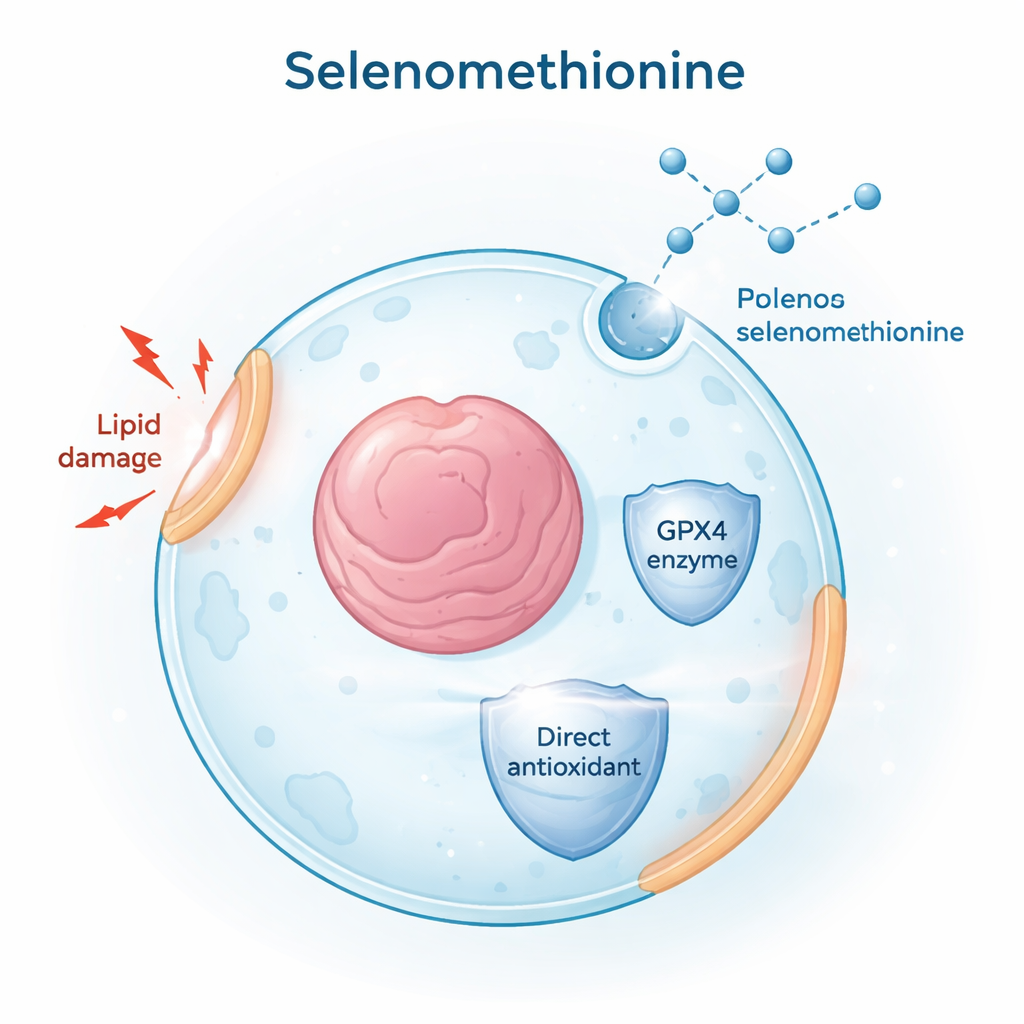
Ana koruyucu enzim için selenyum temini
Hücrelerdeki temel anti-ferroptozis kalkanlarından biri, fonksiyonu için selenyuma bağımlı olan GPX4 adlı bir enzimdir. Araştırma ekibi, selenometiyoninin bu yolakları yalnızca besleyip beslemediğini yoksa daha fazlasını mı yaptığını belirlemeye çalıştı. Selenometiyoninden gelen selenyumun, transsülfürasyon adı verilen tipik bir yolak zayıf veya bloke olsa bile GPX4 inşa etmek için uygun formlara nasıl dönüştürülebileceğini izlediler. Bu kükürt–selenyum yollarındaki enzimlerin genetik susturmaları (knockdown) ve kimyasal inhibitörleri kullanıldığında, selenometiyoninin hâlâ GPX4 düzeylerini artırdığı ve hücreleri koruduğu görüldü. Bu, hücrelerin selenometiyoninden selenyumu çıkarmak ve GPX4 üretimini sürdürmek için birden fazla metabolik rotayı kullanabileceğini; klasik yolun zayıf olduğu dokularda bile GPX4 yapımının devam edebildiğini gösterdi.
Alışılagelmiş enzime dayanmayan koruma
Şaşırtıcı şekilde, araştırmacılar CRISPR gen düzenleme ile hücrelerden GPX4’ü tamamen kaldırdıklarında, selenometiyoninin ferroptozise karşı korumaya devam ettiği görüldü. Hâlâ zar lipid hasarını ve hücre ölümünü azalttı; bu da GPX4’ün tüm hikâye olmadığını gösteriyor. Ek deneyler, korumanın bir bölümünün selenometiyoninin yeni sentezlenen proteinlerin içine dahil edilmesiyle ilişkili olabileceğine işaret etti, ancak bunun etkinin yalnızca bir parçası olduğu anlaşıldı. Yazarlar daha sonra selenometiyoninin kimyasal reaktivitesine odaklandı. Bunun reaktif oksijen türlerini (ROS), hidrojen peroksit dahil, doğrudan etkisiz hale getirebildiğini ve okside olarak “sülfoksit” formuna dönüştüğünü buldular. Kütle spektrometrisi bu ürünü doğruladı ve hücrelere sülfoksit formu verildiğinde de ferroptozisin azaldığı görüldü; bu da hücrelerin bunu redoks döngüsünde tekrar etkin selenometiyonine geri çevirebildiğini ima ediyor.
Hücre kültüründen canlı hayvanlarda böbrek korumasına
Bu mekanizmaların bütün bir organizmada önemli olup olmadığını test etmek için ekip, ferroptozisi içeren bir durum olarak bilinen kanser ilacı sisplatin kaynaklı akut böbrek hasarı fare modeline yöneldi. Sisplatinle tedavi edilen farelerde kilo kaybı, böbrek şişmesi, kötü böbrek fonksiyonu ve yüksek düzeyde ferroptozis belirteçleri görüldü. Hayvanlara selenometiyonin verildiğinde bu sorunların birçoğu düzeldi: vücut ağırlığı toparlandı, böbrek şişliği azaldı, kanla ölçülen böbrek fonksiyon ölçütleri normalleşti, inflamatuar sinyaller düştü ve lipid hasarının kimyasal belirteçleri azaldı. Böbrek dokusunda ayrıca daha yüksek GPX4 düzeyleri ve daha az yapısal hasar gözlendi. Bu yararlar, iyi bilinen deneysel bir ferroptozis blokeri olan ferrostatin-1 ile gözlemlenenlere kıyaslanabilirdi. 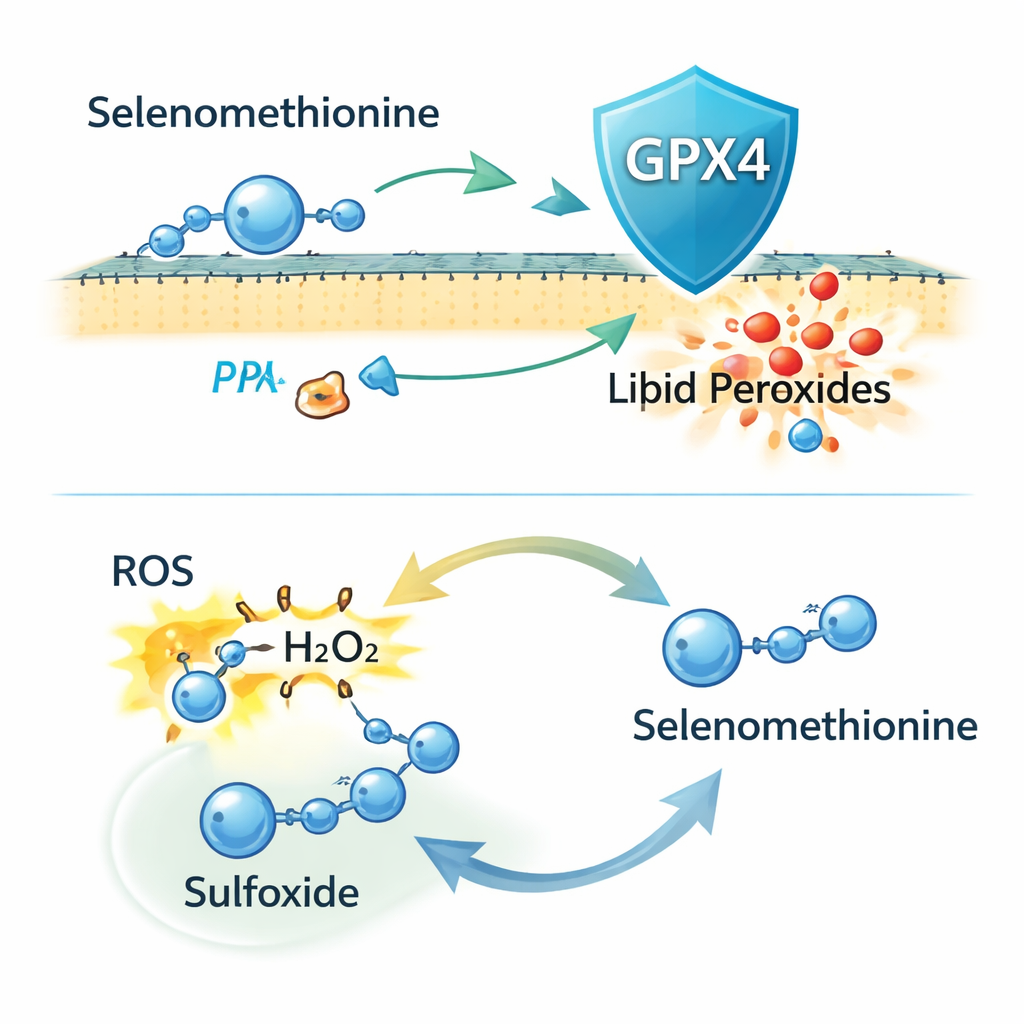
Gelecek tedaviler için anlamı
Günlük ifadeyle, bu çalışma selenometiyoninin hücre zarlarının demirle alevlenen “paslanmasına” karşı çift amaçlı bir yangın söndürücü gibi davrandığını öne sürüyor. Bir yandan, hücrelerin hasarlı yağları temizleyen iç düzeni olan GPX4 enzimini daha fazla üretebilmesi için selenyum sağlıyor. Öte yandan, selenometiyonin kendisi zararlı oksidanları yakalayabiliyor ve geri dönüştürülebilir şekilde GPX4’e bağımsız bir yedek koruma sunuyor. Bu özellikler bir araya geldiğinde selenometiyonini, ferroptozisin merkezi rol oynadığı hastalıkların —ilaç kaynaklı böbrek hasarı gibi— önlenmesi veya tedavisi için umut verici bir aday haline getiriyor ve kontrolsüz oksidatif stresin yol açtığı diğer durumlarda da potansiyel taşıyor.
Atıf: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Anahtar kelimeler: ferroptozis, selenyum, selenometiyonin, oksidatif stres, akut böbrek hasarı