Clear Sky Science · tr
Şaperonin TRiC bileşeni Cct3 aksiyonel transport, miyelinleşme ve nöromüsküler kavşak olgunlaşması için gereklidir
Sinir Bağlantıları Yanlış Gittiğinde
Beyinlerimiz ve vücudumuz, sinyalleri hızlı ve güvenilir şekilde taşıyan uzun, kablo benzeri sinir liflerine dayanır. Bu iş için birçok sinir yalıtkan bir tabaka olan miyelinle sarılır ve uçlarının kaslarla hassas temaslar kurması gerekir. Bu makale, protein katlanmasına yardımcı olan hücresel bir “yardımcı” olan Cct3 başarısız olduğunda neler olduğunu araştırıyor. Zebrafish ve insan dokusu kullanarak, araştırmacılar bu büyük şaperon makinesinin tek bir bileşeninin miyelini, sinir–kas bağlantılarını ve sinir hücrelerini canlı ve işlevsel tutan iç taşıma sistemini nasıl bozabileceğini gösteriyor.
Sinir İnşasında Hücresel Bir Terzi
Her hücrede yeni üretilen proteinlerin doğru şekillere katlanması gerekir; bu, özenle dikilmiş bir takımı andırır. Cct3 alt birimini içeren TRiC kompleksi, özellikle aktin ve tubulin gibi yapısal proteinlerin yaklaşık %10’unun doğru katlanmasına yardımcı olan ana “terzilerden” biridir. Bu yapı taşları hücrenin iç iskelesini ve hayati yüklerin taşındığı yolları oluşturur. CCT3 ve ilgili genlerin hatalı versiyonlarına sahip hastalarda beyin görüntüleri beyaz madde (beynin miyelin açısından zengin kablolaması) azalması ve periferik sinirler ile kaslarda sorunlar gösterir. Yazarlar, Cct3 kaybının sinir gelişimini ve işlevini nasıl raydan çıkardığını anlamaya çalıştı.
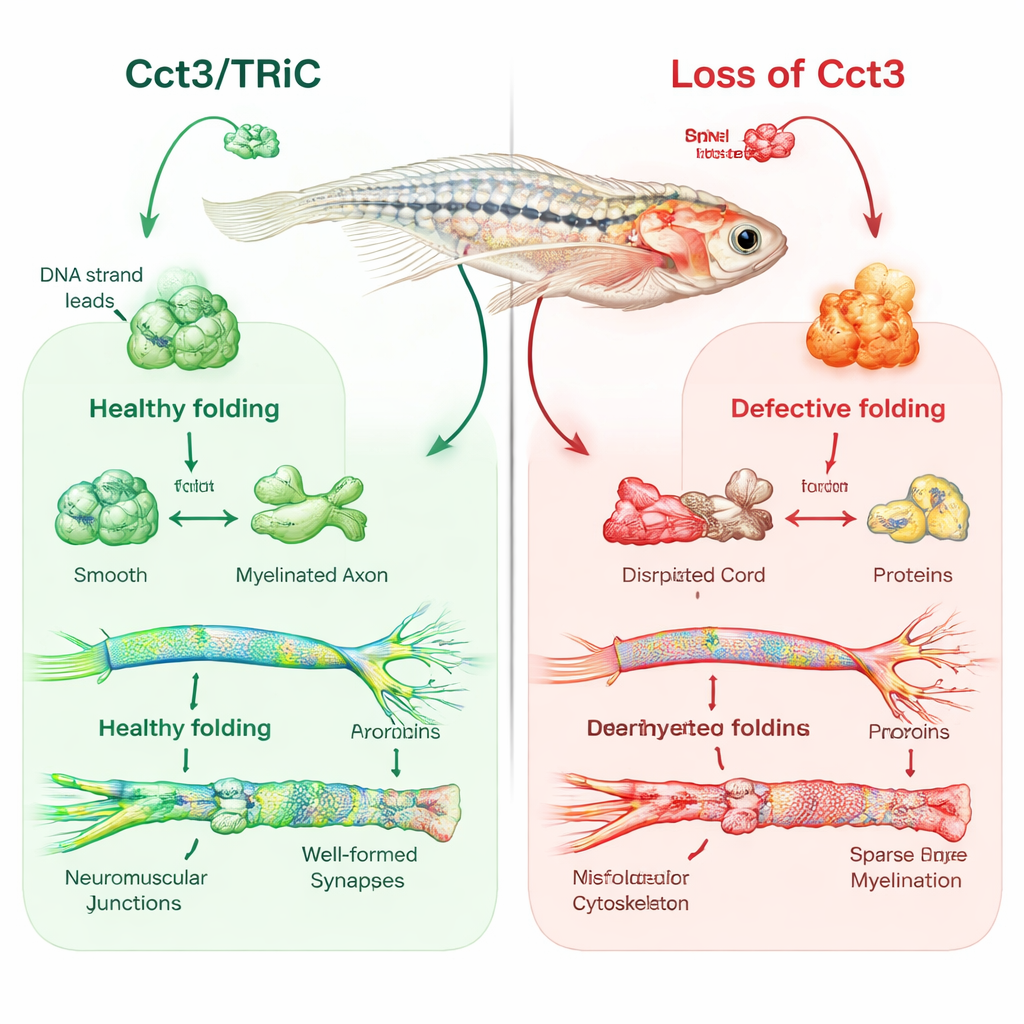
Miyelinlenmeye Açılan Bir Pencere Olarak Zebrafish
Araştırma ekibi işlevsel cct3 eksik zebrafishlar oluşturmak için CRISPR/Cas9 gen düzenlemesi kullandı. Bu küçük balıklarda daha küçük beyin ve gözler, kalp çevresinde sıvı birikimi, dokunmaya zayıf tepki ve birkaç gün içinde ölüm görüldü. Araştırmacılar cct3’ün haberci RNA’sını enjekte ederek normal cct3’ü yeniden sağladıklarında birçok kusur düzeldi ve bu da Cct3 kaybının temel neden olduğunu doğruladı. Miyeline odaklanarak, sinirlerin etrafındaki yalıtkan katmanları görselleştirmek için floresan belirteçler ve elektron mikroskobu kullandılar. Normal balıklarda beyin ve periferik sinirlerde miyelin oluşturan hücreler gelişimin dördüncü gününde aksonları düzenli, katmanlı kılıflarla sarmıştı. Buna karşın, cct3 mutantlarında miyelinizasyon yapan hücre sayısı çok daha azdı ve birçok aksonun etrafında neredeyse hiç uygun miyelin yoktu; oysa bu aksonlar yüzeyden normal şekilli görünüyordu.
Kırılgan Destek Hücreleri ve Gerilmiş Sinir–Kas Bağlantıları
Miyelinin neden eksik olduğunu bulmak için yazarlar periferik sinirleri saran destek hücreleri olan Schwann hücreleri ve ilgili nöral krest hücrelerini inceledi. Normal balıklarda bu hücreler uzun, ince uzantılar gönderiyor ve miyelin segmentlerini oluştururken şekillerini rafine ediyorlardı. Mutantlarda bu hücreler yuvarlaklaşıp uzantılarını kısaltıyor ve parçalanıyordu. Çekirdekleri programlı hücre ölümü tipik bir desen göstererek parçalanmıştı ve önemli bir ölüm belirteci (aktive olmuş Kaspaz 3) ortaya çıkarak bu hücrelerin birçoğunun erken öldüğünü gösterdi. Bu arada sinirlerin kasla buluştuğu nöromüsküler kavşaklarda kas üzerindeki reseptör “sıcak noktaları”nın düzeni rafine olamadı. Birçok küçük, hassas küme yerine mutantlarda daha az ve daha büyük reseptör yamaları görüldü; bu durum CCT3 mutasyonu olan bir insan hastada gözlemlenen basitleşmiş sinaptik kıvrımları yansıtıyordu.
Kırılmış İç Yollar ve Yavaşlayan Yük Trafiği
TRiC aktin ve tubulinin katlanmasına yardım ettiği için yazarlar motor aksonlarının iç iskeletini yakından inceledi. Mutantlarda tubulinin genel seviyelerinin keskin şekilde azaldığını ve hem merkezi hem de periferik sinirlerde normal mikro tübüllerin (taşıma için yol oluşturan boş tüpler) sayısının dramatik şekilde düştüğünü buldular. Taşıma için stabil, hazır mikro tübüller açısından önemli olan tubulin üzerindeki kimyasal “etiketler” de ciddi şekilde değişmişti. Motor aksonlar içindeki parlayan mitokondri ve endozomların canlı görüntülenmesiyle bu yüklerin nasıl hareket ettiğini izlediler. Sağlıklı balıklarda organeller akson boyunca hızlı ve yönlü olarak yol alıyordu. Mutantlarda birçok organel durdu veya sadece ileri geri sallanıyordu; bu, hasar görmüş yollar ve bozulmuş taşıma ile tutarlıydı.
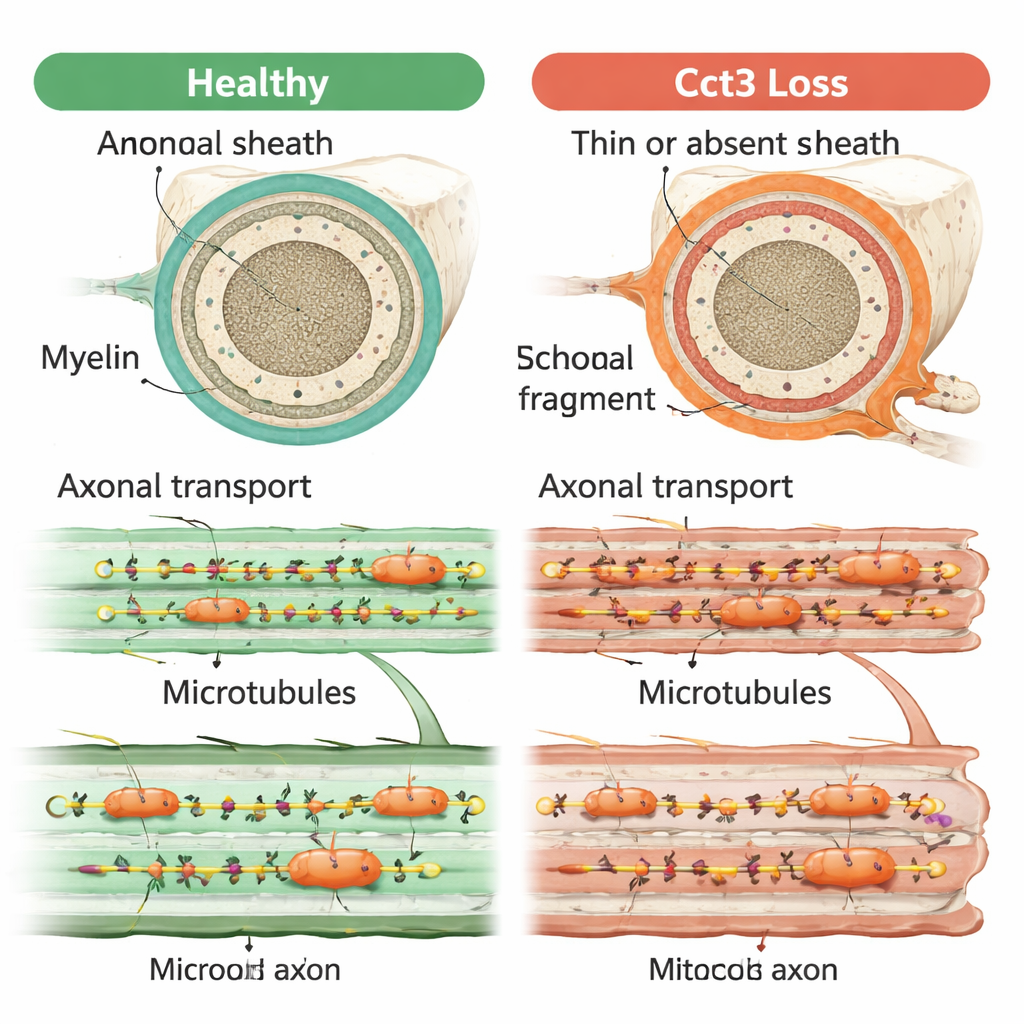
Birçok Belirtilerin Arkasındaki Temel Sorun
Bir arada ele alındığında, bulgular Cct3’ün sinir sağlığının birkaç birbirine bağlı yönü için vazgeçilmez olduğunu gösteriyor: miyelin oluşturan destek hücrelerin hayatta kalmasını destekliyor, uygun miyelin sarımını sağlıyor ve olgunlaşan nöromüsküler kavşakların ince ayara kavuşmasını mümkün kılıyor. Bu rollerin tümü, sitoskeletonu ve aksonel taşıma için kullanılan mikro tüp yollarını inşa eden proteinlerin katlanması ve korunması görevine dayandırılabilir. Bu yollar başarısız olduğunda, temel sinyaller ve malzemeler sinir boyunca doğru yerlere ulaşamaz; bu muhtemelen hem miyelin oluşturan hücrelerle iletişimi hem de sinir–kas temaslarının şekillenmesini zayıflatır. Bu çalışma, bozulmuş aksiyonel taşınmanın TRiC ile ilişkili bozukluklarda görülen çeşitli beyin ve sinir sorunlarını birleştiren ortak iplik olabileceğini öne sürüyor.
Atıf: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Anahtar kelimeler: miyelinleşme, aksiyonel transport, nöromüsküler kavşak, moleküler şaperonlar, zebrafish modeli