Clear Sky Science · tr
PDHA1–asetilasyon sinyali, prostat kanserinde anti‑androjen etkinliği zayıflatarak kuproptozu baskılar
Bu araştırma neden önemli
Prostat kanseri erkeklerde en yaygın görülen kanserlerden biridir ve ileri olgularda sıklıkla erkek hormon sinyallerini kapatan ilaçlarla tedavi uygulanır. Önemli bir ilaç olan enzalutamid başlangıçta genellikle etkilidir, ancak tümörler direnç geliştirdikçe işe yaramayı bırakır. Bu çalışma, bazı prostat kanserlerinin enzalutamid etkisinden nasıl kaçtığına dair şaşırtıcı bir neden ortaya koyuyor ve tek bir metabolik yolun engellenmesiyle tümörlerin yeniden duyarlı hale getirilebileceğini göstererek daha dayanıklı tedavilere kapı aralıyor.
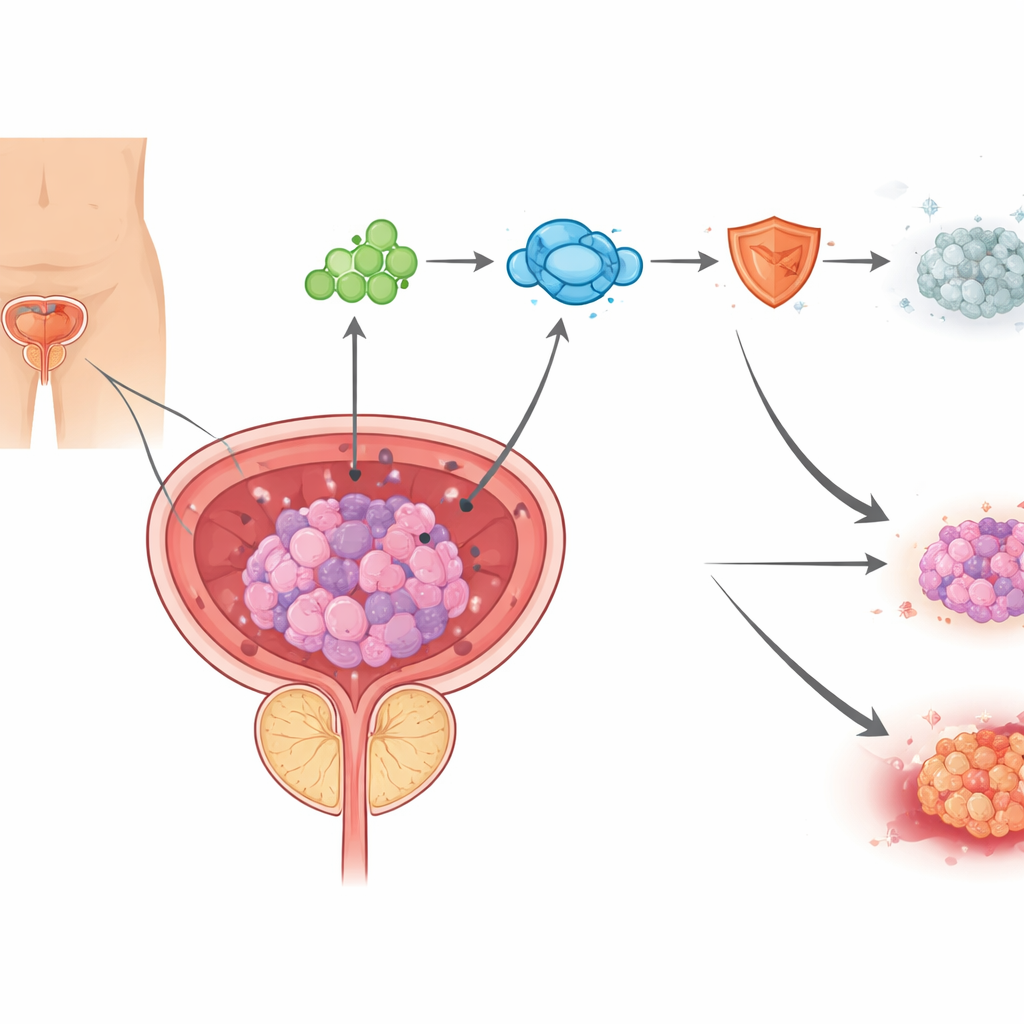
Bakırın tetiklediği yeni bir hücre ölümü türü
Hücreler birçok farklı yolla ölebilir ve modern kanser araştırmaları bu doğal ölüm programlarını tümör hücrelerinde yeniden harekete geçirmeye çalışıyor. Yazarlar, mitokondrilerde, yani hücrenin enerji santrallerinde bakır biriktiğinde tetiklenen ve yeni tanımlanmış bir hücre ölümü biçimi olan kuproptoz üzerine odaklanıyor. Androjen engelleyici ilaçlarla tedavi edilmiş prostat kanseri örneklerinde ekip, bakır birikimi ve mitokondri hasarına dair işaretler ile kuproptozun ayırt edici protein değişikliklerini buldu. Hücre kültürlerinde enzalutamid bakır düzeylerini artırdı ve mitokondrilere zarar verdi; bakır bağlayan bir bileşik hücreleri büyük ölçüde kurtarabildi, bu da enzalutamidin prostat kanseri hücrelerini kısmen bakır kaynaklı ölüme iterek öldürebildiğini gösteriyor.
Tümörlerin bakırın toksisitesini nasıl azaltığı
Yine de tüm kanser hücreleri yenilmiyor. Enzalutamid direnci gösteren prostat tümörlerinin birkaç veri setini inceleyip kuproptozla ilişkili genlere odaklanarak araştırmacılar öne çıkan bir proteini belirlediler: şeker kaynaklı yakıtı asetil‑CoA’ya çeviren mekanizmanın merkezi parçası olan PDHA1. PDHA1 düzeyleri dirençli tümörlerde daha yüksekti, daha kötü sağkalım ve daha agresif hastalıkla ilişkiliydi ve enzalutamid tarafından kendisi artırılıyordu. Laboratuvar deneylerinde PDHA1’i azaltmak kanser hücrelerini hem enzalutamide hem de doğrudan kuproptozu indükleyen bir ilaça karşı çok daha duyarlı hale getirirken, PDHA1’i yükseltmek onları öldürmeyi zorlaştırdı. Farelerde PDHA1 azaltılmış tümörler enzalutamid tedavisi altında çok daha fazla küçüldü; bu da bu enzimin yaşayan organizmalarda tümörlerin tedaviye dayanmasına yardımcı olduğunu doğruluyor.
Tedaviye karşı metabolik ve epigenetik bir kalkan
Araştırmacılar daha sonra PDHA1’in bu kalkanı nasıl kurduğunu çözdüler. PDHA1 asetil‑CoA üretimine katkıda bulunduğu için DNA’nın nasıl paketlendiği ve okunduğunu değiştirip değiştirmediğini test ettiler. PDHA1 yüksek olduğunda asetil‑CoA düzeyleri ve özellikle aktif genlerle ilişkili bir histon asetil işareti dahil olmak üzere histon proteinlerindeki kimyasal “asetil” etiketleri arttı. Bu artıştan fayda sağlayan önemli hedeflerden biri, sisteini hücre içine çekip glutatyon üretimine katkıda bulunan taşıyıcı SLC7A11 oldu. Daha fazla PDHA1 ile hücreler daha fazla glutatyon üretti; PDHA1 azaldığında sistein ve glutatyon düştü. Glutatyon ise bakırı bağlayıp etkisiz hale getirerek kuproptozu tetikleyen stresi azalttı. Glutatyonun veya SLC7A11’in geri verilmesi, PDHA1 bloke edildiğinde görülen artmış bakır stresini geri alabiliyordu; bu da PDHA1–asetil‑CoA–histon–SLC7A11–glutatyon zincirinin kanser hücrelerinin bakırı temizleyip ölümden kaçmasına izin verdiğini gösteriyor.
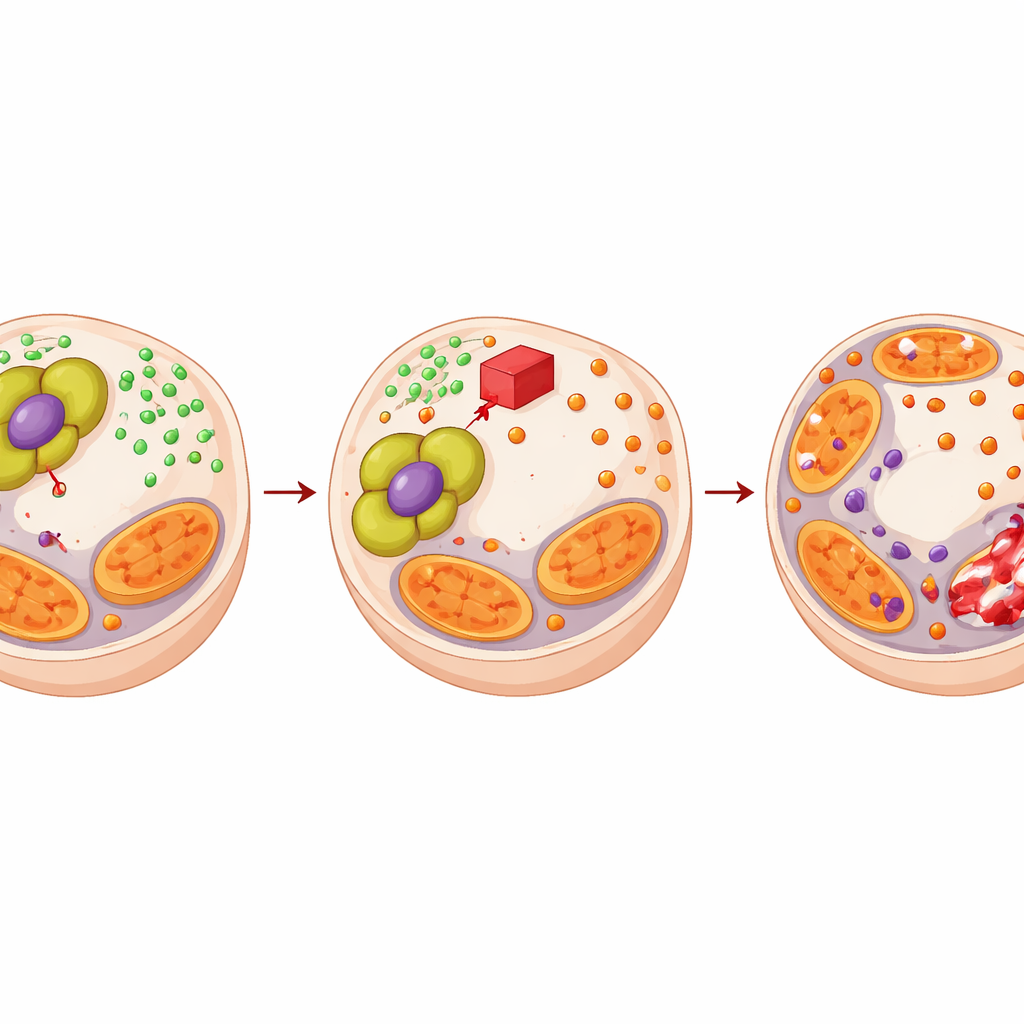
Bir zafiyeti tedavi stratejisine dönüştürmek
PDHA1 bu bakır tamponlama sistemini güçlendirerek tümörlerin enzalutamide karşı direnmesine yardımcı olduğundan yazarlar PDHA1 hedefli bir ilacın durumu tersine çevirip çeviremeyeceğini sordular. Aynı metabolik kompleksi bozan CPI‑613 adlı bir bileşik kullandılar. CPI‑613 tek başına prostat kanseri hücrelerinde bakır stresini artırdı ve mitokondri proteinlerine zarar verdi ancak normal prostat hücrelerine fazla zarar vermedi. Enzalutamid ile birlikte kullanıldığında CPI‑613, her iki tedavinin tek başına yaptığı etkiyi katlayarak kanser hücresi büyümesini çok daha fazla azalttı; matematiksel analiz gerçek bir sinerjiyi doğruladı. Fare tümör modellerinde ve hastadan türetilmiş tümör implantlarında ilaç çiftinin uygulanması, daha küçük tümörler, daha fazla ölü doku, daha az bölünen hücre ve bakır kaynaklı hücre ölümü imzalarının güçlenmesiyle sonuçlandı.
Hastalar için ne anlama geliyor
Bu bulgular birlikte bazı prostat kanserlerinin enzalutamidden kaçmak için metabolizmalarını yeniden düzenleyip daha fazla asetil‑CoA ürettiklerini, gen aktivitesini yeniden yazdıklarını ve toksik bakırı emen glutatyonu artırdıklarını gösteriyor; bu da kuproptozu engelliyor. PDHA1’i inhibe ederek bu koruyucu devre dağıtılabilir, böylece bakır kaynaklı hücre ölümü ilerleyebilir ve hormon baskılayıcı tedavinin etkisi yeniden sağlanabilir. Klinik denemeler hâlâ gerekli olsa da bu çalışma somut, test edilebilir bir stratejiye işaret ediyor: ileri evre ve tedavisi güç prostat kanserli erkeklerde direnci aşmak için enzalutamid ile CPI‑613 gibi PDHA1 hedefli ilaçların eşleştirilmesi.
Atıf: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
Anahtar kelimeler: prostat kanseri, ilaç direnci, bakır kaynaklı hücre ölümü, kanser metabolizması, epigenetik düzenleme