Clear Sky Science · tr
USP30 aracılı Deubiquitinasyonunun Hemokinaz 2’nin Glukoz Metabolik Kaderini ve Tümör İlerlemesini Kontrol Etmesi
Kanser Hücreleri Şeker Kullanımını Nasıl Yeniden Düzenliyor
Kanser hücreleri “şeker tutkunu” olmalarıyla bilinir: hızlı büyümeyi desteklemek için şekeri alışılmadık biçimlerde yakarlar. Bu çalışma, tümör hücrelerinin glukozu nasıl kullanacaklarına karar vermesine yardımcı olan USP30 adında yeni bir anahtar proteini ortaya koyuyor. Hemokinaz 2 (HK2) adlı diğer bir proteini hassas şekilde ayarlayarak USP30, kanser hücrelerini daha fazla şeker yakmaya ve daha hızlı büyümeye ittiği için gelecekteki anti-kanser ilaçlar için yeni bir hedefe işaret ediyor. 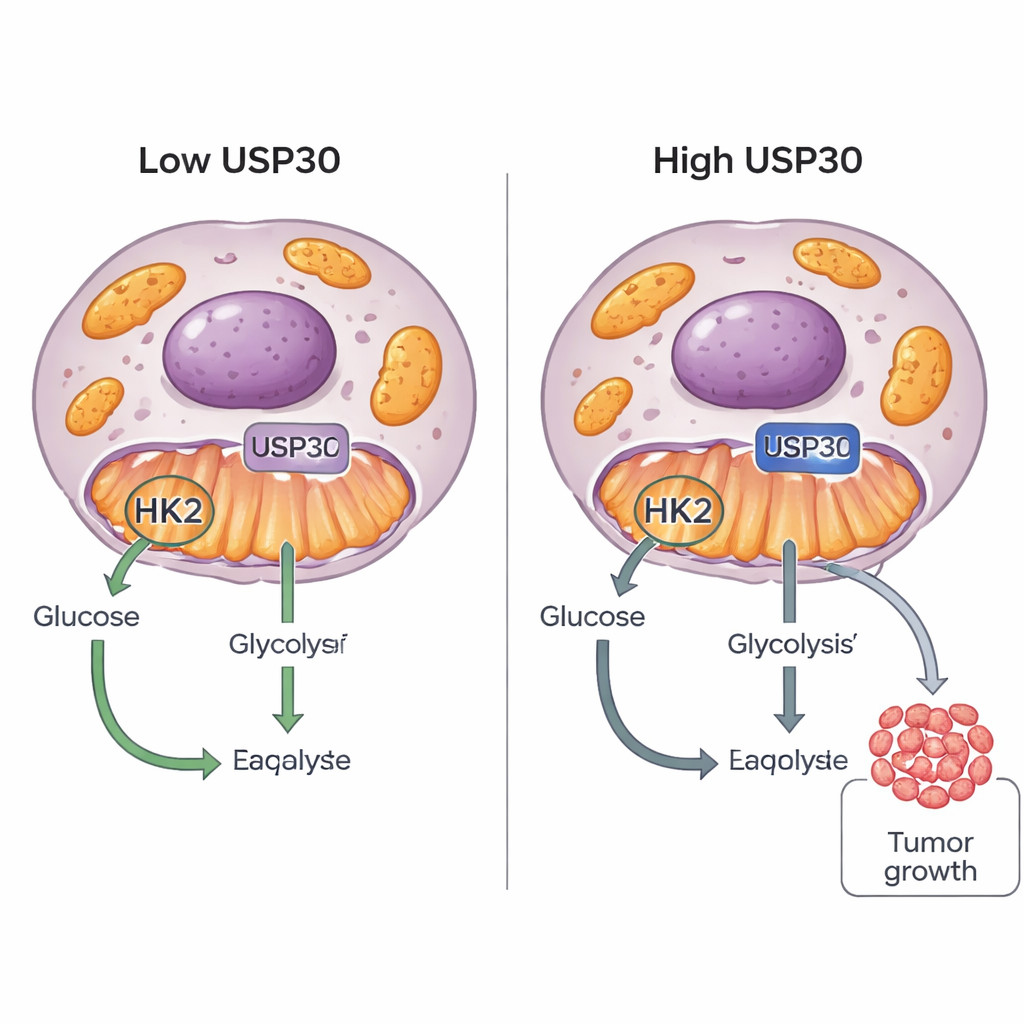
Tümörlerin İçindeki Şeker Yiyen Yaşam Tarzı
Çoğu sağlıklı hücre besinlerden verimli şekilde enerji elde eder, ancak birçok kanser hücresi Warburg etkisi olarak da bilinen hızlı ve verimsiz bir yol olan aeropik glikolizi tercih eder. Oksijen yeterliyken bile bol miktarda glukoz alır ve hızla laktata çevirirler. Bu strateji yalnızca enerji üretmekle kalmaz: DNA, yağ ve protein için yapı taşları sağlar, tümörlerin strese dayanmasına yardımcı olur ve bağışıklık saldırılarını zayıflatabilir. Bu yolun girişinde, gelen glukozu fosfatla işaretleyip onu daha fazla yıkıma ve büyümeyi destekleyen kimyasallara bağlayan hemokinaz bulunur.
Mitochondriyal Bir Enzim Sahneye Çıkıyor
USP30, hücrenin enerji santralleri olan mitokondrilerin dış yüzünde yer alan bir enzimdir. Ubiquitin adı verilen küçük protein etiketlerini diğer proteinlerden çıkaran “deubiquitinazlar” aileye aittir; bu çıkarma genellikle hedef proteinin kararlılığını, konumunu veya aktivitesini değiştirir. USP30 daha önce beyin hücrelerindeki rollerinde ve mitokondri kalitesinin kontrolünde bilinmesine rağmen, kanser üzerindeki etkisi belirsizdi. Büyük kanser gen veri tabanlarını tarayarak araştırmacılar, USP30 düzeyi yüksek tümörlerin daha güçlü glukoz yakma imzaları ve daha zayıf yağ yakma imzaları gösterme eğiliminde olduğunu fark ettiler; bu da USP30’un kanserlerin şekerle beslenen bir yaşam tarzına kaymasına yardımcı olabileceğini düşündürdü.
USP30’u Hücrenin Şeker Bekçileriyle Bağlamak
Bu bağlantıyı incelemek için ekip, birkaç kanser hücre hattında USP30’u azalttı veya ortadan kaldırdı ve enerji işleyişlerini ölçtü. Asit üretimini ve oksijen kullanımını gerçek zamanlı izleyen cihazlarla yaptıkları ölçümlerde, USP30 kaybının hem glikoliz hem de mitokondriyal solunumu keskin şekilde azalttığını buldular. Laktat üretimi ve glukoz tüketimi düştü; hücrelerin şeker yakma motoru yavaşlamıştı. Ardından yapılan kütle spektrometrisi deneyleri USP30’un özellikle hemokinazlar HK1 ve HK2 olmak üzere glukoz metabolizmasıyla ilişkili birkaç enzimle fiziksel etkileşime girdiğini ortaya koydu. İzleme testleri bu etkileşimin USP30’un katalitik aktivitesine bağlı olduğunu ve dolaylı ortaklar aracılığıyla değil doğrudan gerçekleştiğini gösterdi.
Hemokinaz 2 Üzerinde Kesin Bir Moleküler Tutamaç
Daha derine inildiğinde, araştırmacılar USP30’un HK1 ve HK2’den olağandışı ubiquitin zincirleri adı verilen belirli tiplerdeki ubiquitin bağlarını çıkardığını buldular. HK2 için bu düzenleme tek bir kritik amino asitte, lizin 144 (K144) üzerinde gerçekleşiyor. K144 artık ubiquitin taşıyamayacak şekilde değiştirildiğinde, HK2 daha kararlı hale geliyor, mitokondrideki VDAC1 adlı kanal proteiniyle daha güçlü bağlanıyor ve daha yüksek enzim aktivitesi gösteriyor. Bu K144 değişikliğini taşıyan hücreler daha fazla HK2’yi mitokondriye gönderdi, daha fazla glukoz yaktı, daha fazla laktat saldı ve laboratuvar kaplarında daha hızlı büyüme ve hareket sergiledi. Farelerde, K144 mutant HK2 taşıyan hücrelerden büyüyen tümörler normal HK2’ye sahip olanlardan daha büyük ve hızlı büyüdü; bu küçük moleküler anahtarın etkisinin altını çizdi. 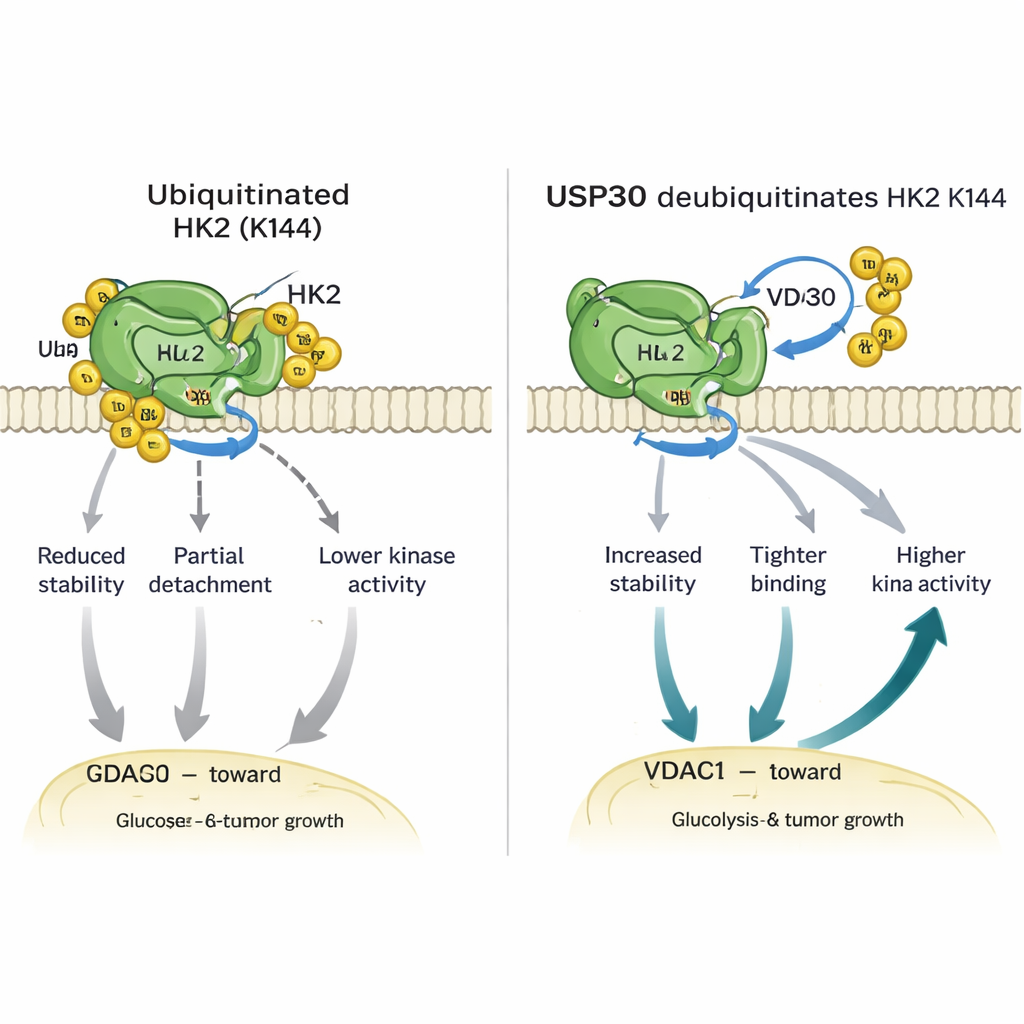
Bir Metabolik Anahtarı Büyüme Avantajına Çevirmek
Bu sonuçlar net bir olay zincirini haritalandırıyor: USP30 HK2’ye bağlanıyor, K144’ten ubiquitin etiketlerini çıkarıyor ve böylece HK2’yi aktif ve mitokondri üzerinde sabit tutuyor. Bu, glikolizi artırıyor, tümör hücresi bölünmesi ve göçünü besliyor ve nihayetinde tümör büyümesini hızlandırıyor. USP30 eksik veya etkisiz olduğunda HK2 daha az kararlı ve daha az etkili oluyor ve kanser hücreleri metabolik avantajlarının bir kısmını kaybediyor. Gayri uzman bir bakışla, USP30 tümör hücresinin şeker motorunu ayarlı ve yerinde tutan bir tamirci gibi davranıyor—tamirciyi çıkarın, motor sekteye uğruyor.
Gelecek Kanser Tedavileri İçin Anlamı
Bir uzman olmayan için alınacak ana mesaj şudur: kanser hücreleri şekeri nasıl yaktıkları üzerinde ince ayarlı kontrol mekanizmalarına dayanır ve USP30 bu kontrol panelinde yeni keşfedilmiş bir düğmedir. USP30, HK2’yi tek bir spesifik yerde stabilize ederek tümörlerin glukoz açlığını destekleyen metabolizmayı sürdürmesine yardımcı olur ve daha agresif büyümeyi kolaylaştırır. USP30’u bloke eden ilaçlar veya USP30’un HK2’ye, özellikle lizin 144’teki tutuşunu bozan yaklaşımlar, tümörleri şekere bağlı motorlarını zayıflatarak zayıflatabilir; bu, normal hücreleri aynı ölçüde zarar görmeyecek biçimde hedefleme şansı sunar. Bu çalışma böylece kanserin metabolizmayı nasıl yeniden düzenlediğine dair önemli bir parça ekliyor ve hedefe yönelik terapiler için umut verici yeni bir açı öneriyor.
Atıf: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Anahtar kelimeler: kanser metabolizması, glikoliz, hemokinaz 2, USP30, Warburg etkisi