Clear Sky Science · tr
İnsan iPSC kökenli duyusal nöronlarda paklitaksel maruziyetinin zaman çözünür çok-omik analizi: kemoterapi kaynaklı periferik nöropatinin mekanizmalarını ortaya çıkarma
Neden bazı kanser ilaçları sinirlere zarar veriyor
Kemoterapi milyonlarca insanın kanseri yenmesine yardımcı oldu, ancak birçok hasta bunun gizli bir bedelini ödüyor: ellerde ve ayaklarda aylarca ya da yıllarca sürebilen yanma, karıncalanma ve uyuşukluk. Bu çalışma basit ama önemli bir soruyu soruyor: yaygın olarak kullanılan paklitaksel adlı kanser ilacı insan duyusal sinir hücrelerine tam olarak ne yapıyor ve bu değişikliklerin anlaşılması sinir hasarının daha iyi önlenmesi ve tedavisine nasıl ışık tutabilir?
Hastaların hücrelerinden laboratuvarda yetiştirilmiş ağrı algılayan sinirlere
Araştırmacılar hayvan deneylerine dayanmak yerine beş insan bağışçının hücreleriyle çalıştı; bunlar arasında paklitaksel alan meme kanseri hastaları da vardı. Bu hücreleri indüklenmiş pluripotent kök hücrelere (iPSC) dönüştürdüler ve ardından bunları duyusal nöronlara yönlendirdiler—deriden omuriliğe dokunma ve ağrı sinyallerini taşıyan aynı sinir hücresi türü. Laboratuvarda yetişen bu nöronlar uzun, ince lifler geliştirdi ve vücut içindeki gerçek ağrı algılayıcı sinirlere çok benzeyen elektriksel aktivite gösterdi. Ekip daha sonra bunları hastalarda görülen ilaç düzeylerini taklit ederek artan dozlarda paklitaksele maruz bıraktı ve birkaç gün boyunca hücre sağlığını izledi. Düşük konsantrasyonlarda nöronlar iyi dayanırken, klinik olarak anlamlı bir dozda (100 nM) hayatta kalma oranı yaklaşık iki gün sonra düşmeye başladı ve bu toksik sinir hasarının başlangıcını işaret etti.
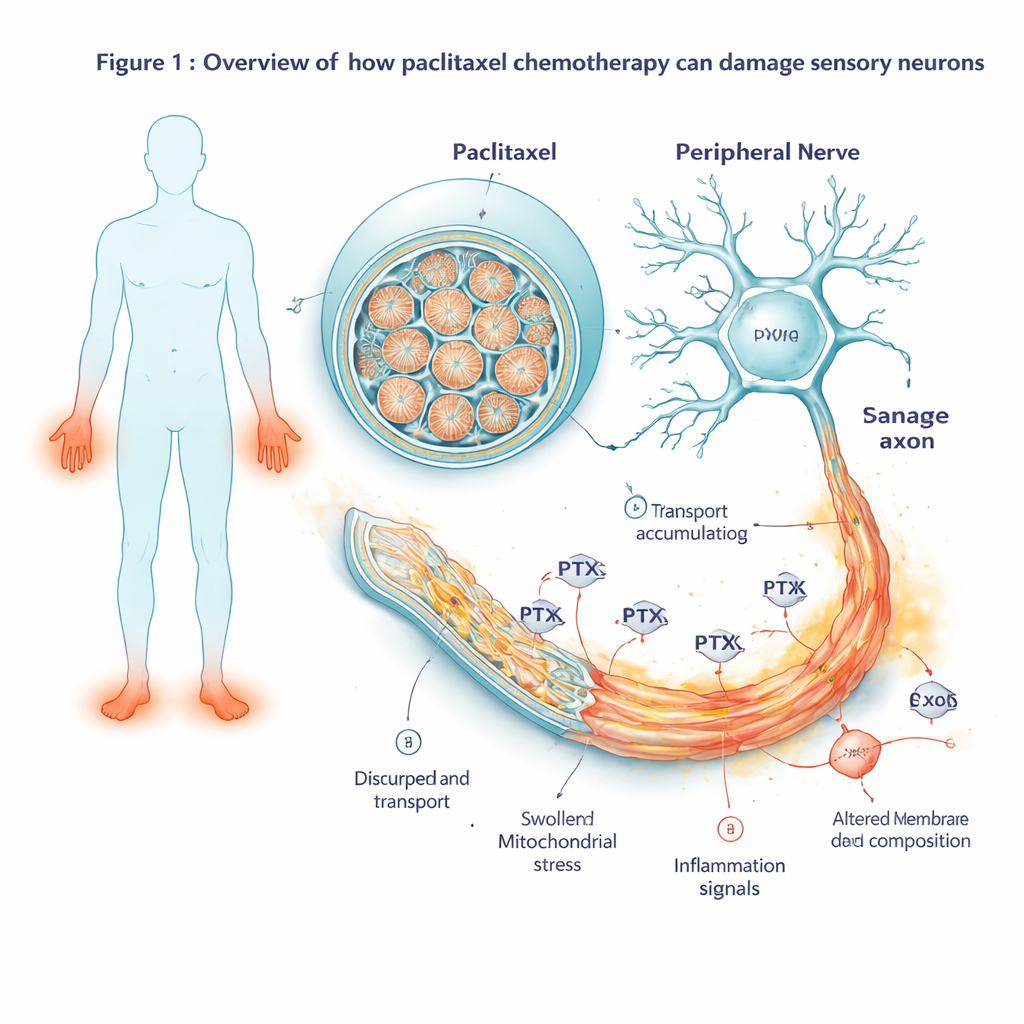
Zaman içinde gen aktivitesini izlemek
Hücreler gözle görülür şekilde bozulmadan önce nasıl yanıt verdiklerini görmek için bilim insanları ilaç maruziyetinin iki saat sonundan ilacın yıkanmasından birkaç gün sonrasına kadar birden çok zaman noktasında hangi genlerin açılıp kapandığını ölçtüler. Erken dönemde JUN adlı bir gen etrafında toplanan klasik bir hücresel stres programının aktive olduğunu gördüler. Maruziyet devam ettikçe bu stres sinyali daha geniş bir kendini yok etme kaskadına dönüştü: hücreleri programe edilmiş ölüme iten genler güçlü şekilde açılırken koruyucu ortaklar yeterince etkili olamadı. Aynı zamanda enflamasyon ve ağrı sinyallemesine bağlı genler daha aktif hale geldi. Nöronlar daha fazla enflamatuar haberci, ağrı ilişkili peptitler ve hücreleri zararlı uyaranlara daha duyarlı yapan reseptörler üretmeye başladı; bu değişiklikler ağrılı sinir bozukluklarında görülenlerle paralel.
Nöronların içindeki proteinler ve yağlara derin bakış
Genler yalnızca bir plan olduğundan, ekip ayrıca nöronlarda gerçekten bulunan proteinleri ve lipid (yağ) bileşimini de inceledi. Paklitaksel maruziyetinin 48 saatinden sonra RNA düzeyinde tespit edilen birçok stres ve enflamatuar sinyal protein seviyelerinde de artmış olarak belirdi; bu, nöronların bu zararlı programları uyguladığını doğruladı. Çarpıcı şekilde, aksonal taşıma için gereken proteinler—uzun sinir lifleri boyunca kargoyu hareket ettiren moleküler motorlar ve iskeletler—keskin şekilde azaldı. Buna kinesinler ve mikrotübül yollarını stabil tutan düzenleyici proteinler de dahildi. Lipid düzeyinde ise nöronlar kolesterol ve membran lipidleri için önemli yapı taşlarında bir düşüş ve depolanmış yağlar olan triagliserollerde bir artış gösterdi. Bu değişimler bir arada paklitakselin yalnızca hücre ölüm yollarını tetiklemediğini, aynı zamanda sinir liflerinin fiziksel yapısını ve enerji dengesini zayıflattığını düşündürüyor.
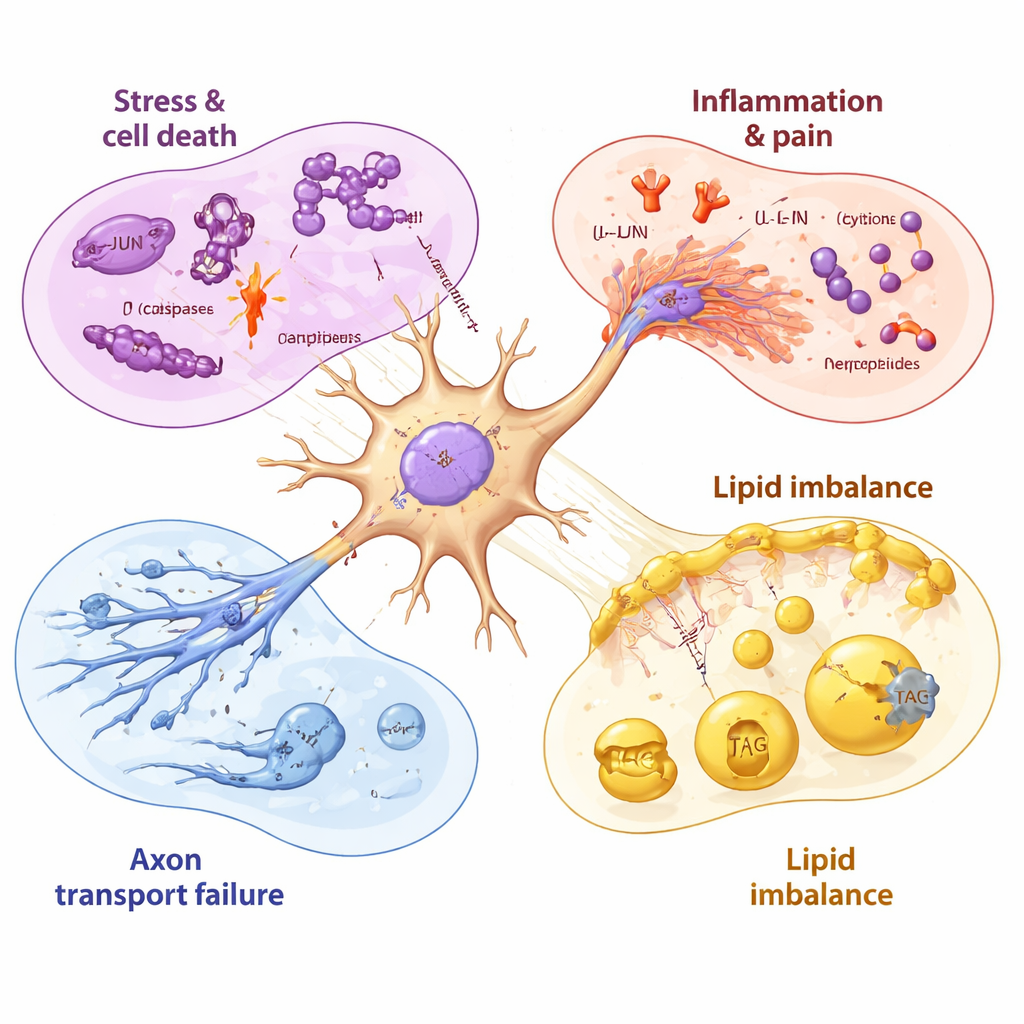
Sinir yaralanması ve eksik iyileşme zaman çizelgesi
Araştırmacılar nöronları ilaç maruziyeti öncesinde, sırasında ve sonrasında örnekleyerek bu olayları zaman içinde sıra ile dizmeyi başardı. Saatler içinde mitokondriyel (enerjiyle ilgili) genler bozuldu, ardından stres geni JUN aktifleşti ve canlılık düşmeye başladıkça hücre ölümü ve enflamatuar programların daha güçlü aktivasyonu izlendi. Paklitaksel uzaklaştırıldıktan sonra bile birçok zararlı sinyal günlerce yüksek kaldı; sağlıklı membran lipidleri yapmak için gereken genler ise düşmeye devam etti. Bazı geç yükselen moleküller—paklitakseli dışarı atabilen bir ilaç-efluks pompası ve belirli büyüme faktörleri gibi—nöronların kendilerini korumaya ve onarmaya çalıştığını gösterse de; bu yanıtlar hasara doğru hızlı, erken eğilime kıyasla görece yavaş ve eksik görünüyordu.
Sinir ağrısıyla yaşayan hastalar için bunun anlamı
Halk için mesaj şu: paklitaksel duyusal sinirlere bir dizi koordineli darbe ile zarar veriyor—enerji sistemlerini zorluyor, hücresel ölümü yönlendiren genetik anahtarları çeviriyor, enflamasyon ve ağrı sinyallemesini kışkırtıyor, sinir lifleri içindeki içsel “taşıma otoyollarını” bozuyor ve sinir membranlarını stabil tutan yağları değiştiriyor. Bu değişiklikleri insan kökenli nöronlarda ayrıntılı biçimde haritalandırarak çalışma, sinirleri kanser tedavisinin etkinliğini zayıflatmadan korumak için hedef alınabilecek somut, ilaçlanabilir hedefleri—örneğin belirli stres düzenleyicileri, enflamatuar reseptörler ve lipid sentezleyen enzimleri—vurguluyor. Yeni tedaviler daha fazla test gerektirse de, bu çalışma kemoterapi kaynaklı sinir hasarını önleme veya hafifletme yolunda daha net bir yol haritası sunuyor ve kanserden kurtulanların yaşam kalitesini iyileştirme potansiyeli taşıyor.
Atıf: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Anahtar kelimeler: kemoterapi kaynaklı periferik nöropati, paklitaksel, duyusal nöronlar, nöroenflamasyon, aksom dejenerasyonu