Clear Sky Science · tr
Geri dönüşümlü arginin metilasyonu mitokondriyal IDH2 aktivitesini düzenliyor: CARM1 ve KDM3A/4A tarafından koordineli kontrol
Hücrenin Enerji Santrallerini İnce Ayarlamak
Hücrelerimizin enerji santralleri olarak anılan mitokondriler yalnızca enerji üretmekten fazlasını yapar. Yakıt yakma biçimlerini sürekli olarak vücudun ihtiyaçlarına uyacak şekilde ayarlarlar ve bu süreç bozulduğunda diyabet, kalp yetmezliği ve kanser gibi hastalıklara katkıda bulunabilir. Bu çalışma, mitokondriler içinde gizli bir “karartma düğmesini” ortaya çıkarıyor: bir ana enzimin, IDH2’nin tek bir yapı taşındaki küçük bir kimyasal işaret, mitokondrilerin düşük devreden yüksek enerji üretimine geçip geçmeyeceğine yardımcı oluyor.
Büyük Sonuçları Olan Küçük Bir İşaret
Hücrelerimizdeki proteinler durağan değildir; davranışlarını değiştiren küçük kimyasal gruplarla sıkça modifiye olurlar. Hücrenin çekirdeği ve sıvı içindeki birçok böyle değişiklik iyi bilinirken, mitokondri içindekiler daha az keşfedilmiştir. Yazarlar arginin metilasyonu adı verilen belirli bir işaret türüne odaklandı ve bunun mitokondriyal enzimleri kontrol edip etmediğini sordular. Trikarboksilik asit (TCA) döngüsünün önemli bir çalışanı olan ve besinleri enerji ve önemli metabolik yapı taşlarına çeviren IDH2 enzimi üzerinde yoğunlaştılar. Biyokimyasal araçlar ve kütle spektrometrisi kullanarak, IDH2’nin spesifik olarak bir aminoasit olan arginin 188 üzerinde bir metil işareti taşıdığını ve bu işaretin şaşırtıcı biçimde mitokondri içinde faaliyet gösteren CARM1 adlı bir enzim tarafından yerleştirildiğini buldular.
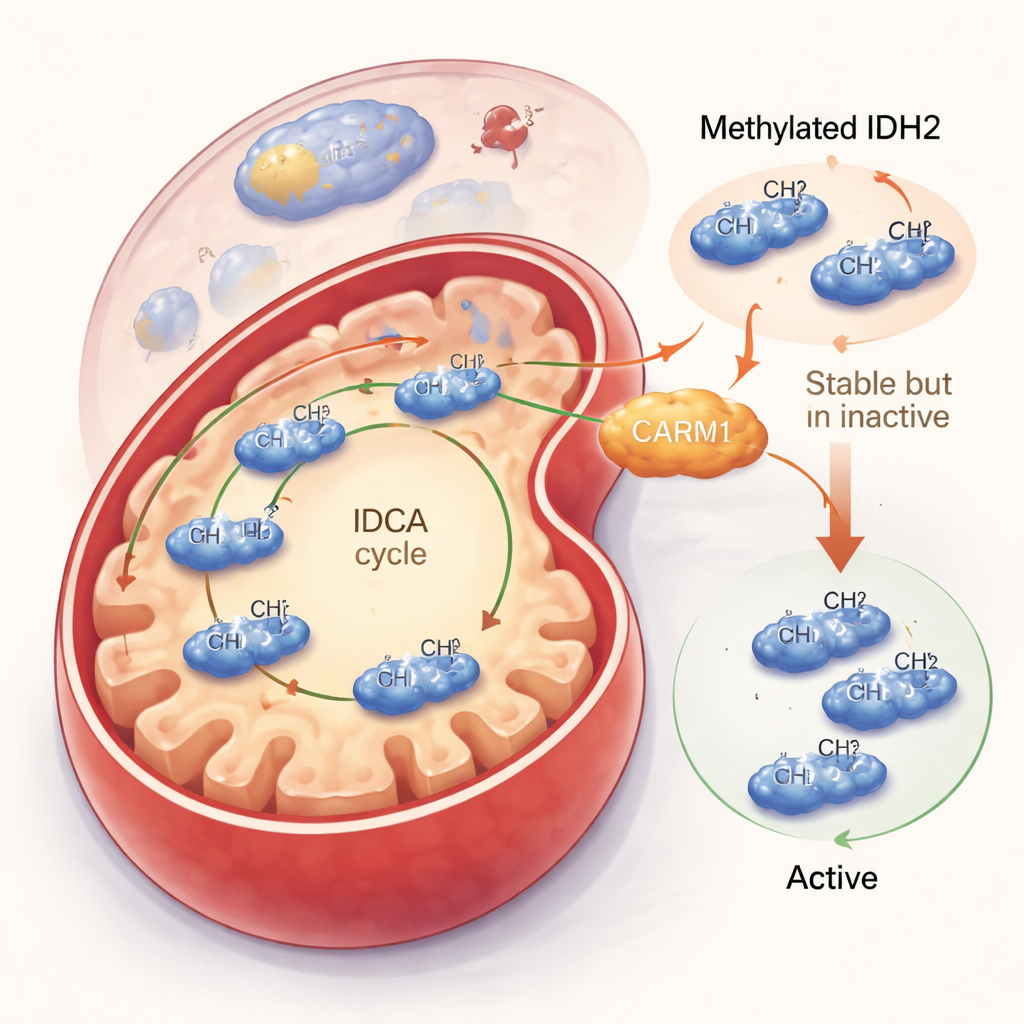
IDH2’yi Sönümlendirmek ama Daha Uzun Süre Yaşatmak
Araştırma ekibi bu metil işaretinin aslında ne yaptığını sordu. CARM1 etkin olduğunda ve IDH2’yi metilebildiğinde, IDH2 proteini daha stabil hale geldi ve hücrede daha uzun süre kaldı. Ancak bu görünür avantaj bir takas ile geldi: metillenmiş IDH2 daha az aktiftir. Hücre deneyleri ve saflaştırılmış protein testlerinde, metillenmiş IDH2 ana ürünü olan alfa-ketoglutarat üretimini ve koruyucu molekül NADPH üretimini azaltıyordu. Buna karşılık, arginin 188 üzerinde metillenemeyen bir IDH2 versiyonu daha aktif dimer şeklini daha fazla oluşturdu, daha hızlı çalıştı ve hem alfa-ketoglutarat hem de NADPH seviyelerini artırdı. Toplamda bu metillenmemiş IDH2 daha az bulunmasına rağmen, her bir molekül daha fazla iş yaptığı için mitokondri çıkışında net bir artışa yol açtı.
İki Silgisi Olan Geri Döndürülebilir Bir Anahtar
Önemli olarak, bu metil işareti kalıcı değildir. Araştırmacılar, normalde farklı bir işareti kaldırmalarıyla bilinen lizinin demetilazları KDM3A ve KDM4A adlı iki enziminin de IDH2 üzerindeki arginin metil işaretini silebildiğini gösterdi. Bu demetilazlar var olduğunda, 188 pozisyonundaki metillenmiş arginin ekstra kimyasal gruplarını kaybetti, IDH2 daha az stabil fakat daha aktif hale geldi ve dimer formu arttı. Daha aktif KDM3A veya KDM4A’ya sahip hücreler daha yüksek mitokondriyal membran potansiyeli gösterdi ve daha fazla oksijen tükettikçe, bunlar mitokondrilerinin oksidatif metabolizmada daha fazla çalıştığına işaretti. Bu enzimler azaltıldığında ise tersi oldu: IDH2 aktivitesi düştü ve mitokondri performansı azaldı; bu da bunun tek yönlü değil, geri döndürülebilir bir kontrol sistemi olduğunu vurguluyor.
Metabolizma ile Hastalık Arasındaki Bağ
IDH2 kanser ve diğer bozukluklarla ilişkilendirildiği için yazarlar bu metilasyon anahtarının hastalığa benzer ortamlarda ne kadar önemli olabileceğini incelediler. Çeşitli normal ve kanser hücre hatlarında, daha yüksek IDH2 protein düzeylerinin sıklıkla daha fazla metilasyon ve şaşırtıcı şekilde daha düşük enzim aktivitesi ile el ele gittiğini gözlemlediler; bu da “daha fazla protein”in her zaman “daha fazla fonksiyon” anlamına gelmediğini düşündürüyor. Meme kanseri veri setlerinde, daha yüksek IDH2 protein seviyelerine sahip hastalar genellikle daha kötü sağkalım gösterdi; oysa IDH2 gen aktivitesi sonuçla paralel değildi. Sonuçlar, CARM1 kaynaklı metilasyonun TCA döngüsünü yavaşlattığı ve hücreleri besinleri kullanmanın kanser tarafından tercih edilen alternatif yollarına iteleyebileceği; KDM3A ve KDM4A gibi demetilazların ise hücreleri daha verimli enerji üretimine geri itebileceği modelini destekliyor.
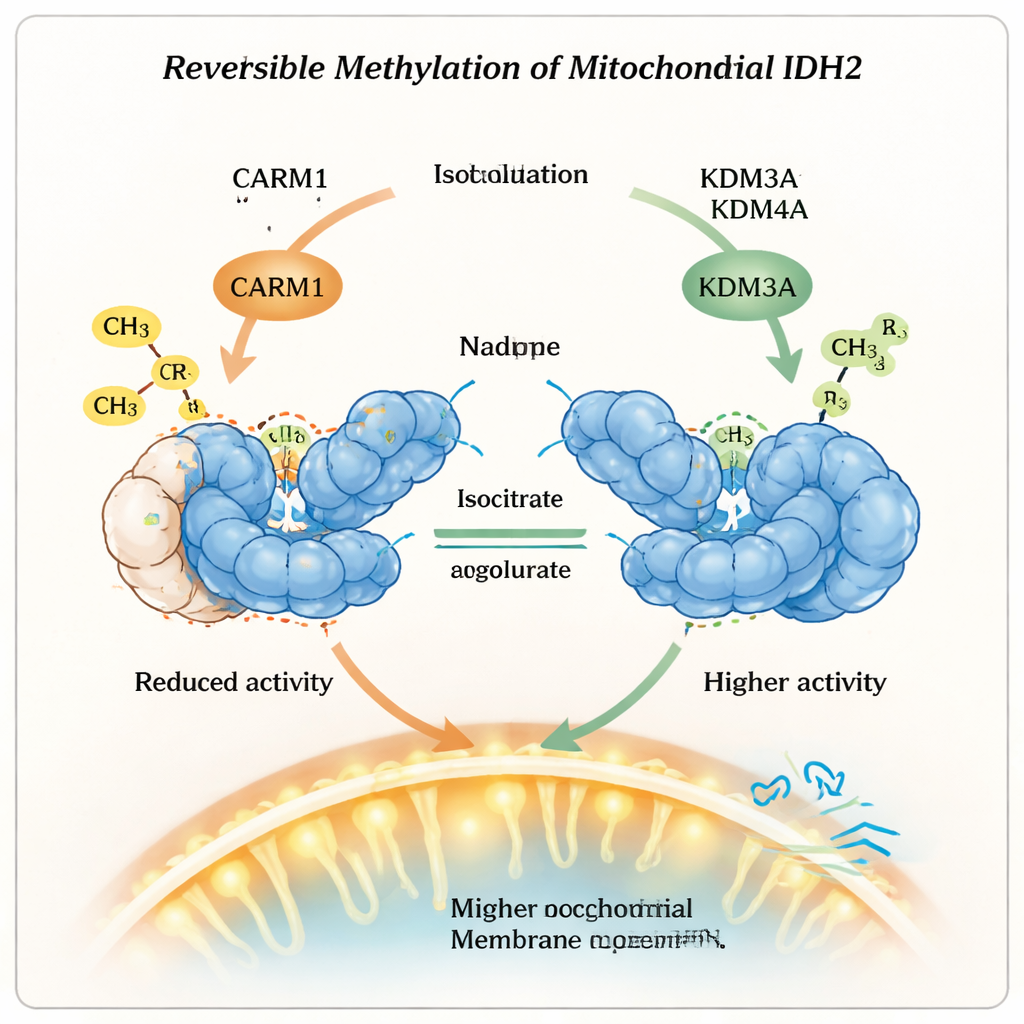
Sağlık ve Tedavi Açısından Anlamı
Günlük terimlerle, bu çalışma mitokondrilerin enzimleri basitçe açıp kapatmadığını, bunun yerine geri döndürülebilir kimyasal işaretleri ince ayarlı düğmeler olarak kullandığını gösteriyor. Bir metil grubu ekleyerek CARM1, IDH2’yi daha uzun ömürlü ama daha az aktif bir forma çeviriyor; bu etiketi kaldırarak KDM3A ve KDM4A bazı stabiliteyi feda edip daha fazla güç çıktısı sağlıyor. Bu denge, hücrelerin hızlı ama verimsiz şeker yakımı ile daha yavaş fakat daha verimli enerji üretimi arasında nasıl seçim yaptıklarını etkiliyor. IDH2 üzerindeki bu metilasyon “karartma düğmesini” anlamak, bu küçük ama güçlü kimyasal işaretleri yazan ve silen enzimleri hedefleyerek kanser ve metabolik hastalıklar gibi durumlardaki bozuk mitokondriyal metabolizmayı düzeltmeyi amaçlayan yeni tedavi olasılıklarını açıyor.
Atıf: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Anahtar kelimeler: mitokondri, IDH2, arginin metilasyonu, hücre metabolizması, CARM1