Clear Sky Science · tr
KDM5B, kolesterol metabolizmasını düzenleyerek ER+ meme kanserinin tümör oluşumunu teşvik etmek için CRL4B kompleksi ile iş birliği yapar
Bu araştırma gündelik sağlık açısından neden önemli
Meme kanseri kadınlarda en yaygın görülen kanserdir ve birçok tümör östrojen hormonu etkisiyle büyür. Bu kanserler yalnızca hızlı bölünmezler—aynı zamanda kolesterol gibi yağların kullanım şeklini yeniden düzenlerler. Bu çalışma, KDM5B adındaki bir gen düzenleyici proteinin CRL4B adlı başka bir protein kompleksiyle iş birliği yaparak östrojen reseptör‑pozitif (ER+) meme kanseri hücrelerinde kolesterolü artırdığını ortaya koyuyor. Bu gizli ortaklığı anlamak, araştırmacıların tümör büyümesini yavaşlatmak ve hormon terapisi ile kolesterol düşürücü ilaçlar gibi mevcut tedavileri geliştirmek için yeni yollar bulmasına yardımcı olabilir.
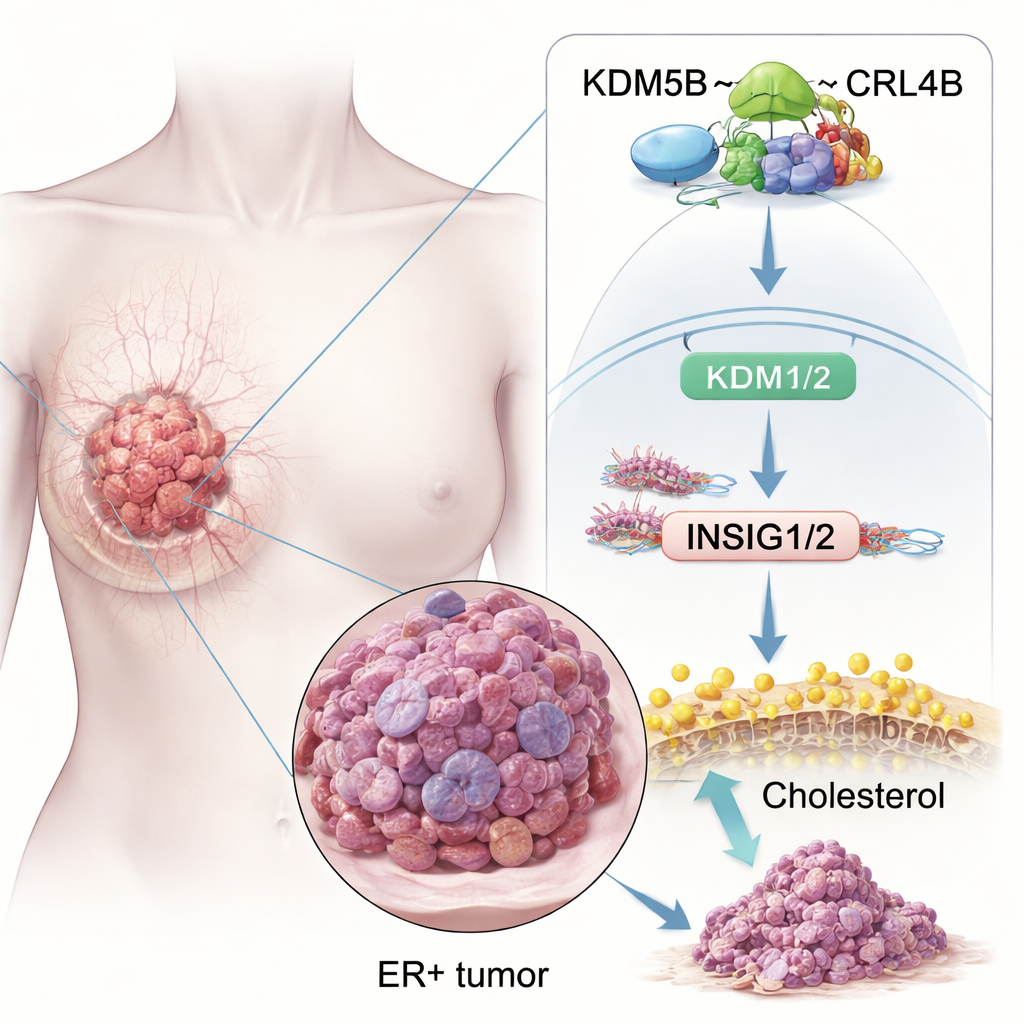
Kansere yatkınlığı artıran bir protein
Araştırmacılar önce KDM5B’nin ER+ meme kanserlerinde yalnızca bulunduğunu mu yoksa gerçekten de süreci mi hızlandırdığını sordular. Büyük kanser veri tabanları ve doku örneklerinin analizinde KDM5B seviyelerinin normal meme dokusuna göre tümörlerde daha yüksek olduğunu ve özellikle ER+ tümörlerde çok daha fazla olduğunu buldular. Kanserleri daha fazla KDM5B üreten hastaların sağkalımları, standart kemoterapi veya hormon terapisi alsalar bile daha kötü olma eğilimindeydi. Hücre kültürü deneylerinde KDM5B’nin arttırılması ER+ meme kanseri hücrelerinin daha hızlı çoğalmasına, çevre dokuyu daha kolay işgal etmesine ve yeni tümörleri başlatan kök hücre benzeri kümeler oluşturmasına neden oldu. KDM5B’nin azaltılması ise ters etki göstererek kültürdeki koloni sayısını ve farelerdeki tümörleri küçülttü.
Moleküler düzeyde güçlü bir ortaklık
KDM5B’nin bu etkileri nasıl oluşturduğunu görmek için ekip protein ortaklarını aradı. KDM5B’nin CRL4B kompleksi olarak adlandırılan moleküler bir makinenin parçalarına fiziksel olarak bağlandığını keşfettiler; bu kompleks proteinleri işaretleyen ve DNA paketlenme şeklini değiştiren bir enzim sistemidir. Ayrıntılı biyokimyasal testler KDM5B’nin CUL4B ve DDB1 adlı iki CRL4B bileşeniyle proteinlerin özgül bölgeleri üzerinden doğrudan etkileştiğini gösterdi. ER+ meme kanseri hücrelerinde bu KDM5B–CRL4B kompleksi birçok genin açma/kapama anahtarlarına etki ediyor. Genom çapında haritalama kullanılarak yazarlar KDM5B ve CUL4B’nin sıklıkla gen promotörlerinde bir arada bulunduğunu ve histon proteinleri üzerindeki kimyasal işaretleri değiştirerek genleri kapattıklarını gösterdiler.
Kolesterol üzerindeki frenleri serbest bırakmak
Etkilenen birçok yol arasında kolesterol metabolizması öne çıktı. Kanser hücreleri zar inşa etmek ve stresle başa çıkmak için ekstra kolesterole ihtiyaç duyar ve ER+ tümörler ayrıca östrojen taklidi yapan kolesterol türevli molekülleri kullanır. Çalışma, KDM5B–CRL4B kompleksinin iki önemli “fren” geni INSIG1 ve INSIG2’nin kontrol bölgelerine doğrudan bağlandığını gösteriyor. Bu genler normalde ana kolesterol düzenleyicisi SREBP2’yi kontrol altında tutmaya yardımcı olur. KDM5B–CRL4B, INSIG1/2 promotörlerindeki histonlara baskılayıcı bir işaret (H2AK119ub1) ekliyor ve etkinleştirici bir işaret (H3K4me3) çıkarıyor; böylece bu genlerin ifadesini azaltıyor. Daha az INSIG1/2 proteiniyle SREBP2 serbest kalarak kolesterol yapım genlerini açıyor, ER+ meme kanseri hücreleri içinde kolesterolü yükseltiyor ve hücrelerin istilacı davranışını artırıyor. Araştırmacılar KDM5B veya CRL4B’yi bozduklarında INSIG1/2 düzeyi yükseldi, SREBP2 aktivitesi düştü ve hücrelerde toplam kolesterol azaldı.
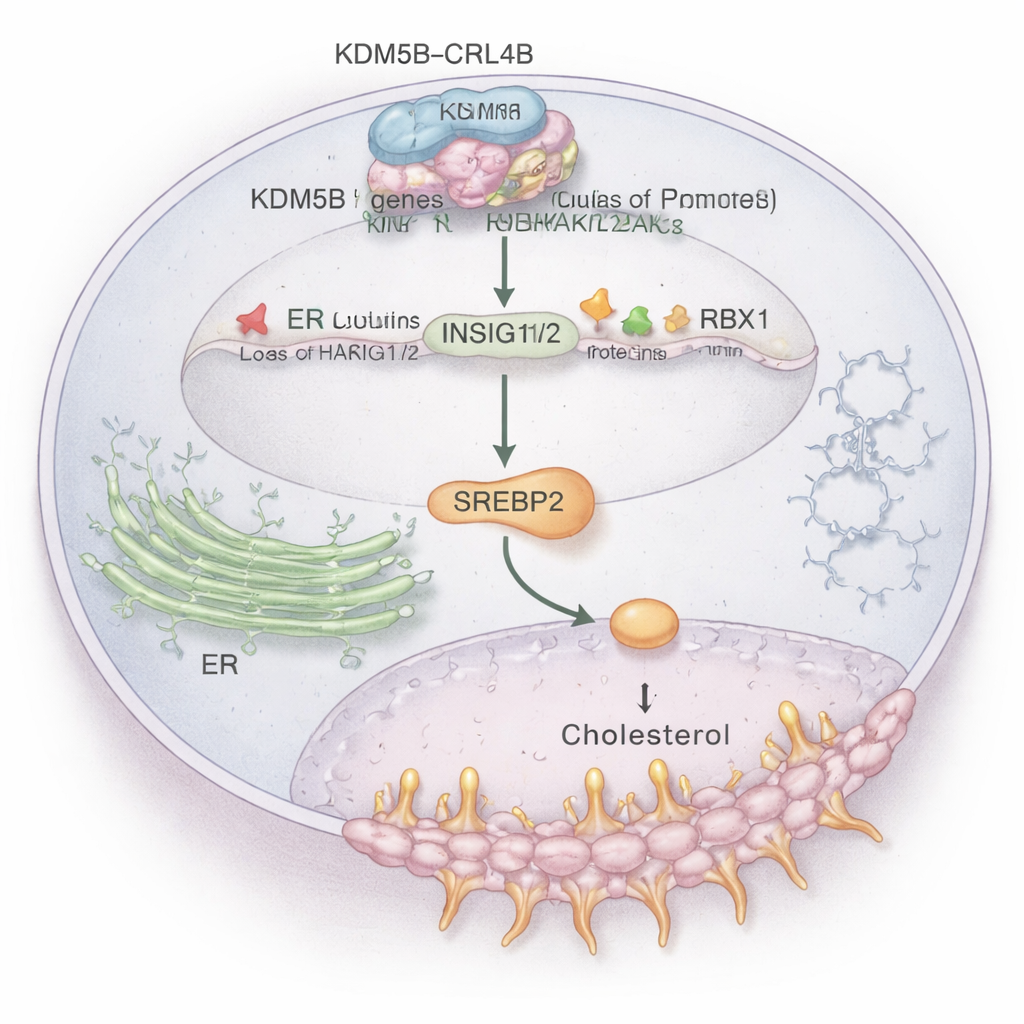
Kolesterol ilaçları ile kanser sinyalleri kesişiyor
Çalışma ayrıca bu yolun 27‑hidroksikolesterol (27‑HC) adlı kolesterol türevi bir sinyalle bağlantısını gösteriyor; 27‑HC’nin ER+ meme kanserini teşvik ettiği zaten biliniyordu. ER+ hücrelere 27‑HC uygulanması KDM5B seviyelerini artırdı ve INSIG1/2’yi daha da baskıladı, hücreleri daha fazla büyüme ve istilaya itti. Önemli olarak, KDM5B veya CRL4B’nin engellenmesi bu saldırgan etkileri hafifletti; bu da 27‑HC’nin kısmen KDM5B–CRL4B eksenine beslenerek etkisini gösterdiğini düşündürüyor. Ayrı olarak, araştırmacılar yaygın kullanılan kolesterol düşürücü bir statin olan simvastatinin meme kanseri hücresi büyümesini yavaşlattığını ve KDM5B inhibitörü ile birleştirildiğinde antitumör etkinin daha güçlü olduğunu gösterdiler. Bu, kolesterol üretimini hedefleyen ilaçları KDM5B’nin gen kontrollerini hedefleyen ilaçlarla eşleştirmenin umut verici bir tedavi stratejisi olabileceğini ima ediyor.
Hastalar ve gelecekteki tedaviler için ne anlama geliyor
Bu çalışma ER+ meme kanseri hücreleri içinde yeni bir olay zincirini açığa çıkarıyor: kolesterolle ilişkili bir sinyal (27‑HC) KDM5B’yi artırır; KDM5B CRL4B kompleksiyle iş birliği yaparak INSIG1 ve INSIG2’yi kapatır; bu SREBP2’yi serbest bırakır, kolesterol üretimini hızlandırır ve tümörlerin büyümesine, istila etmesine ve kök hücre‑benzeri hücreleri korumasına yardımcı olur. KDM5B’nin birkaç başka kanserde de yükselmiş olması ve kötü sağkalımla ilişkilendirilmesi, bu proteinin engellenmesi veya INSIG1/2 frenlerinin geri getirilmesinin tümör büyümesini kontrol altına almak için yeni yollar sunabileceğini gösteriyor. Bu bulguların rutin bakıma dönüşmesi için daha fazla çalışma gerekse de, sonuçlar kanser davranışının kolesterol gibi gündelik moleküllerle ne kadar yakın ilişkili olduğunu ve statinler gibi mevcut ilaçların bir gün epigenetik terapilerle birleştirilerek sonuçları iyileştirebileceğini vurguluyor.
Atıf: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
Anahtar kelimeler: ER-pozitif meme kanseri, kolesterol metabolizması, KDM5B, INSIG1/INSIG2, epigenetik tedavi