Clear Sky Science · tr
Mutant TDP-43, amyotrofik lateral skleroz (ALS) fare kök hücre kaynaklı motor nöron modelinde aksonel transport ve glikolizde bozulmalara yol açıyor
Bu araştırma ALS’liler için neden önemli
Amyotrofik lateral skleroz (ALS), kasları kontrol eden sinir hücrelerini öldürerek kişileri giderek felç eden ölümcül bir hastalıktır. Hastaların çoğunda TDP-43 adlı bir proteinle ilişkili hasar görülür, ancak bilim insanları bu hasarın motor nöronlara nasıl zarar verdiğini hâlâ tam olarak anlayamıyor. Bu çalışma, hastalıkla ilişkili bir TDP-43 çeşidinin neden olduğu en erken sorunlardan bazılarını belirlemek için dikkatle tasarlanmış bir fare kök hücresi modelini kullanıyor ve gelecekteki tedavileri şekillendirebilecek ipuçları sunuyor.
Bir kültürde motor nöronlar oluşturmak
ALS’i kontrollü bir ortamda incelemek için araştırmacılar fare embriyonik kök hücreleriyle başlayıp bunları omurilikten kaslara sinyal gönderen uzun, kablo benzeri motor nöronlara dönüştürdüler. Hücrelere insan TDP-43 geninin tek bir ekstra kopyasını eklediler; ya normal formunda ya da M337V adlı ALS ile ilişkili belirli bir mutasyonu taşıyan biçimde. Hücre içindeki insan proteinini izlemek için floresan bir etikete yer verildi. Kültürde 20. günde hem normal hem de mutant hücreler tipik belirteçleri ifade eden, dallanmış ağlar oluşturmuş ve sinaps benzeri bağlantılar kurmuş olgun motor nöronlara dönüşmüştü; bu durum sinir sisteminde bulunan nöronları yakından andırıyordu. 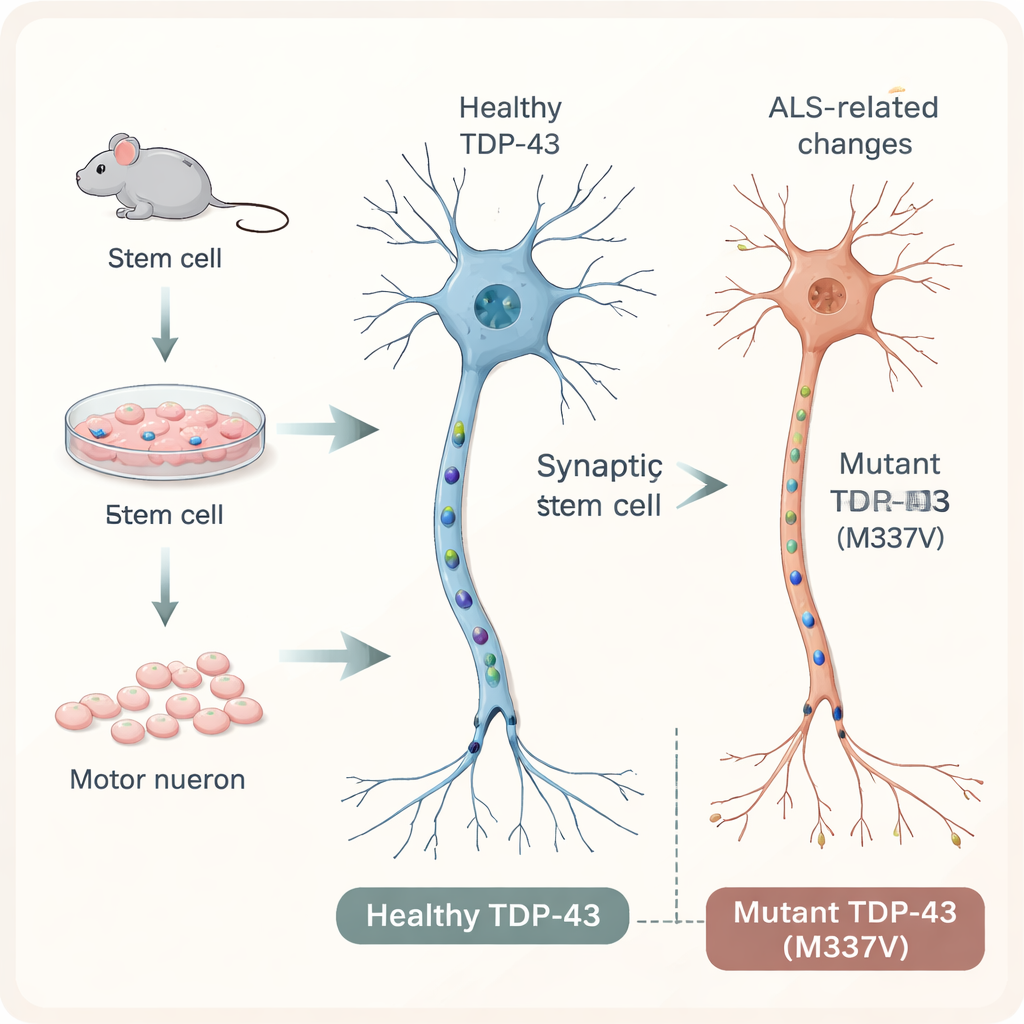
Görünür protein kümeleri olmadan gizli zarar
ALS’li kişilerde TDP-43 genellikle çekirdekteki normal konumundan hücrenin dış bölmesine kayar ve mikroskopta görülen klasik bir patolojik işaret olarak kümeler oluşturur. Şaşırtıcı şekilde, bu kök hücre modelinde mutant TDP-43, normal versiyonla karşılaştırıldığında artmış yanlış konumlanma veya agregasyon göstermedi. Proteinin çoğu olması gerektiği yerde kaldı. Buna rağmen nöronlar belirgin şekilde daha az sağlıklıydi: mutasyonlu proteine sahip kültürlerde daha az hücre gövdesi, daha küçük sinir lifi ağları ve azalmış genel canlılık gözlendi. Bu, ciddi motor nöron hasarının hasta beyinlerinde ve omuriliklerinde görülen dramatik protein kümelerinden önce ya da hatta bunlar olmadan da ortaya çıkabileceğini öne sürer.
Sinir “otoyollarında” trafik sıkışmaları
Motor nöronlar, hayati yükleri aksonları boyunca aşağı yukarı taşıyan hızlı, verimli taşımacılık sistemlerine güveniyor. Aksonları küçük kanallarda izole eden mikroakışkan cihazlar kullanarak ekip canlı hücrelerde sinyal paketleri (endozomlar) ve enerji üreten mitokondrilerin hareketini takip etti. Mutant TDP-43’lü nöronlarda bu yükler çoğunlukla doğru yönlere hareket etmeye devam etti, ancak daha yavaş ilerlediler. Sinyal endozomları hücre gövdesine geri hareket ederken hızlarda azalma gösterdi ve mitokondriler her iki yönde de daha yavaş hareket etti, yerlerinde daha fazla süre durakladılar. Önemli olarak, bu hareketi sağlayan temel mekanizma—iç izler boyunca yürüyen motor proteinler—miktar olarak değişmiş görünmedi; bu da sorunun miktardan ziyade bu mekanizmanın nasıl işlediğinde yattığına işaret ediyor.
Mitokondride değil, şeker yakımında enerji açıkları
Aksonel taşımacılık enerji talep eden bir süreç olduğundan araştırmacılar bu nöronların enerjiyi nasıl ürettiğini ve kullandığını test etti. İki ana kaynağı ölçtüler: oksijen kullanarak yakıt yakan mitokondriyal solunum ve çevresel sıvıda şekeri parçalayan glikoliz. Mitokondriler sayı, şekil ve membran potansiyeli açısından normal görünüyordu ve genel olarak enerji üretme yetenekleri mutant hücrelerde değişmemiş gibi durdu. Buna karşılık, mutant TDP-43’lü nöronlarda bazal glikolizde belirgin bir düşüş görüldü. Önceki çalışmalar aksonlar boyunca yerel glikolizin veziküllerin hızlı taşınması için “yol üstü” yakıt sağlayabileceğini göstermişti. Burada görülen azalmış şeker yakma kapasitesi, dolayısıyla yüklerin yavaşlamasına katkıda bulunarak zaten savunmasız olan motor nöronlar üzerinde ek bir baskı oluşturabilir.
Geleceğin ALS tedavileri için ne anlama geliyor
Bir araya getirildiğinde çalışma, düşük seviyelerdeki ALS ile ilişkili mutant TDP-43’ün bile motor nöronları daha kırılgan hale getirmeye, aksonları boyunca hayati yüklerin hareketini yavaşlatmaya ve şekerden enerji üretme kapasitesini azaltmaya yeterli olduğunu gösteriyor—patologların genellikle aradığı belirgin protein kümeleri olmadan. Uzman olmayanlar için ana mesaj, hücresel “trafik akışı” ve enerji kullanımındaki erken, ince değişikliklerin ALS’de daha sonraki, daha dramatik hasara zemin hazırlayabileceğidir. Bu durum aksonel transport ve özellikle glikoliz gibi hücresel enerji yollarını, geri dönüşü olmayan dejenerasyon başlamadan önce motor nöronları korumayı amaçlayan tedaviler için umut vaat eden hedefler olarak öne çıkarıyor. 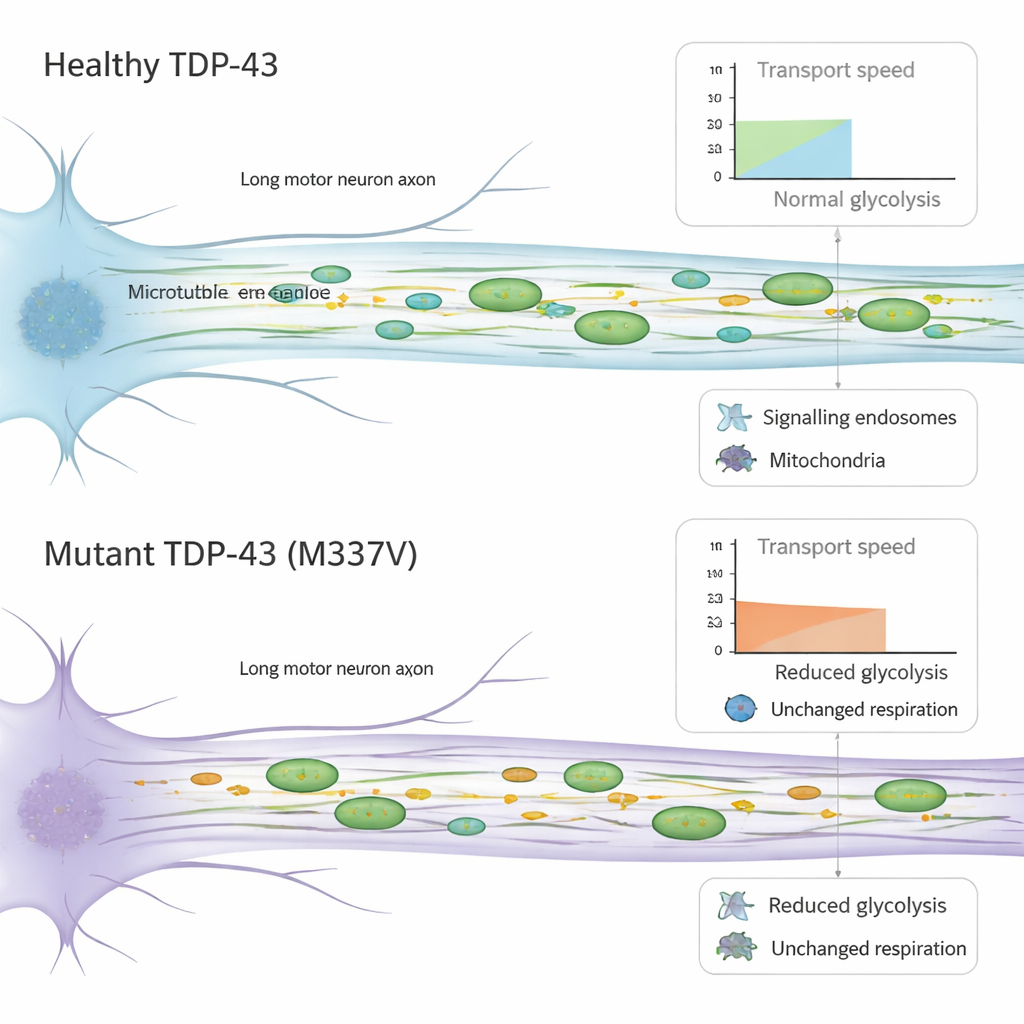
Atıf: Carroll, E., Scaber, J., Pasniceanu, IS. et al. Mutant TDP-43 drives impairments in axonal transport and glycolysis in a mouse stem-cell-derived motor neuron model of amyotrophic lateral sclerosis (ALS). Cell Death Dis 17, 193 (2026). https://doi.org/10.1038/s41419-026-08437-2
Anahtar kelimeler: amyotrofik lateral skleroz, TDP-43, motor nöronlar, aksonel transport, hücresel enerji