Clear Sky Science · tr
Cetuximab’a dirençli kolorektal kanserde terapötik hedef olarak BCL-xL
Kolon kanseri olan kişiler için bunun önemi
Kolorektal (kolon ve rektum) kanser dünya çapında en sık görülen kanserlerden biridir ve ileri evre hastaların birçoğu cetuximab adı verilen hedefe yönelik bir antikor ilacı alır. Bu ilaç başlangıçta tümörleri küçültebilir, ancak çoğu hastada kanser aylar içinde kaçış yolları bulur ve hekimleri sınırlı seçeneklerle bırakır. Bu çalışma şu acil soruyu soruyor: kolon tümörleri cetuximab’a yanıt vermeyi kestiğinde, yeni ilaçların kanser hücrelerini öldürmek için kullanabileceği başka bir zayıf nokta var mı?
Hedefe yönelik bir ilaç işe yaramayı bıraktığında
Cetuximab, kanser hücrelerinin büyümesini destekleyen epidermal büyüme faktörü reseptörü (EGFR) adlı yüzey antenini bloke ederek çalışır. Araştırma ekibi, hassas bir kolorektal kanser hücre hattı (LIM1215) üzerinde altı ay boyunca kademeli olarak artan cetuximab dozlarına maruz bırakarak laboratuvar ortamında direnç modeli oluşturdu. İki bağımsız olarak türetilmiş dirençli hücre popülasyonu, yüksek ilaç düzeylerinde bile büyümeye devam etti; ilaç çıkarıldığında orijinal hücreler kadar sağlıklı ve hızlı çoğalıyor gibi görünüyordu. Önemli olarak, dirençli hücreler hâlâ yüzeylerinde ilacın hedefini taşıyordu ve cetuximab buna hâlâ bağlanabiliyordu; bu da kanserin reseptörü basitçe “gizlemediğini” veya değiştirmediğini gösteriyordu.
Dirençli hücreler büyüme sinyallerini yeniden yönlendiriyor
Hücrelerin cetuximab’ı nasıl atladığını anlamak için araştırmacılar hücre içindeki kilit büyüme yollarını inceledi. Ebeveyn hücrelerde cetuximab genellikle hücre bölünmesinin önemli motoru olan MAPK yolunu baskılıyordu. Dirençli hücrelerde, EGFR bloke edildiğinde bile MAPK aktivitesi yüksek kaldı; bu, büyüme sinyalinin orijinal reseptörden ayrıldığını gösteriyordu. Hücre RNA’sının dizilenmesi, dirençli hücrelerin alt popülasyonlarında başka bir RAS geni olan HRAS’ta yeni aktivasyon mutasyonları ortaya koydu, ancak KRAS, NRAS veya BRAF gibi diğer yaygın adaylarda değil. Bu yeniden yönlenmiş sinyalleşmeyi RAS’ın aşağısında etki eden bir MEK inhibitörü ile kapatmaya yönelik girişimler büyümeyi yalnızca sınırlı ölçüde azalttı. Bu, her yeni mutasyonu kovalamaktansa farklı dirençli klonlar arasında paylaşılan hücresel yaşam-yaşamayla ilgili mekanizmalara saldırmanın daha etkili olabileceğini vurguladı. 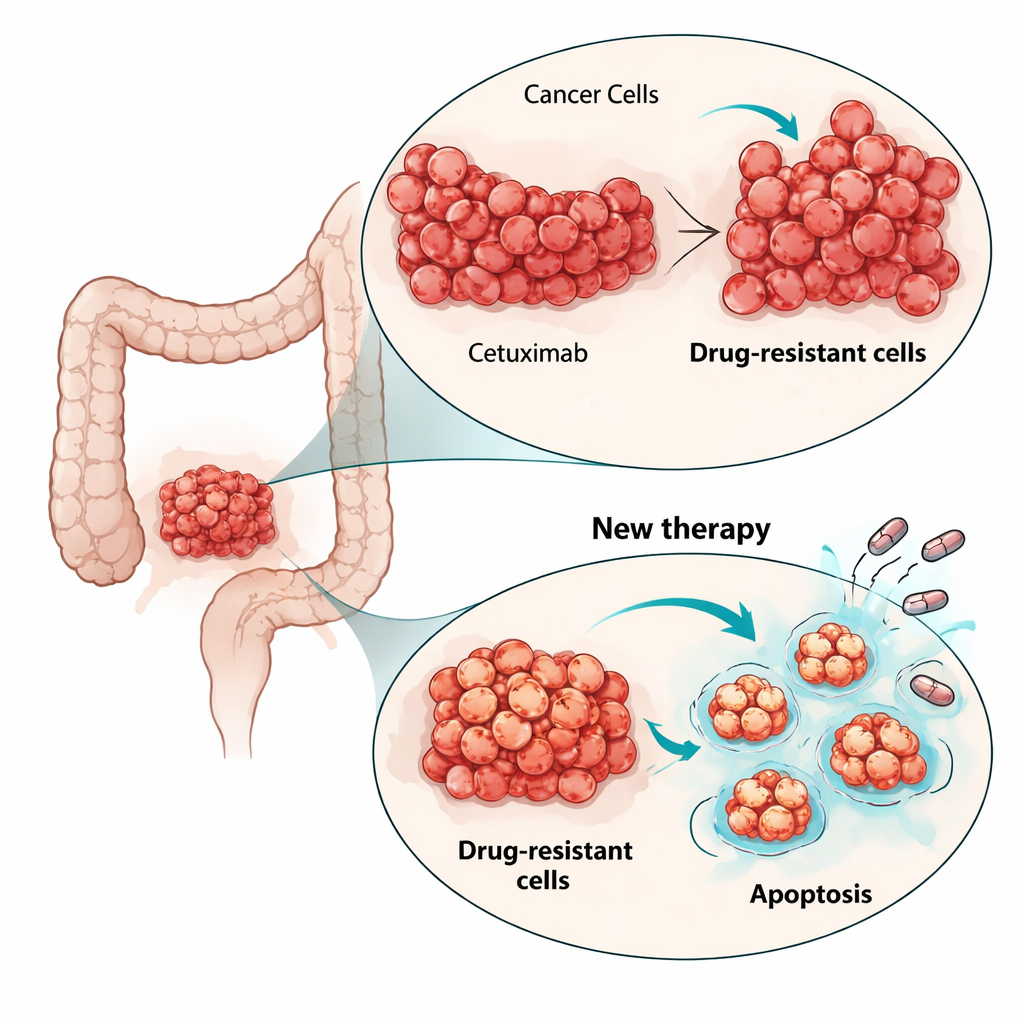
Kansere yaşam destek sisteminden vurmak
Bilim insanları dikkatlerini, kanserlerin sıklıkla baskıladığı yerleşik hücre intihar programı apoptoza çevirdiler. Gen ekspresyonu analizi, apoptozla ilgili yolların dirençli hücrelerde değiştiğini gösterdi. Özellikle, anti-ölüm proteini BCL-xL bir dirençli popülasyonda daha yüksek, diğerinde ise ılımlı derecede artmıştı; ayrıca başka bir hayatta kalma proteini olan MCL-1 de mevcuttu. Ekip, bu hayatta kalma proteinlerini bloke edip ölüm mekanizmasını serbest bırakmak üzere tasarlanmış BH3 benzerleri adlı küçük moleküllü ilaçları test etti. İki boyutlu hücre kültürlerinde hem ebeveyn hem de iki dirençli hücre hattı BCL-xL veya MCL-1’i bloke eden ilaçlara duyarlıydı; ancak çarpıcı biçimde, daha düşük dozlar cetuximab’a dirençli hücreleri daha etkili öldürdü. Proteazom inhibitörü bortezomib’in düşük bir dozu eklendiğinde—bu, pro-ölüm sinyallerinin birikmesine yardımcı olur—özellikle MCL-1 blokeri ile birlikte kullanıldığında öldürme daha da arttı.
Düz plaklardan 3B mini-tümörlere ve hasta dokularına
Düz hücre katmanlarının vücuttaki tümörleri tam olarak taklit edemeyeceği için ekip, hücreleri jel içinde gömülü üç boyutlu sferoidler olarak büyüttü; bu, gerçek tümörlerin mimarisi ve ilacın nüfuz etme zorluklarını daha iyi yansıtır. Yine, BCL-xL veya MCL-1’in bloke edilmesi sferoid canlılığını azalttı ve bu ilaçların bortezomib ile kombinasyonu metabolik aktivitede dramatik düşüşlere ve belirgin hücre ölümü belirtilerine neden oldu. Bu kırılganlığın daha gerçekçi insan tümör materyalinde de mevcut olup olmadığını test etmek için hasta tümörlerinden türetilen ve farelerde büyütülen cetuximab’a dirençli kolorektal kanserlerin ince dilimlerini kullandılar (patient-derived xenografts). Bu modellerin hepsi orijinal LIM1215 hücreleri gibi KRAS vahşi tipti ancak klinikte görülen genetik çeşitliliği yansıtarak BRAF ve TP53 dahil olmak üzere farklı ek mutasyonlar taşıyordu. 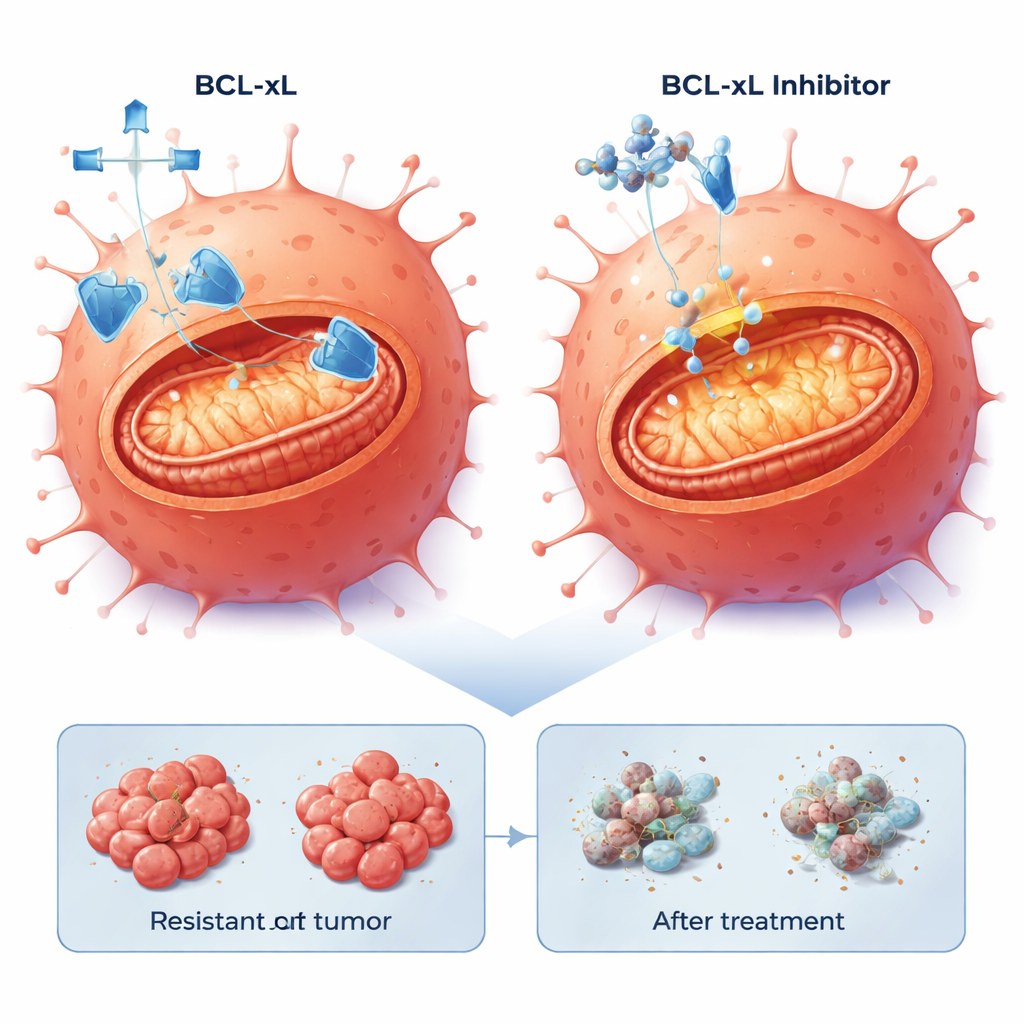
Farklı dirençli tümörlerde BCL-xL’i hedeflemek etkili
Bu hasta kaynaklı tümör dilimlerinde, BCL-xL inhibitörü ile düşük doz bortezomib kombinasyonu, agresif BRAF mutasyonlarına sahip modeller dahil olmak üzere dört farklı modelde tümör hücrelerinin %20–40’ında tutarlı ve güçlü hücre ölümü tetikledi. Buna karşılık, bortezomib ile MCL-1 bloke edilmesi sadece bazı tümörlerde güçlü etkiler gösterdi. Önemli olarak, dirençli hücrelerin apoptoz geçirme yeteneği korundu: BCL-xL güvenlik ağı kaldırıldığında, tümörün cetuximab’tan kaçmak için izlediği spesifik genetik yola bakılmaksızın içsel ölüm programı hâlâ aktive edilebildi.
Hastalar için bunun anlamı
Cetuximab’a yanıt vermeyi kesen kolorektal kanseri olan kişiler için bu çalışma temkinli bir iyimserlik sunuyor. Çalışma, tümörler EGFR hedefli tedaviye direnç geliştirdikten sonra bile birçok kanser hücresinin önemli bir hayatta kalma proteini olan BCL-xL engellendiğinde ölmeye hazır kaldığını öne sürüyor. BCL-xL inhibitörlerinin özellikle kan pulcukları üzerinde yan etkileri olabilir, ancak çalışma toksisiteyi sınırlayabilecek kombinasyon ve doz-optimizasyon stratejilerine işaret ediyor ve zor tedavi edilen tümörlerin ortak bir Achilles topuğunu kullanmayı öneriyor. Gelecekte, BCL-xL’i etkisiz hale getiren ilaçlar, tümörün değişen mutasyon manzarasına daha az bağımlı olarak cetuximab’a dirençli kolorektal kanser için yeni ikinci basamak tedavilerin omurgasını oluşturabilir.
Atıf: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Anahtar kelimeler: kolorektal kanser, ilaç direnci, cetuximab, BCL-xL inhibitasyonu, apoptoz