Clear Sky Science · tr
LAP2α, replikasyon stresini hafifleterek meme tümörojenezini yönlendirir
Meme kanseri açısından neden önemli
Meme tümörleri, kanser hücrelerinin DNA’sını kopyalarken sürekli strese rağmen hayatta kalmanın yollarını bulması sayesinde kısmen büyür. Bu çalışma, LAP2α adı verilen daha az bilinen bir proteinin, meme kanseri hücrelerinin replikasyon sırasında DNA’sını nasıl koruduğunu açığa çıkarıyor; bu da tümör büyümesini teşvik ediyor ve kanserleri tedaviye daha dirençli hale getiriyor. Bu gizli destek mekanizmasını anlamak, tümörleri zayıflatmanın ve mevcut ilaçların etkisini artırmanın yeni yollarını önermektedir.
Tümör hücresi çekirdeğinde gizli bir yardımcı
Her hücre bölünmesi sırasında DNA’sını doğru şekilde kopyalamak zorundadır. Kanser hücrelerinde bu süreç özellikle zorlanır: büyüme sinyalleri sürekli “açık” durumdadır ve replikasyon mekanizması sınırlarına kadar zorlanır. Bu baskı, replikasyon stresi olarak bilinir ve hızla kaplanıp stabilize edilmesi gereken tek iplikli DNA bölgeleri bırakır; bu görevi replikasyon proteini A (RPA) adlı protein kompleksi üstlenir. Yazarlar daha önce çekirdeğin iç iskeletiyle ilişkilendirilen LAP2α’nın RPA’ya bağlanabildiğini ve RPA’nın hasarlı DNA’ya ulaşmasına yardımcı olabildiğini bulmuşlardı. Bu çalışmada, LAP2α–RPA ortaklığının gerçekten meme tümör gelişimini destekleyip desteklemediğini ve tümörlerin tedaviye yanıtını nasıl etkilediğini sordular.
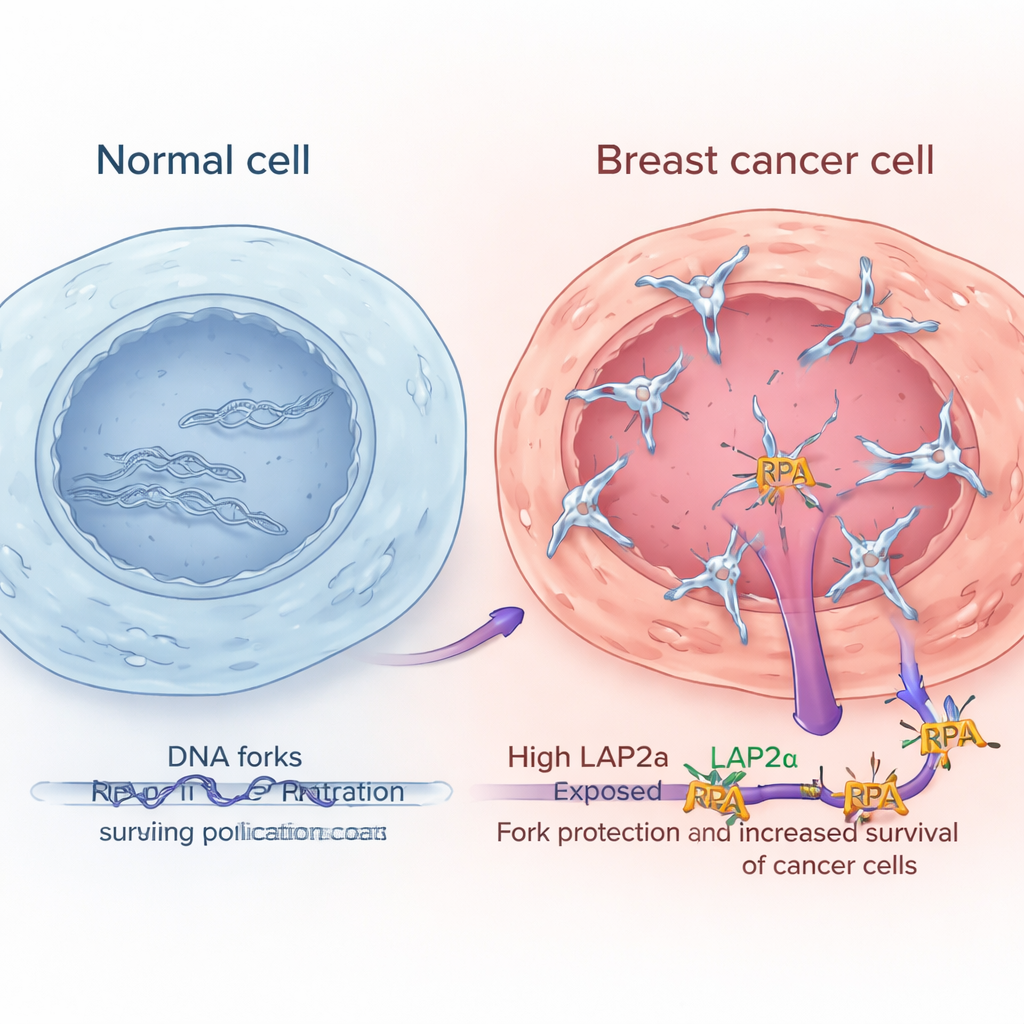
Yüksek LAP2α düzeyleri daha agresif meme tümörlerini işaret ediyor
Büyük halka açık gen ifadesi veri setlerini analiz ederek ve tümör örneklerini mikroskop altında inceleyerek araştırmacılar, LAP2α’nın çevre normal meme dokusuna göre meme kanseri dokusunda tutarlı şekilde daha yüksek olduğunu gösterdiler. Düzeyleri tümör derecesiyle birlikte artıyordu; yani daha anormal ve agresif kanserlerde genellikle daha fazla LAP2α bulunuyordu. Bu desen, hormon reseptör–pozitif, HER2-zenginleşmiş ve üçlü negatif tümörler de dahil olmak üzere birden çok ana meme kanseri alt tipinde görüldü. Hastalar açısından önemli olarak, tümörlerinde yüksek LAP2α olanların sağkalımının daha kötü olma eğiliminde olduğu bulundu. Buna karşılık, RPA’nın çekirdek bileşenleri benzer değişiklikler veya belirgin sonuç ilişkileri göstermedi; bu da kanser hücrelerinin replikasyon stresine karşı daha iyi başa çıkmasına yardımcı olanın, yalnızca daha fazla RPA değil, güçlendirilmiş LAP2α işlevi olduğunu düşündürüyor.
LAP2α kapatıldığında tümörler yavaşlıyor ve zayıf noktalar ortaya çıkıyor
Korelasyonların ötesine geçmek için ekip, LAP2α’nın seçici olarak çıkarılabildiği meme kanseri fare modelleri kullandı. Meme tümörleri oluştuktan sonra genetik olarak LAP2α silindiğinde tümörlerin daha yavaş büyüdüğü ve hayvanların sağkalımının uzadığı görüldü. LAP2α eksikliği olan tümör hücreleri daha az bölündü ve DNA hasarının daha fazla belirtisini taşıdı; bu, artmış DNA kırık belirteçleri boyanması ve DNA üzerindeki RPA kaplamasının azalmasıyla gösterildi. Bu LAP2α eksik tümör hücreleri yeni farelere nakledildiğinde yine daha küçük tümörler oluşturdular ve platin ilacı sisplatin ile bir PARP inhibitörü dahil olmak üzere DNA’ya zarar veren kemoterapilere karşı artmış duyarlılık sergilediler. İnsan meme kanseri hücre hatlarındaki benzer deneyler, LAP2α’yı azaltmanın hücreleri çeşitli genotoksik ilaçlara karşı daha savunmasız hale getirdiğini doğruladı; normal LAP2α’nın geri verilmesi—ancak RPA’ya bağlanamayan bir mutant form değil—hem DNA korumasını hem de ilaç direncini geri kazandırdı.
LAP2α kırılgan DNA ipliklerini nasıl koruyor
Mekanizmayı çözmek için araştırmacılar DNA bağlanma adımlarını test tüpü deneylerinde yeniden oluşturdular. Saflaştırılmış RPA, tek iplikli DNA ve ya normal LAP2α ya da RPA ile etkileşemeyen bir varyant karıştırdılar. LAP2α’nın RPA’nın tek iplikli DNA’yı kaplama verimliliğini doğrudan artırdığını ve RPA’nın bu kırılgan bölgeleri gerip stabilize etmesine yardımcı olduğunu buldular; LAP2α yükleme yardımcısı veya şaperon gibi davranıyordu. DNA bulunduğunda RPA’nın genellikle LAP2α’dan ayrılıp tek ipliğe tam olarak bağlanmaya yöneldiği görüldü; bu da LAP2α’nın nihai koruyucu örtünün bir parçası değil, RPA’yı DNA’ya devreden bir el olduğunu gösteriyor. İşlevsel bir LAP2α–RPA etkileşimi olmadığında daha fazla replikasyon çatallanması çöktü, DNA kırıkları birikti ve kanser hücreleri özellikle kemoterapi ile ilave hasar verildiğinde ölme olasılığı daha yüksek oldu.
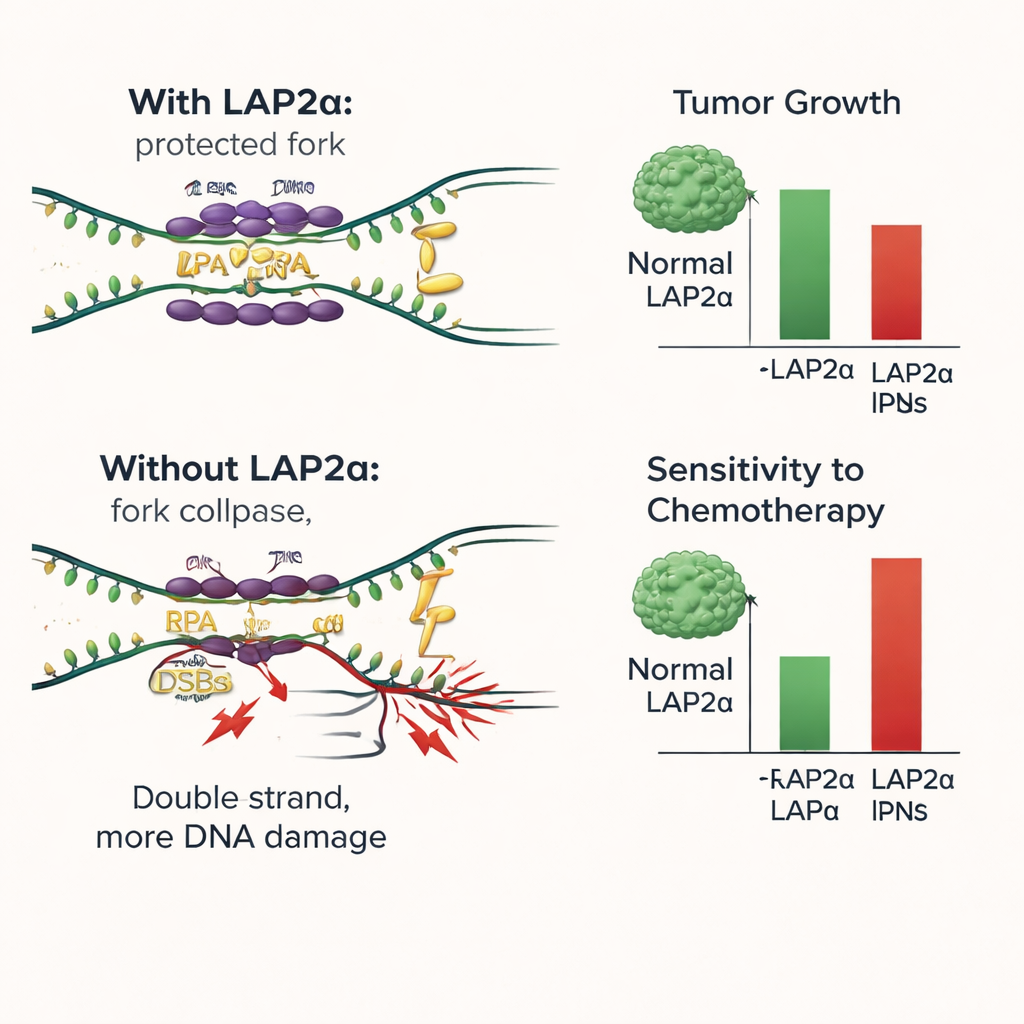
Gelecekteki meme kanseri tedavisi için bunun anlamı
Sade bir ifadeyle, bu çalışma LAP2α’nın meme kanseri hücrelerinin DNA’yı kopyalamanın yükünü taşırken hayatta kalmasına yardımcı olan sahne arkası bir yardımcı olduğunu gösteriyor. Zayıf DNA üzerine RPA’yı verimli şekilde yükleyerek LAP2α hasarı azaltır ve tümör büyümesini destekler. LAP2α’yı kaldırmak veya devre dışı bırakmak dengeyi değiştirir: DNA hasarı birikir, hücreler bölünmeyi durdurur ve DNA’yı hedef alan konvansiyonel ilaçlar daha etkili hale gelir. Bu bulgular LAP2α’nın kötü prognoz işareti ve yeni bir terapötik hedef olarak kullanılabileceğini öne sürüyor. LAP2α’yı veya onun RPA üzerindeki tutuşunu engelleyen ilaçlar, bu stres tamponlama sistemine güçlü şekilde bağımlı tümörlerde platin ajanlar ve PARP inhibitörleri gibi mevcut tedavilerin etkinliğini artırabilir.
Atıf: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Anahtar kelimeler: meme kanseri, DNA replikasyon stresi, LAP2 alfa, replikasyon proteini A, kemoterapi duyarlılığı