Clear Sky Science · tr
Glikerofosfolipit biyosentezinin hedeflenmesi, Ewing sarkomunda SLFN11 kaybının yol açtığı kemorezistansı aşar
Bu araştırma çocukluk çağı kanseri için neden önemli
Ewing sarkomu nadir ama agresif bir kanserdir ve çoğunlukla çocukları ve ergenleri etkiler. Birçok hasta başlangıçta kemoterapiye iyi yanıt verir, ancak kanser nüks ettiğinde mevcut tedaviler sıklıkla başarısız olur. Bu çalışma önemli bir soruyu gündeme getiriyor: Ewing sarkomu hücreleri kemoterapiye direnç kazandığında, onların hayatta kalmasına yardımcı olan içsel değişiklikler nelerdir — ve bu değişiklikler doktorların hedefleyebileceği yeni zayıf noktalara dönüştürülebilir mi?
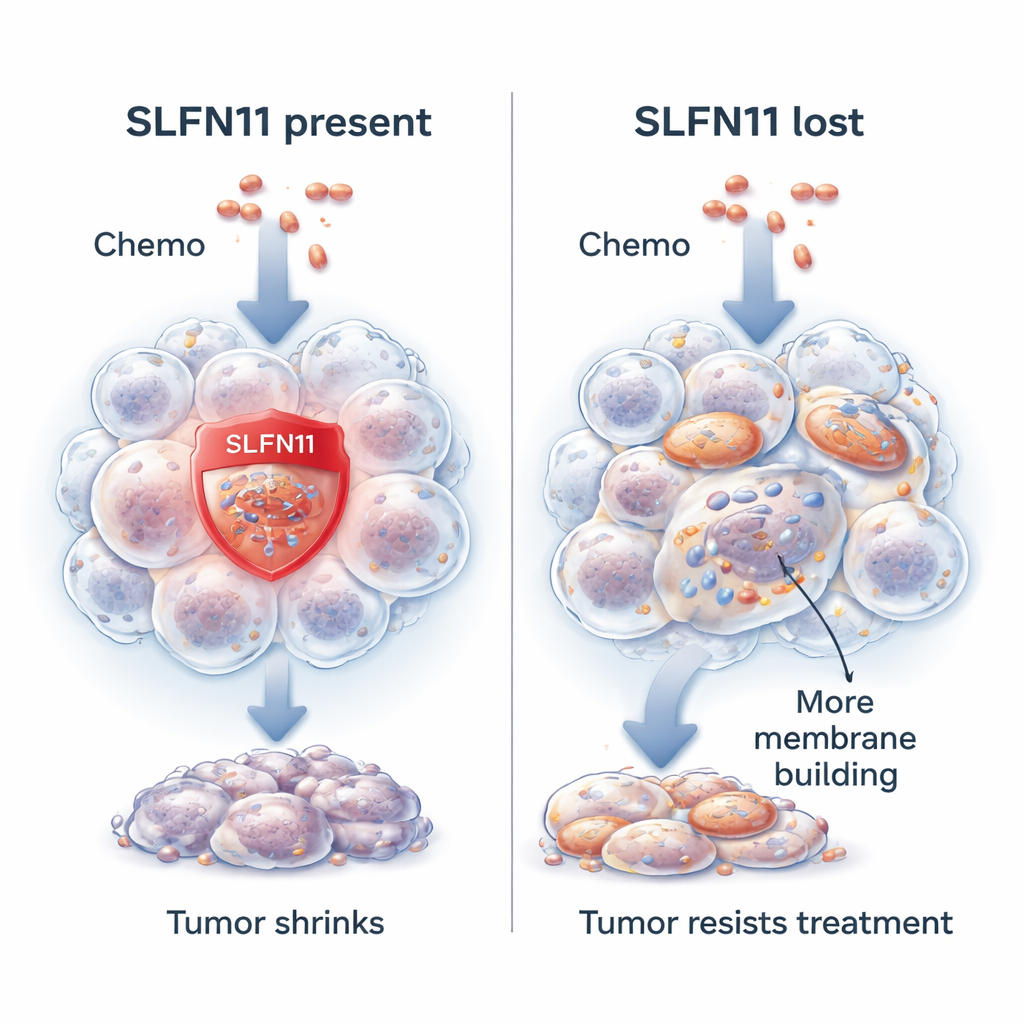
Kanser hücrelerini öldürmeyi kolaylaştıran bir gen
Araştırmacılar SLFN11 adlı bir gene odaklanıyor. Birçok Ewing sarkomu tümöründe SLFN11 yüksek düzeyde aktiftir ve DNA’yı hasara uğratan ilaçlara karşı kanser hücrelerini çok daha hassas hale getirir. Bu ilaçlar verildiğinde, SLFN11 DNA tamirini baskılamaya yardımcı olur ve kanser hücresini ölüme doğru iter. Tümörlerinde daha yüksek SLFN11 seviyeleri bulunan hastalar genellikle daha uzun yaşar ve tedaviye daha iyi yanıt verir. Ancak her on tümörden yaklaşık biri başlangıçta az veya hiç SLFN11 içermez ya da tedavi sürecinde bunu kaybeder. Bu olduğunda aynı kemoterapi çok daha az etkili olur, buna karşın kanser hücreleri büyümeye devam edebilir.
Kanser hücreleri yakıt ve yağ kullanımını nasıl yeniden düzenliyor
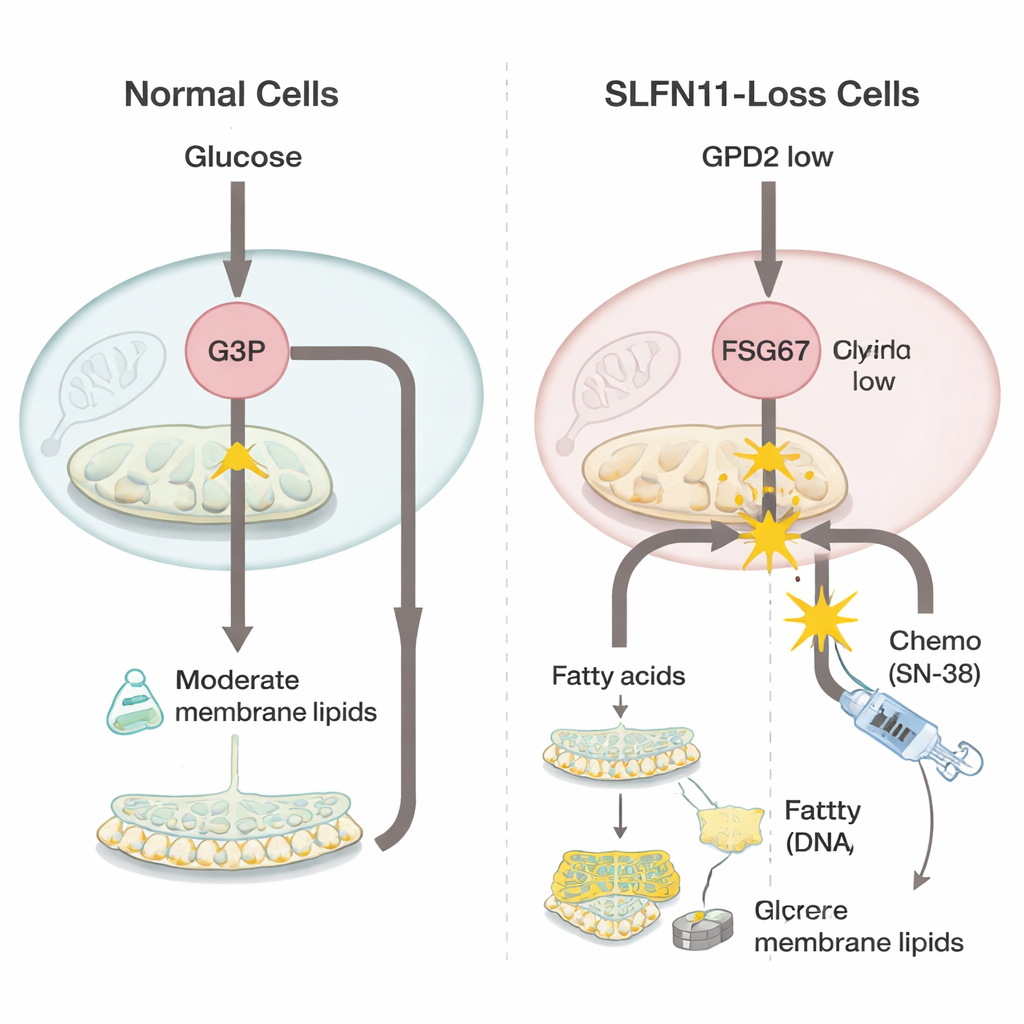
SLFN11 kaybedildiğinde nelerin değiştiğini anlamak için ekip, bu gene sahip olan ve olmayan Ewing sarkomu hücrelerini binlerce gen ve küçük molekülü aynı anda ölçen güçlü “omik” araçlarla karşılaştırdı. SLFN11 eksik hücrelerin mitokondride GPD2 adlı bir enzimi azaltarak çalıştırdığını keşfettiler; bu enzim normalde gliserol‑3‑fosfat adlı bir molekülü enerji üretiminin bir parçası olarak yakmaya yardımcı olur. GPD2 azaldığında gliserol‑3‑fosfat birikir. Bu fazla yapı taşı boşa gitmek yerine hücre membranlarını oluşturan ve gliserofosfolipitler olarak bilinen daha fazla yağlı molekülün yapımına yönlendirilir. Hücreler ayrıca daha esnek, doymamış yağlar yapma belirtileri gösterdi; bu tür yağlar hızla büyüyen tümörlerin strese uyum sağlamasına yardımcı olabilir.
Bir hayatta kalma hilesini zayıf noktaya çevirme
SLFN11 eksik hücreler membran üretimine daha fazla dayandığından, bilim insanları bu süreci engellemenin kemoterapi duyarlılığını geri getirip getirmeyeceğini test ettiler. Gliserofosfolipit üretiminde kilit bir adımı engelleyen FSG67 adlı bir bileşik kullandılar. Tek başına, standart DNA hasar verici ilaç SN‑38 SLFN11 eksik hücrelerde çok daha az etkili hale gelmişti; bu, klinikteki direnç sorununu yansıtıyordu. Ancak SN‑38 FSG67 ile birlikte verildiğinde, önceden dirençli hücreler çok daha ağır darbe aldı ve iki ilaç bireysel etkilerinden beklenenden daha iyi bir iş birliği içinde çalıştı. Buna karşılık, hâlâ SLFN11’e sahip ve SN‑38’e zaten oldukça hassas olan hücrelerde FSG67 eklemenin çok az ek faydası oldu ve hatta bazen hafifçe ters etki gösterebilirdi. Bu desen, yağ ve membran üretimine olan yeni bağımlılığın dirençli, SLFN11 düşük duruma özgü olduğunu düşündürüyor.
Zor tedavi edilen tümörlerin potansiyel noninvaziv işareti
Araştırmacılar sonra bu metabolik yeniden düzenlemenin yalnızca kültürdeki hücrelerde değil, gerçek tümörlerde de tespit edilip edilemeyeceğini sordular. SLFN11’li veya SLFN11’siz Ewing sarkomu tümörlerini farelerde yetiştirdiler ve tümör özütlerinin kimyasal bileşimini incelemek için nükleer manyetik rezonans (NMR) kullandılar. SLFN11 eksik tümörler membran dönüşümü ile ilişkili iki kolin içeren molekülün daha yüksek oranını gösterdi: fosfocholin ve gliserofosfocholin. Yüksek bir fosfocholin/gliserofosfocholin oranı diğer kanserlerde daha agresif davranış ve tedaviye daha zayıf yanıt ile ilişkilendirilmiştir. Kolin sinyalleri gelişmiş görüntüleme teknikleriyle ölçülebildiği için, bu tür bir değişim bir gün bu dirençli, membran‑yapım modunu benimsemiş Ewing sarkomu tümörlerini işaret eden noninvaziv bir belirteç olarak hizmet edebilir.
Gelecekteki tedaviler için bunun anlamı ne olabilir
Genel olarak çalışma, Ewing sarkomu hücreleri SLFN11’i kaybedip DNA’yı hasara uğratan kemoterapiye daha az duyarlı hale geldiğinde, membran yağları yapımına yönelerek metabolizmalarını yeniden düzenlediklerini gösteriyor. Bu değişim sadece hücrelerin hayatta kalmasına yardımcı olmakla kalmıyor; aynı zamanda yeni bir Achilles topuğu yaratıyor. FSG67 gibi bir ilaçla gliserofosfolipit üretimini engellemek, bu dirençli hücrelerde kemoterapinin öldürücü gücünü kısmen geri getirebilir. FSG67’in kendisi henüz klinikte bir ilaç olmasa da, bu çalışma doktorların bir gün hastaların tümörlerini SLFN11 durumu ve metabolik özelliklerine göre eşleştirip DNA’yı hasara uğratan tedavileri yağ ve membran sentezini hedef alan engelleyicilerle kombinleyerek direnci aşabilecekleri bir stratejiye işaret ediyor.
Atıf: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Anahtar kelimeler: Ewing sarkomu, kemorezistans, SLFN11, kanser metabolizması, yağ biyosentezi