Clear Sky Science · tr
Efferositozda bağışık hücrelerin modülasyonu ve metabolik yeniden programlama
Vücudumuzun Ölen Hücreleri Sessizce Nasıl Temizlediği
Her gün milyarlarca hücre yaşamlarının sonuna gelir. Buna rağmen bu mikroskopik yenilenmeyi hissetmeyiz ve artık parçalanmış hücrelerden hasta olmayız. Bu sessiz temizlik, ölen hücreleri tanıyıp yutan ve zararlı iltihabı önleyen bağışık ve doku hücreleri tarafından yürütülür. Derleme, efferositoz adı verilen bu temizleme sürecinin sadece dokuları düzenli tutmakla kalmadığını, aynı zamanda temizlik yapan hücrelerin metabolizmasını yeniden şekillendirerek bağışıklık sistemimizin yatışıp yatışmayacağını, enfeksiyonla mı mücadele edeceğini ya da işler ters giderse hastalığa mı katkıda bulunacağını açıkladığını özetliyor.
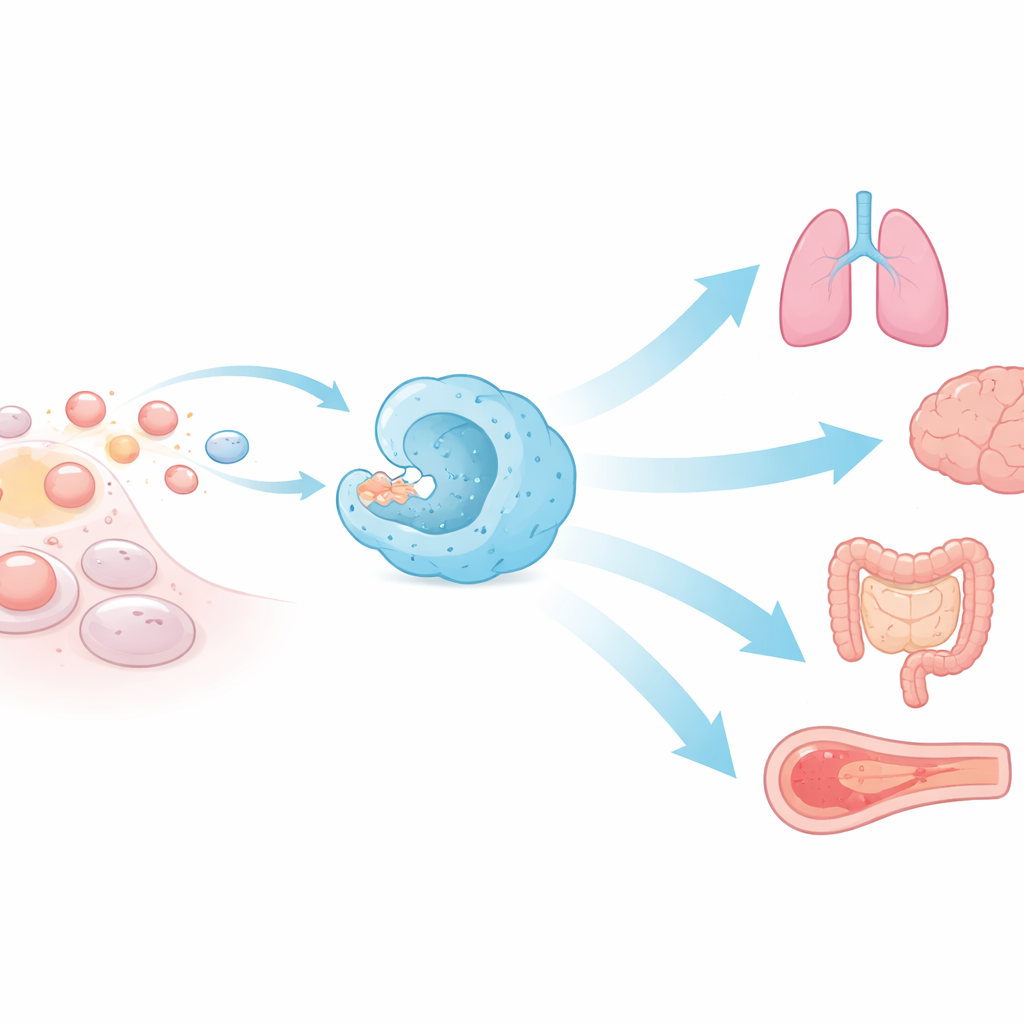
Vücudun Sessiz Çöp Toplayıcıları
Efferositoz, programlı hücre ölümü olan apoptozla ölen hücrelerin yutulması ve yok edilmesi için verilen addır. Makrofajlar ve dendritik hücreler gibi özelleşmiş bağışık hücreler bu işin çoğunu yapar, ancak bağırsak, akciğer, göz ve testislerdeki epitel hücreleri gibi birçok bağışık olmayan hücre de devreye girebilir. Ölen hücreler yakındaki temizleyicileri çeken “beni bul” kimyasal işaretleri salar, yüzeylerinde “beni ye” bayrakları gösterirken “beni yeme” sinyallerini kapatır. Tanındıktan sonra bir zar kesesine sarılır, içeri çekilir ve enzim dolu bölmelerde parçalanır. Bu hızlı, çok aşamalı koreografi apoptozla ölen hücrelerin mikroskopta nadiren görülmesinin, günlük büyük hücre kaybına rağmen nedenini açıklar.
Organları Koruyan Temizlik
Etkili efferositoz birçok organın yapı ve işlevini korur. Gözde, retinadaki hücrelerin ölen fotoreseptör parçalarını temizleyememesi görme kaybına yol açar. Testislerde, ölen germ hücrelerinin kötü temizlenmesi kısırlığa neden olabilir. Gebelik sırasında plasenta hücrelerinin efferositozu, inflamatuar molekülleri baskılayarak ve yatıştırıcı olanları artırarak anne toleransını teşvik eder. Beyinde, mikroglia fazla nöronları budar ve sağlıklı bağlantıların oluşmasına destek olurken, bağırsakta Paneth hücreleri ve diğer fagositler kronik bağırsak iltihabını önlemek için ölen hücreleri temizler. Akciğerlerde, hava yolları makrofajları sürekli olarak ölü hücreleri uzaklaştırır; böylece astım, kronik obstrüktif akciğer hastalığı veya şiddetli viral hasar gibi tehlike sinyallerini tetikleyebilecek durumların önüne geçilir.
Enfeksiyonlar Temizliği Çifte Kenarlı Bir Kılıç Haline Getirdiğinde
Enfeksiyonlar sırasında efferositoz daha karmaşık hale gelir. Patajenler sıklıkla hücre ölümünü tetikler ve enfekte cesetlerin yutulması konak savunmasını zayıflatabilir veya güçlendirebilir. Bazı virüsler ve bakteriler, efferositozun anti-inflamatuar yönünü bağışıklıktan saklanmak veya yayılmak için suiistimal ederek yutulmuş vezikülleri “Truva atı” olarak kullanır. Diğer durumlarda, enfekte ölü hücrelerin yutulması mikrobiyal parçacıkları makrofajlara ve dendritik hücrelere teslim eder; bunlar da bu parçaları T hücrelerine sunarak koruyucu bağışık yanıtları harekete geçirir. Mikrop ve dokuya bağlı olarak efferositoz, T yardımcı hücreleri farklı bağışıklık profillerine yönlendirebilir; bu, ya bakteriyel temizliği destekler ya da mikrobiyal bileşenlerle birlikte sunulan öz moleküller nedeniyle vücudun kendi dokularına saldıran otoimmün T hücrelerinin ortaya çıkmasına yol açabilir.
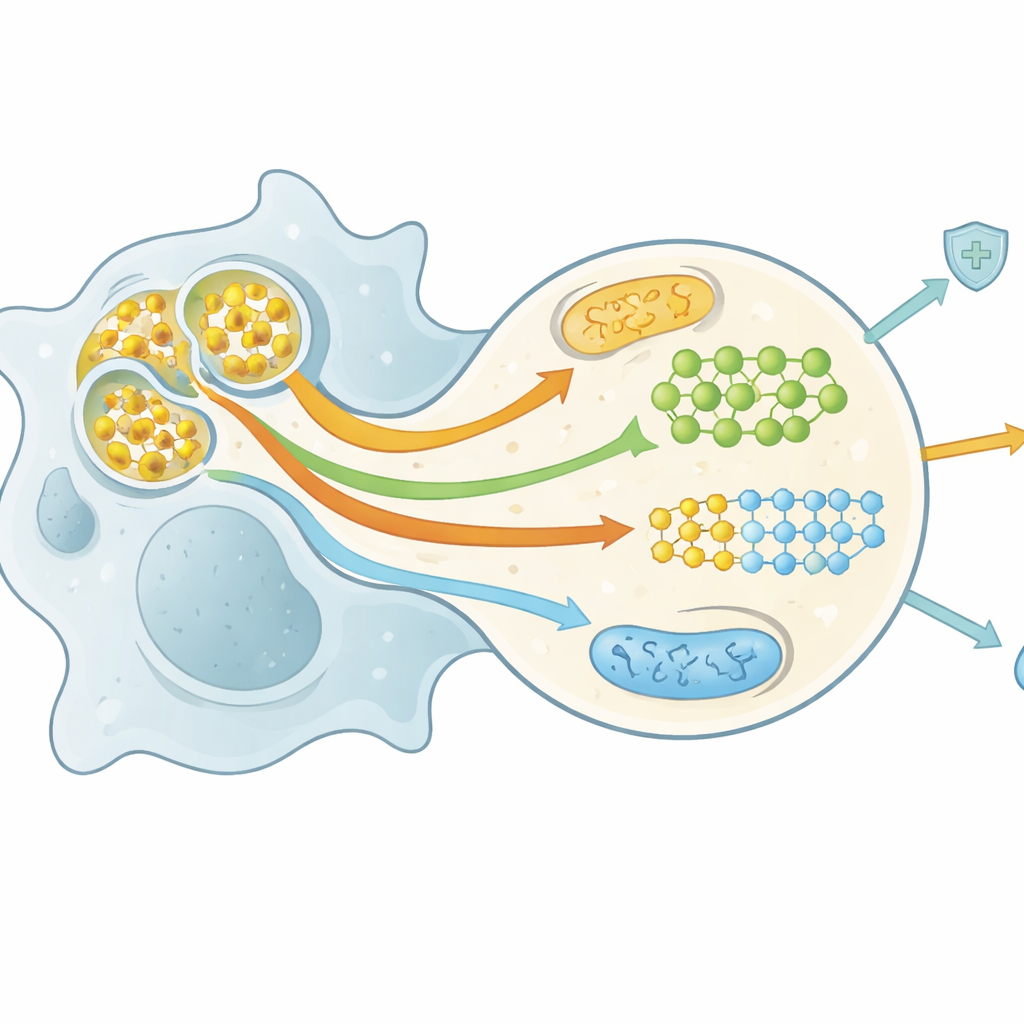
Düşenlerden Gelen Yakıt: Metabolizma Nasıl Yeniden Programlanır
Tam bir hücreyi parçalamak metabolik olarak yük gerektirir, ancak aynı zamanda temizleyiciyi lipitler, şekerler, amino asitler ve nükleotidler gibi besinlerle doldurur. Yazarlar, bu besin akışının makrofajlar ve dendritik hücrelerin metabolizmasını nasıl yeniden programladığını izleyen, bazen efferotabilizma olarak adlandırılan büyüyen bir alanı tanımlıyor. Ölen hücrelerden gelen lipitler, kolesterol ihracını artıran, mitokondriyal yağ yakımını destekleyen ve anti-inflamatuar, doku onarıcı bir durumu teşvik eden nükleer reseptörleri aktive eder. Arjinin, metiyonin ve triptofan gibi amino asitler, tekrar tekrar yutma turları için enerji sağlayan ve çözümleyici sinyalleri tetikleyen moleküllere geri dönüştürülür. Kısa süreli glikoz yıkımı ve ilgili yollar enerji sağlar, redoks dengesini korur ve sürekli temizlik için reseptörleri ve zarları doğru halde tutmaya yardım eder. Bu iç içe geçmiş metabolik değişimler, efferositik hücrelerin toleranslı kalıp kalmayacağını, onarım moduna mı geçeceğini ya da güçlü antimikrobiyal aktiviteyi sürdürüp sürdürmeyeceğini belirler.
Açık Sorular ve Gelecek Tedavi Yolları
Derleme, tüm efferositlerin veya hücre yiyicilerin aynı davranmadığını vurguluyor. Profesyonel bağışık hücreler ile doku hücreleri farklı metabolik programlara güvenebilir ve nekroz veya ferroptoz gibi farklı hücre ölümü biçimleri muhtemelen farklı metabolik ve bağışık izler bırakır. Ana bilinmeyenler arasında, aynı ölen hücre içindeki hem öz hem de mikrobiyal bileşenlerden gelen karışık sinyallerin enerji yollarını ve uzun vadeli bağışıklığı nasıl şekillendirdiği yer alır. Temizlik, metabolizma ve bağışık kaderi arasındaki bu bağlantıları haritalayarak araştırmacılar, efferositozu nazikçe yönlendirecek terapiler tasarlamayı umuyor: kronik inflamasyonu çözmek ve yara onarımını desteklemek için onu artırmak ya da antimikrobiyal gücü korurken otoimmüniteye kaymayı önleyecek şekilde ayarlamak. Özetle, vücudun kendi hücresel artıklarını nasıl 'yediğini' anlamak, inflamasyon, enfeksiyon ve toleransı sağlıklı dengede tutmanın yeni yollarını açabilir.
Atıf: Oliveira, K.C., Marcos, C.M., Penteado, L.d.A. et al. Modulation of immune cells and metabolic reprogramming in efferocytosis. Cell Death Dis 17, 257 (2026). https://doi.org/10.1038/s41419-026-08431-8
Anahtar kelimeler: efferositoz, bağışık tolerans, doğal bağışıklık, immunometabolizma, kronik inflamasyon