Clear Sky Science · tr
Hipoksik ektopik IGFBP2 hedeflenmesi glioblastomada CD47 aracılı bağışıklık kaçışını aşar
Tümörleri oksijenden yoksun bırakmanın nasıl ters tepebileceği
Doktorlar uzun zamandır ölümcül bir beyin kanseri olan glioblastomanın sıklıkla oksijenden yoksun bölgelerde büyüdüğünü biliyor. Bu hipoksik cepler tümörü tedavi etmeyi zorlaştırır. Bu çalışma, düşük oksijenin kanser hücrelerinin bağışıklık sisteminden nasıl saklanmasına yardımcı olduğunu ortaya koyuyor ve vücudun bunlara karşı daha etkili saldırmasını sağlayabilecek yeni bir kombinasyon tedavisi öneriyor.
Savunmalarımızdan sıyrılan ölümcül bir beyin tümörü
Glioblastoma yetişkinlerde en agresif yaygın beyin tümörüdür ve tipik sağkalım aylarla ölçülür. Bağışıklık hücreleri bu tümörlere sızsa da kanser hücreleri sıklıkla yok edilmekten kaçar. Bu kaçış yollarından biri hücre yüzeyindeki CD47 adlı proteindir; bazen “beni yeme” sinyali olarak adlandırılır ve çevredeki makrofajlar gibi bağışıklık hücrelerine tümör hücresini yutmamalarını söyler. CD47’yi bloke eden ilaçlar hâlihazırda test ediliyor, fakat glioblastoma gibi solid tümörlerde elde edilen sonuçlar karışık; bu, tümör ortamındaki diğer faktörlerin bu terapileri zayıflatıyor olabileceğini düşündürüyor.
Hipoksik bölgeler ve minik kanser parçacıkları
Araştırmacılar tek hücre RNA dizilemesi kullanarak glioblastoma örneklerinin farklı bölgelerinden binlerce hücreyi eşleyip tümörün düşük oksijenli çekirdeğini dış kenarıyla karşılaştırdı. Hipoksik çekirdekte, güçlü CD47 ve IGFBP2 proteini eksprese eden, mezenkimal-benzeri GBM hücreleri adı verilen özellikle agresif bir hücre alt tipi buldular. Aynı zamanda bu çekirdek hücrelerin yüzeylerinde IGFBP2 taşıyan çok sayıda nano boyutlu vezikül olan egzosomlar saldığını keşfettiler. Egzosomlar beyin içinde hatta kana dahi yolculuk edebildiğinden, üretildikleri yerin çok ötesine sinyaller yayabilirler. 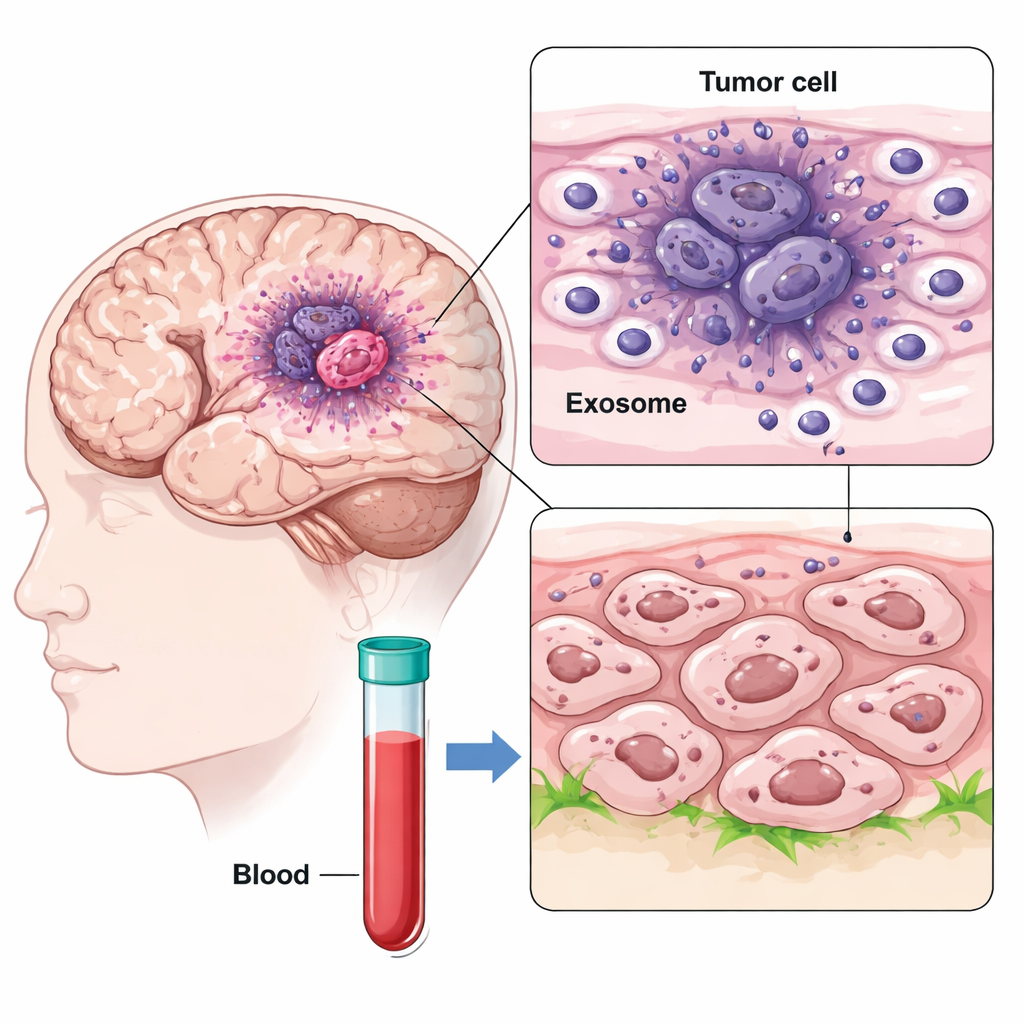
Bir yardımcı protein “beni yeme” sinyalini nasıl güçlendiriyor
Takım daha sonra IGFBP2’nin ne yaptığını inceledi. Düşük oksijen altında HIF-2α adlı bir hipoksi sensörü proteinin tümör hücrelerinde IGFBP2 genini açtığını gösterdiler. IGFBP2 daha sonra egzosomların yüzeyindeki integrin adı verilen belirli reseptörlere bağlanarak dış zarlarını süslüyor. Bu IGFBP2 kaplı egzosomlar diğer tümör hücreleriyle kaynaştığında, hücre içindeki FAK ve STAT3 olarak bilinen proteinleri içeren bir sinyal zincirini aktive ediyor. Bu kaskad sonunda tümör hücresi yüzeyindeki CD47 miktarını artırıyor, makrofajlara gönderilen “beni yeme” mesajını güçlendiriyor ve kanser hücrelerini bağışıklık saldırısından daha fazla koruyor. 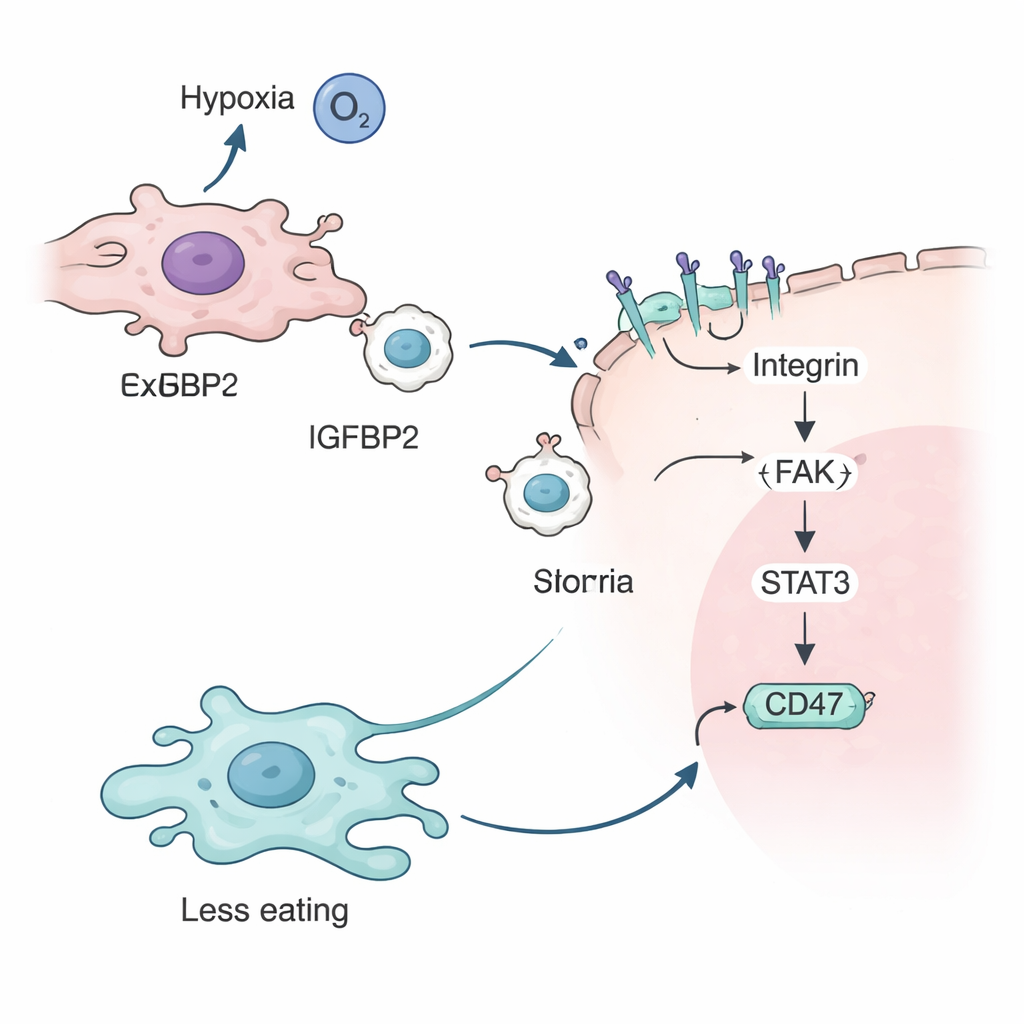
Hasta örnekleri ve hayvan modellerinden kanıt
Bu laboratuvar bulgularını gerçek hastalığa bağlamak için araştırmacılar glioma hastalarının tümör dokusu ve kanını incelediler. IGFBP2 düzeylerinin daha ileri hastalığı olan hastaların hem tümörlerinde hem de kan egzosomlarında daha yüksek olduğunu buldular; bu da IGFBP2-pozitif egzosomların tümör derecesinin kan bazlı bir belirteci olabileceğini düşündürüyor. Fare modellerinde glioblastoma hücrelerinde IGFBP2’yi düşürmek, hücreleri makrofajlar tarafından yutulmaya daha duyarlı hale getirdi, tümör büyümesini yavaşlattı ve sağkalımı uzattı. Tersine, ekstra IGFBP2 zengini egzosomlar eklemek CD47 seviyelerini artırdı, bağışıklık hücresi yutmasını azalttı ve tümör ilerlemesini hızlandırdı.
Umut vaat eden bir iki yönlü saldırı tedavisi
Son olarak ekip, IGFBP2’yi engellemenin CD47 hedefli tedaviyi daha etkili kılıp kılmayacağını test etti. Beyin tümörü olan farelerde hem IGFBP2’ye hem de CD47’ye karşı antikorlarla yapılan tedavi, tek başına uygulananlardan daha güçlü makrofaj aktivitesi, daha küçük tümörler ve daha uzun sağkalım sağladı. Hipoksinin yönlendirdiği IGFBP2 sinyalini keserek ve doğrudan CD47 “beni yeme” sinyalini bloke ederek bu kombinasyon tedavisi tümörün bağışıklık kamuflajına iki yönden saldırdı. Hastalar için bu bulgular, kan egzosomlarındaki IGFBP2’nin CD47 bazlı immünoterapiden en çok yararlanması muhtemel kişileri belirlemeye yardımcı olabileceğini ve IGFBP2 ile CD47 inhibitörlerinin eşleştirilmesinin tek başına her bir ilaçtan daha güçlü bir strateji olabileceğini öne sürüyor.
Atıf: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Anahtar kelimeler: glioblastoma, egzosomlar, bağışıklık kaçışı, CD47, hipoksi