Clear Sky Science · tr
HSPA5, Hippo yolundan bağımsız olarak YAP/TAZ kararlılığını artırır ve glioblastomada proneural‑den mezenkimal geçişi tetikler
Bu beyin kanseri çalışması neden önemli
Glioblastoma, kısmen birçok tümörün zaman içinde daha sert, tedaviye daha dirençli bir hâle geçmesi nedeniyle en ölümcül beyin kanserlerinden biridir. Bu çalışma, yaygın bir stres‑yanıt proteini olan HSPA5’in bu geçişi nasıl kolaylaştırdığını ve tümörü destekleyen molekülleri beklenenden daha uzun süre hayatta tuttuğunu ortaya koyuyor. Bu "hayatta kalma hilesini" anlamak, glioblastomayı daha az agresif hâle getirecek ve mevcut tedavilere daha duyarlı kılacak yeni yaklaşımları işaret ediyor.
Kişiliğini değiştiren bir tümör
Doktorlar ve bilim insanları artık glioblastomanın tek bir hastalık olmadığını, moleküler alt türlerin bir karışımı olduğunu kabul ediyor. İki ana biçim “proneural” tür, genellikle biraz daha az agresif olma eğiliminde, ve “mezenkimal” tür, daha invaziv, tedaviye dirençli ve daha erken nüksle ilişkili. Tümörler proneural durumdan mezenkimal duruma evrilebilir; yazarların proneural‑den‑mezenkimal geçiş (PMT) olarak adlandırdığı süreç bu. Ekip, tümörleri bu tehlikeli yola iten hangi stres‑yanıt proteinlerinin olabileceğini bulmaya koyuldu.
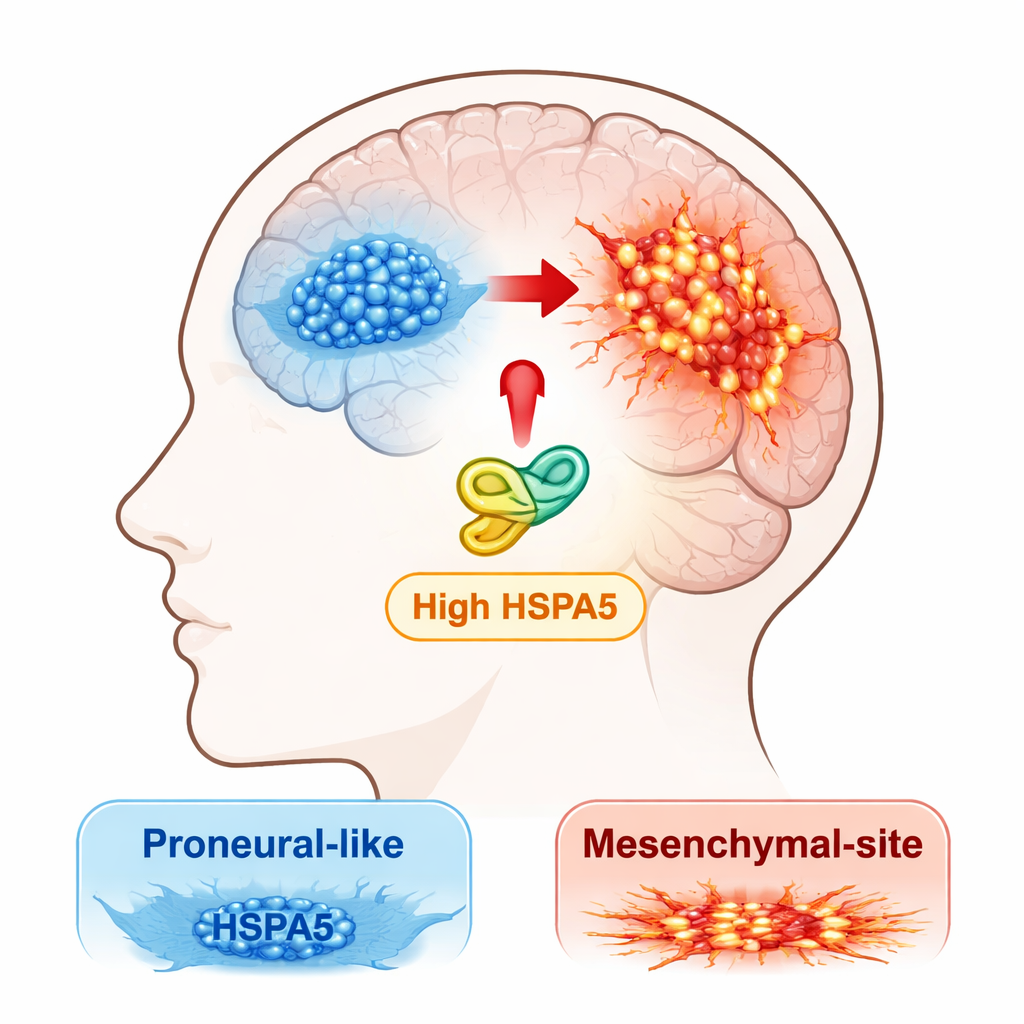
İlgi odağındaki bir stres yardımcısı proteini
Araştırmacılar, HSP70 ailesinin üyelerini — stres altındayken diğer proteinlerin katlanmasına ve hayatta kalmasına yardımcı olan “şaperon” proteinler — büyük kamu kanser veri setlerinde ve kendi hasta örneklerinde tarayarak başladılar. Bir şaperon olan HSPA5 öne çıktı. Aktivitesi glioblastomanın mezenkimal alt türünde en yüksekti ve tümörlerde normal beyin dokusuna kıyasla belirgin şekilde daha fazlaydı. Tümörlerinde daha fazla HSPA5 bulunan hastaların genel sağkalımları daha kötü eğilim gösterdi; bu da HSPA5’i pasif bir izleyiciden ziyade agresif hastalığın potansiyel bir sürücüsü olarak vurguluyor.
Hücreleri daha agresif olmaya zorlamak
HSPA5’in tümör hücreleri içinde gerçekte ne yaptığını keşfetmek için ekip, hastalardan doğrudan alınan primer glioblastoma hücrelerini kültüre aldı ve bunları proneural‑benzeri ve mezenkimal‑benzeri gruplara ayırdı. Proneural hücrelere ekstra HSPA5 ürettirildiğinde, bu hücreler mezenkimal hücreler gibi davranmaya başladı: daha hızlı bölündüler, daha çok göç edip invade ettiler ve CD44 ve c‑MET gibi karakteristik mezenkimal belirteçleri açarken SOX2 ve OLIG2 gibi proneural belirteçleri kapattılar. Tersi de geçerliydi—mezenkimal hücrelerde HSPA5 seviyesini azaltmak, onların büyüme ve invazyonunu zayıflattı ve kısmen daha az agresif bir profile geri itmeye yardımcı oldu.
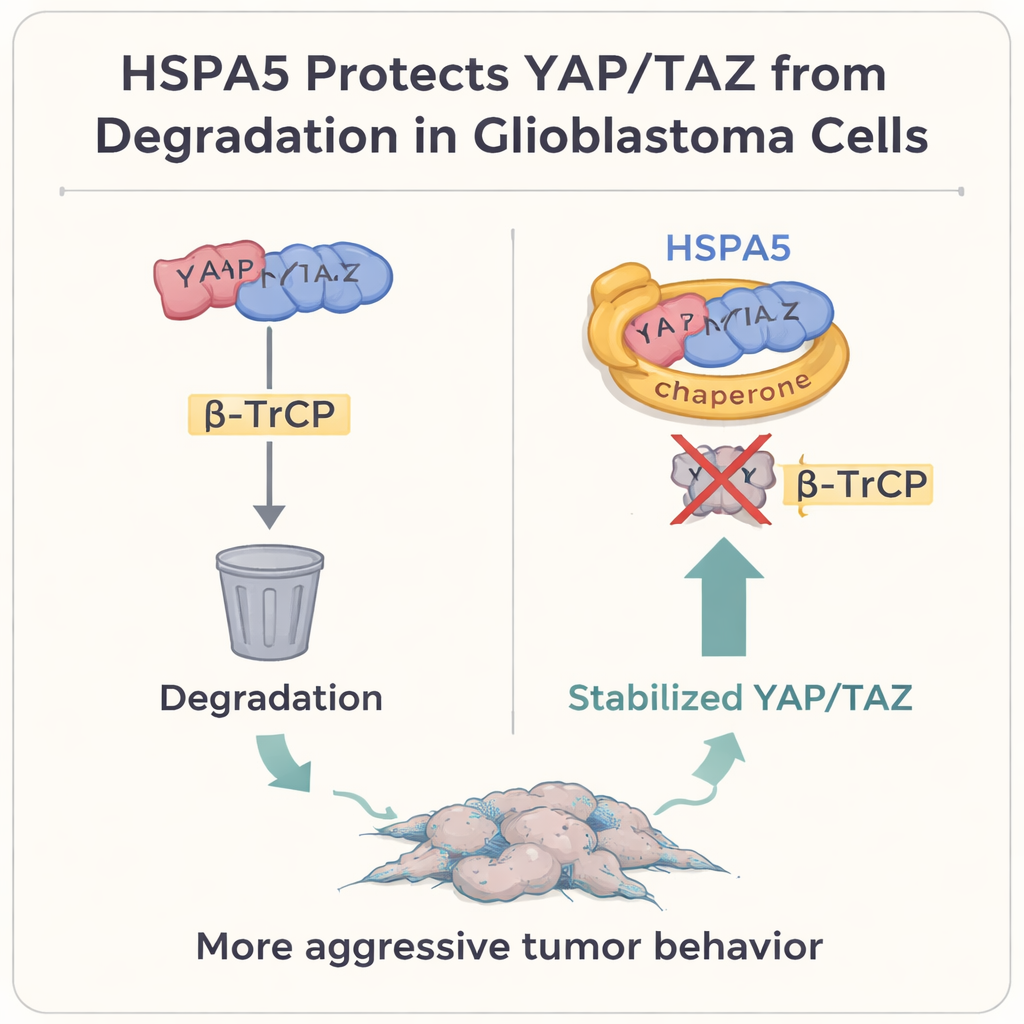
Önemli büyüme anahtarlarını hücresel çöp kutusundan korumak
Daha derine indiklerinde, yazarlar Hippo sinyal yolunun merkezinde yer alan güçlü iki büyüme düzenleyicisi YAP ve TAZ’a odaklandılar. Birçok solid tümörde, dahil olmak üzere glioblastomada, bu proteinler hücre büyümesini, plastisiteyi ve mezenkimal durumunu teşvik eden anahtar anahtarlar gibi davranır. Normalde hücreler bu programı frenlemek istediğinde, YAP ve TAZ’ı β‑TrCP adlı bir protein aracılığıyla etiketleyip proteazoma yani hücrenin “çöp kutusuna” gönderirler. Çalışma, HSPA5’in YAP ve TAZ’a fiziksel olarak bağlandığını ve substrat bağlama bölgesini koruyucu bir eldiven gibi kullanarak β‑TrCP’nin bağlanmasını engellediğini, YAP/TAZ’ın ubikitinasyon ve yıkımını önlediğini ve bunların çekirdeklerinde birikerek CD44 ve c‑MET de dahil olmak üzere mezenkimal genleri açtığını gösteriyor.
Plaklarda ve farelerde hasta tümörlerine kadar
Ekip bu mekanizmayı çeşitli şekillerde doğruladı. HSPA5’i engellemek YAP ve TAZ proteinlerinin daha hızlı kaybolmasına neden oldu; proteazom kimyasal olarak inhibe edilmediği sürece bu gözlendi ve bu proteinlerde “çöp etiketi” sinyallerini artırdı. YAP ve TAZ’ın yeniden etkinleştirilmesi, HSPA5 azaltıldığında görülen büyüme ve invazyon kaybını kurtardı; YAP/TAZ susturulması ise HSPA5 fazla eksprese edildiğinde görülen tümör destekleyici etkileri ortadan kaldırdı. İnsan glioblastoma hücrelerinin fare beyinlerine implante edildiği modellerde, yüksek HSPA5’e sahip tümörler daha hızlı büyüdü ve hayvanları daha çabuk öldürdü; HSPA5’i azaltmak veya YAP/TAZ desteğini kesmek büyümeyi yavaşlattı ve sağkalımı uzattı. Son olarak, nükseden ve daha mezenkimal olan tekrar oluşan tümörler, aynı hastalardan alınan başlangıç proneural‑benzeri örneklere kıyasla daha yüksek HSPA5, YAP, TAZ ve mezenkimal belirteç seviyeleri gösterdi.
Gelecekteki beyin kanseri tedavisi için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma glioblastoma hücrelerinin kritik büyüme anahtarları (YAP ve TAZ) parçalanmaktan korumak için stres‑yanıt yardımcısı HSPA5’i istismar ettiğini öne sürüyor. Bu koruma, tümörlerin daha agresif ve tedaviye dirençli bir kimliğe geçmesine ve bu kimliği sürdürmesine yardımcı oluyor. HSPA5 inhibitörleri gibi küçük‑molekül ilaçlar zaten var ve tümör hücrelerinin bu şaperona normal hücrelerden daha fazla bağımlı olabileceği düşünüldüğünde, HSPA5–YAP/TAZ ekseni çekici bir yeni hedef sunuyor. Bu koruyucu kalkanı zayıflatan tedaviler, glioblastoma hücrelerini daha az uyumlu, daha az invaziv ve kemoterapi ile radyoterapi gibi standart tedavilere karşı daha savunmasız hâle getirebilir.
Atıf: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Anahtar kelimeler: glioblastoma, HSPA5, YAP/TAZ, tümör plastisitesi, mezenkimal geçiş