Clear Sky Science · tr
Mitokondriyal DNA, NLRP3’e bağlanarak mikroglide NLRP3-IL-1β ekseninin aktivasyonunu tetikliyor ve Parkinson hastalği modellerinde nörodejenerasyona yol açıyor
Parkinson hastalığı açısından neden önemli
Parkinson hastalığı titreme ve hareketlerde yavaşlama ile tanınsa da, bu belirtilerin altında beyinde süren karmaşık bir mücadele vardır. Bu çalışma, hasarlı mitokondrilerden kopan küçük genetik parçaların beyin bağışıklık hücrelerinde iltihabı nasıl ateşleyebildiğini ve zaman içinde düzgün hareket için gerekli dopamin üreten nöronların ölümüne yol açtığını açığa çıkarıyor. Bu zinciri anlamak, Parkinson’a benzer hasarı yavaşlatabilecek veya önleyebilecek çok daha spesifik ilaç hedeflerini ortaya koyuyor.
Beynin bağışıklık hücreleri ve stres altındaki enerji santralleri
Beyinde yalnızca nöronlar değil, aynı zamanda yerel bağışıklık hücreleri olan mikroglialar da bulunur. Parkinson hastalığında bu mikroglialar sık sık aşırı aktif hale gelir, çevrelerindeki nöronlara zarar veren toksik moleküller ve inflamatuar sinyaller salar. Yazarlar, kendi DNA’sına sahip olan hücrelerin “enerji santralleri” mitokondrilere odaklandı. Mitokondriler toksinler, yaşlanma veya diğer stresler nedeniyle zarar gördüğünde DNA’ları okside olabilir; bu, reaktif oksijen türlerinin yol açtığı kimyasal bir hasardır. Mitokondriyal DNA bakteriyel DNA’ya benzediği için bu hasarlı parçalar beyinde bir alarm sinyali gibi davranabilir, bağışıklık sistemini uyarabilir ve kronik inflamasyonu tetikleyebilir.
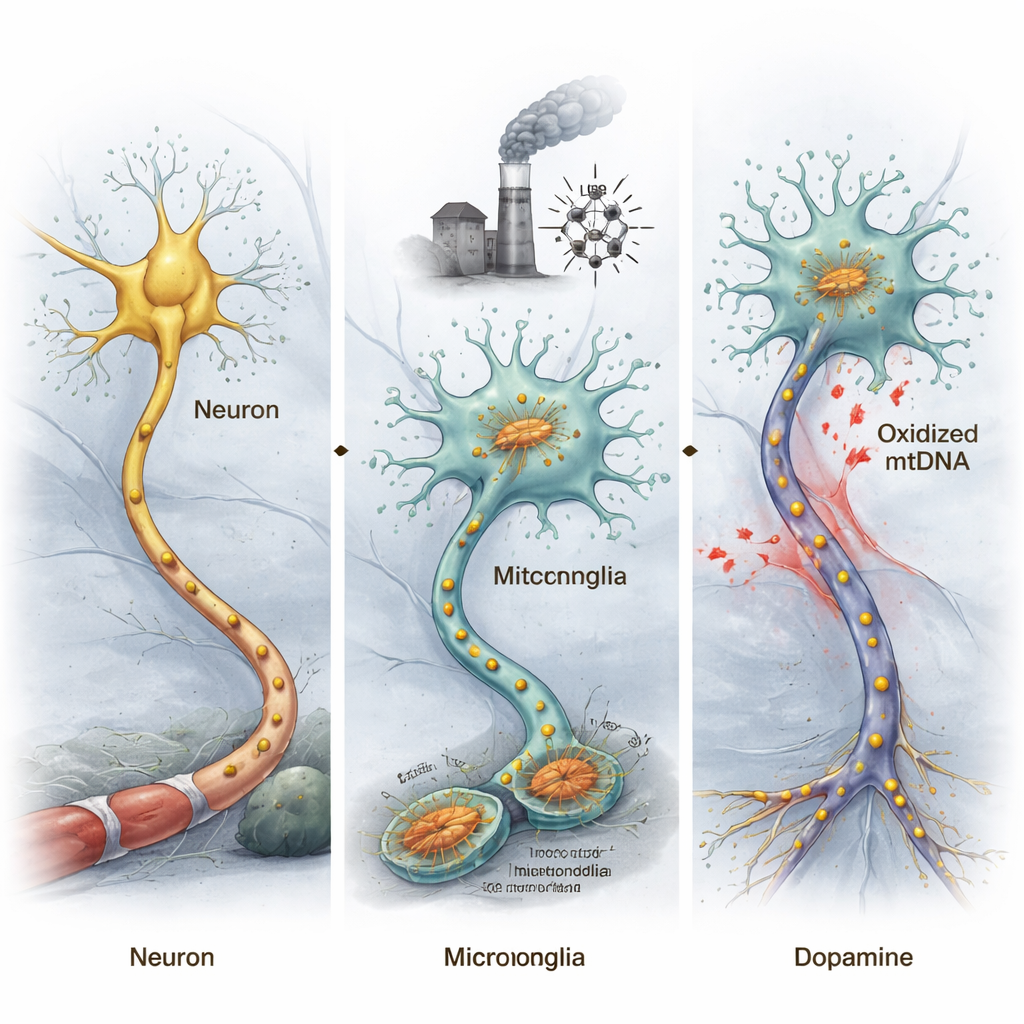
Hasarlı mitokondriyal DNA fareleri Parkinson benzeri duruma itebiliyor
Okside mitokondriyal DNA’nın (ox-mtDNA) gerçekten Parkinson benzeri değişiklikleri tetikleyip tetiklemediğini test etmek için araştırmacılar stres altındaki mikroglialardan ox-mtDNA çıkardı ve bunu hareket için önemli dopamin üreten nöronların bulunduğu bir beyin bölgesine doğrudan enjekte etti. Bu ox-mtDNA’ya maruz kalan fareler davranış testlerinde azalan hareketlilik ve bu dopamin nöronlarının kaybını gösterdi; bu, Parkinson hastalığının temel özelliklerini yansıtır. Orta beyin’den nöronları ve mikrogliaları ayırıp gen etkinliklerini analiz ederek, ekip nöronlarda Parkinson ile ilişkili genlerin daha anormal hale geldiğini, mikroglialarda ise inflamasyonla bağlantılı genlerin güçlü şekilde aktive olduğunu buldu.
Mikroglialarda moleküler bir alarm anahtarı
Çalışma, mikroglialarda inflammazom olarak bilinen daha geniş bir yapının parçası olan NLRP3 adlı protein kompleksine odaklandı. Açıldığında NLRP3, inflamatuar molekül IL-1β’yi aktif, zararlı forma kesen bir enzim olan kaspaz-1’in aktivasyonuna yardımcı olur. Farelerde ve kültürdeki hücrelerde, inflamatuar bir ön uyarı sinyali (LPS, bakteriyel bir bileşen) ile pestisit benzeri bir toksin olan rotenonun kombinasyonu, mikroglialardaki mitokondrilerin okside mtDNA’yı hücre sıvısına salmasına neden oldu. Bu salınım, NLRP3 aktivasyonunda artış, daha fazla kesilmiş (aktif) kaspaz-1 ve daha yüksek IL-1β seviyeleri ile eş zamanlıydı. Aşırı aktive olmuş bu mikroglialardan alınan ortam, kültürde büyütülen dopamin benzeri nöronlar için doğrudan toksik olup hayatta kalmalarını ve ana işaretleyicileri olan tirozin hidroksilaz düzeylerini azalttı.
Doğrudan bağlanma: okside DNA’nın NLRP3 anahtarını nasıl açtığı
Basit bir korelasyonun ötesinde, yazarlar ox-mtDNA’nın inflamasyon sırasında yalnızca mevcut olmadığını—fiziksel olarak NLRP3’e bağlanıp onu açtığını gösterdiler. Mitokondriyal DNA salınımını bir ilaçla engellediklerinde kaspaz-1 ve IL-1β aktivasyonu düştü. Buna karşılık, okside mtDNA’yı doğrudan mikroglialara vermek NLRP3 sinyallemesini kuvvetle artırdı; bu etki okside olmayan mtDNA’ya göre daha güçlüydü. Biyokimyasal çekme (pull-down) deneylerinde, oksidatif hasar belirteçleri açısından zengin mtDNA’nın NLRP3’e bağlı olduğu tespit edildi. Bilgisayar modellemesi ve protein kimyası, ox-mtDNA’nın NLRP3’ün pozitif yüklü, esnek bir bölgesine (aminokasitler 180–187 arasındaki “içsel olarak düzensiz bölge”) bağlandığını ortaya koydu. Bu kritik segment NLRP3’ten çıkarıldığında, ox-mtDNA’yı bağlama ve kaspaz-1’i aktive etme yeteneği büyük ölçüde azaldı.
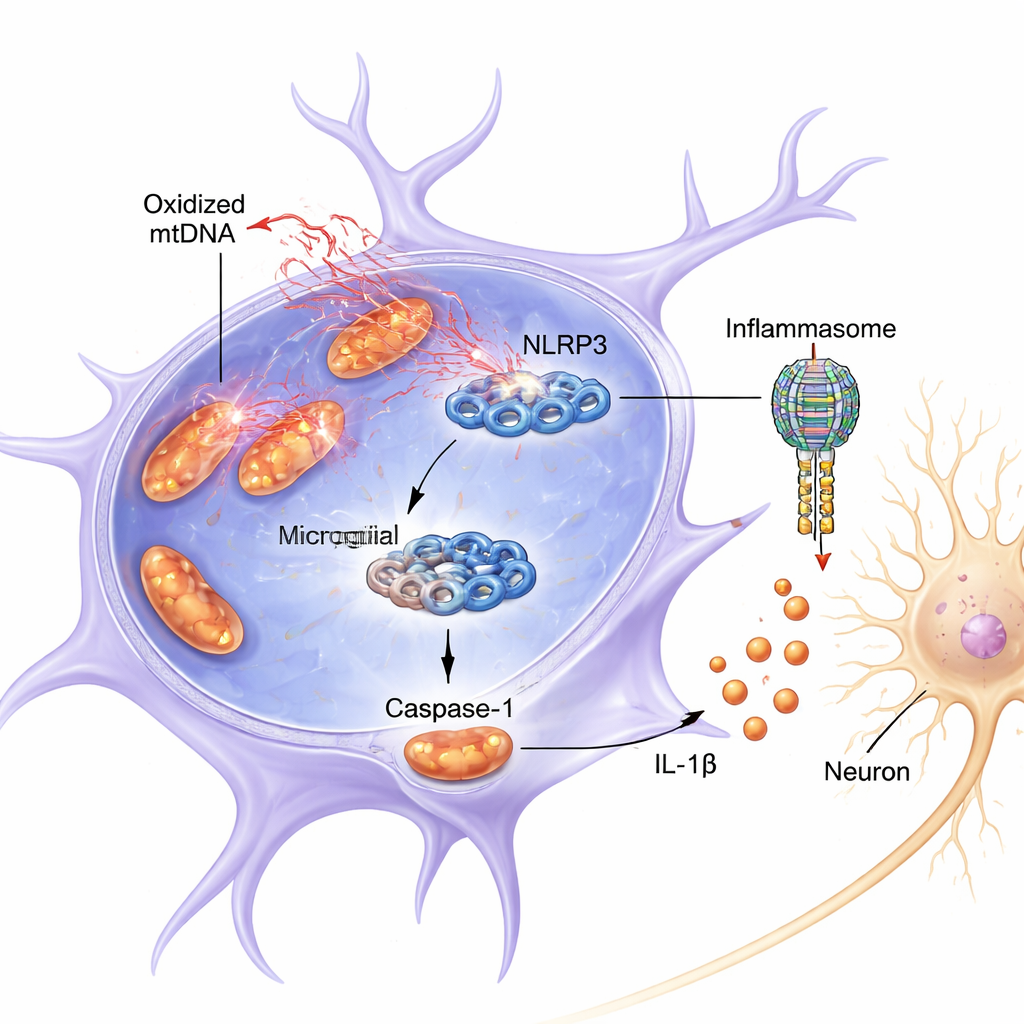
Inflammazomu kapatmak nöronları koruyor
Araştırmacılar daha sonra NLRP3 ile müdahale etmenin nöronları koruyup koruyamayacağını sorguladı. Kültürdeki mikroglialarda NLRP3’ü genetik olarak azaltmak, LPS ve rotenon tedavisinden sonra kaspaz-1 ve IL-1β aktivasyonunu keskin biçimde düşürdü ve bu hücrelerden elde edilen koşullu ortam dopamin benzeri nöronlar için çok daha az toksikti. Farelerde seçici bir NLRP3 inhibitörü (MCC950), mikroglial aktivasyonu azalttı, dopamin nöronlarını korudu ve LPS artı rotenonla ya da enjekte edilen mtDNA ile tetiklenen modellerde inflammazomla ilişkili protein düzeylerini düşürdü. Bu deneyler birlikte ox-mtDNA–NLRP3–IL-1β zincirinin yalnızca hasarla ilişkili olmadığını; gözlemlenen nöron kaybının büyük bölümünde gerekli olduğunu gösteriyor.
Gelecekteki Parkinson tedavileri için ne anlama geliyor
Uzman olmayanlar için temel mesaj şudur: Beyin bağışıklık hücrelerinden sızan hasarlı mitokondriyal DNA doğrudan içsel bir “alarm anahtarına” (NLRP3) tutunabilir, bu da dopamin nöronlarına zarar veren ve modellerde Parkinson’a benzer hastalığı tetikleyen bir inflamasyon dalgası yaratır. Bu etkileşim NLRP3 proteinindeki kısa, tanımlı bir segmente ve mitokondriyal DNA’nın okside doğasına bağlı olduğu için kesin yeni ilaç hedefleri sunar. Mitokondriyal DNA hasarını veya kaçağını önleyen, onun NLRP3’e bağlanmasını engelleyen veya doğrudan NLRP3’ü inhibe eden tedaviler teoride bu inflamatuar kaskadı soğutarak Parkinson hastalığının ilerlemesini yavaşlatabilir.
Atıf: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Anahtar kelimeler: Parkinson hastalığı, mikroglia, mitokondriyal DNA, NLRP3 inflammazom, nöroenflamasyon