Clear Sky Science · tr
Asidik tümör mikroçevresinde SLC26A3’ün laktilasyonu kolorektal karsinomanın kötü huylu ilerlemesini teşvik ediyor
Tümör Asitliğinin Neden Önemli Olduğu
Kolorektal kanser, tümörlerin sıklıkla nüks etmesi, yayılması veya ilaçlara yanıt vermeyi bırakması nedeniyle dünya çapında en ölümcül kanserlerden biri olmaya devam ediyor. Bu çalışma, bu davranışın arkasındaki fazla dikkate alınmamış bir suçluyu inceliyor: tümör içindeki asidik, laktik asit açısından zengin ortam. Bu sert ortamın SLC26A3 adlı koruyucu bir membran proteinini nasıl kararsızlaştırdığını ortaya koyarak, yazarlar kanser hücrelerinin daha kök hücre benzeri, invaziv ve ilaç direncine sahip hâle gelmesini sağlayan yeni bir olay zincirini gösteriyor — tedavi için yeni fikirler sunuyor.
Kanser Hücrelerinin Çevresindeki Sert Bir Mahalle
Hızla büyüyen tümörler büyük miktarlarda şeker ve oksijen tüketir, laktik asit ve hidrojen iyonları salgılar; bu da çevreyi asidik hale getirir. Geniş hasta veri setleri ve doku örneklerini kullanarak araştırmacılar, CA9 adlı bir belirteç proteiniyle izlenen bu asidik durumun agresif kolorektal tümörlerle el ele gittiğini gösteriyor. Daha ileri kanserlerde CA9 düzeyleri yüksekken, SLC26A3 düzeyleri tutarlı şekilde düşüktür. SLC26A3 normalde kolon hücrelerinin yüzeyinde yer alır ve tuz ile bikarbonat dengesine yardımcı olarak pH kontrolüne katkı sağlar. Tümör örneklerinde, kanser hücre hatlarında ve tek hücre analizlerinde ekip, asidite arttığında SLC26A3 düzeylerinin—özellikle kötü huylu, kök hücre benzeri kanser hücrelerinde—azaldığını buluyor. 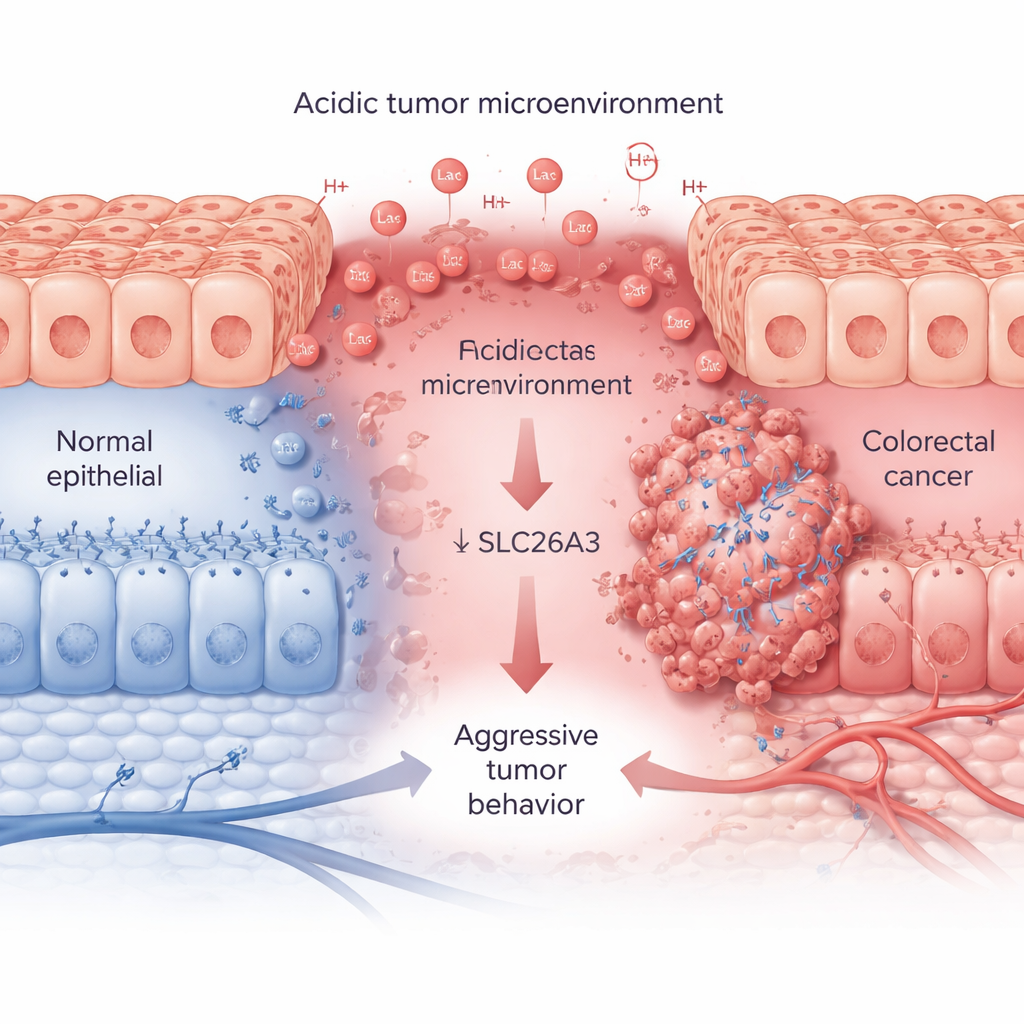
Laktik Asidin Yok Etme İşareti Nasıl Koyduğu
Yazarlar daha sonra neden SLC26A3’ün asidik tümörlerde düştüğünü sorguluyor. Odaklandıkları nokta, laktik asitten türeyen ve proteinlere eklenebilen yeni keşfedilmiş bir kimyasal etiket olan laktilasyon. Kolorektal kanser hücreleri laktik aside maruz kaldığında veya asidik koşullarda büyütüldüğünde SLC26A3 yoğun şekilde laktilasyona uğruyor. Ayrıntılı protein analizleri, bu etiketin eklendiği kritik bir yer olan K536 adlı aminoasidi işaretliyor. K536’daki laktilasyon SLC26A3’ü daha az kararlı hâle getiriyor: protein daha kolay ubikuitin ile işaretleniyor ve hücrenin geri dönüşüm mekanizmasına gönderiliyor. Laktilasyon işaretlerini eklemeye yardımcı olan p300 enzimini engellemek, SLC26A3’ün parçalanmasına kısmen koruma sağlıyor. Sonuç olarak, asidite ve laktat, zararlı bir geri besleme döngüsü kuruyor—daha fazla laktat daha fazla laktilasyona yol açıyor, bu da SLC26A3’ü azaltıyor, pH dengesini daha da bozuyor ve daha asidik bir mikroçevreyi teşvik ediyor.
Kanser Kök Hücre Özellikleri ve Yayılma Üzerindeki Bir Frenin Kapanması
SLC26A3 tükenince kanser hücreleri daha agresif davranıyor. Hücre kültüründe, kolorektal kanser kök hücre benzeri hücreler doğal olarak SLC26A3’ü kök olmayan muadillerinden daha az ifade ediyor. Araştırmacılar SLC26A3 düzeylerini kasıtlı olarak düşürdüklerinde, tümör hücreleri daha fazla küre oluşturuyor (kök hücresellik belirtisi), kendilerini daha verimli yeniliyor, yapay membranlardan daha kolay invaze ediyor ve yara iyileştirme (scratch) hızında daha hızlı göç ediyor. Ayrıca oksaliplatin ve 5‑florourasil gibi yaygın kemoterapi ilaçlarına karşı daha az duyarlı hale geliyorlar. Tersine, SLC26A3’ü artırmak kök hücrelik belirteçlerini azaltıyor ve invazyon ile göçü yavaşlatıyor—ancak bu fayda ek laktat eklendiğinde zayıflıyor; bu da asitliğin koruyucu etkiyi nasıl geçersiz kılabileceğini vurguluyor.
Gen Kontrolüne Gizli Bir Bağlantı
Ayrıca SLC26A3, asitliği düzenlemeye yardımcı olmasının ötesinde HuR ve CUGBP1 adlı iki RNA-bağlayıcı proteini bağlayan bir iskele görevi görüyor. Bu proteinler, kanserle ilişkili birçok mesajcı RNA’nın ömrünü kontrol ediyor. SLC26A3 bol olduğunda, bazı HuR ve CUGBP1 moleküllerini tutarak bunların belirli kanserle ilgili mesajları stabilize etme veya bozma gücünü sınırlıyor. SLC26A3 laktilasyon ve yıkım yoluyla kaybolduğunda, HuR ve CUGBP1 onkogenik mRNA’lara bağlanmakta daha serbest kalıyor; bu da kök hücresellik, epitel‑mezankimal geçiş (EMT), invazyon ve hayatta kalmayı destekliyor. Deneyler HuR’nin kök hücrelik belirteçleri ve hücre birleşim proteinleri için mRNA’ları stabilize etmeye yardımcı olduğunu, CUGBP1’in ise bazı hedeflerde HuR’ye karşı çıkarak birleşim bütünlüğünü azaltıp EMT’yi teşvik ederek tümör yayılımını destekleyebildiğini gösteriyor.
Ortamı Yeniden Dengeleyerek Kanserle Mücadele
Bu bulguların tedavi stratejilerine dönüştürülüp dönüştürülemeyeceğini test etmek için araştırmacılar kolorektal kanserin fare modellerini kullanıyor. Tümör asiditesini sodyum bikarbonat ile nötralize etmek, laktat taşımasını bir MCT1 inhibitörü ile engellemek veya SLC26A3’ü aşırı eksprese etmek tümü tümör büyümesini yavaşlatıyor. SLC26A3 restorasyonunu kemoterapi ile birleştirmek tümörleri daha da küçültüyor. Hasta verilerinde daha yüksek SLC26A3 düzeyleri daha iyi sağkalım, daha az nüks, daha az metastaz ve kemoterapiye daha iyi yanıtlarla korele; bu da bu proteinin hem bir biyobelirteç hem de terapötik bir hedef olarak hizmet edebileceğini düşündürüyor. 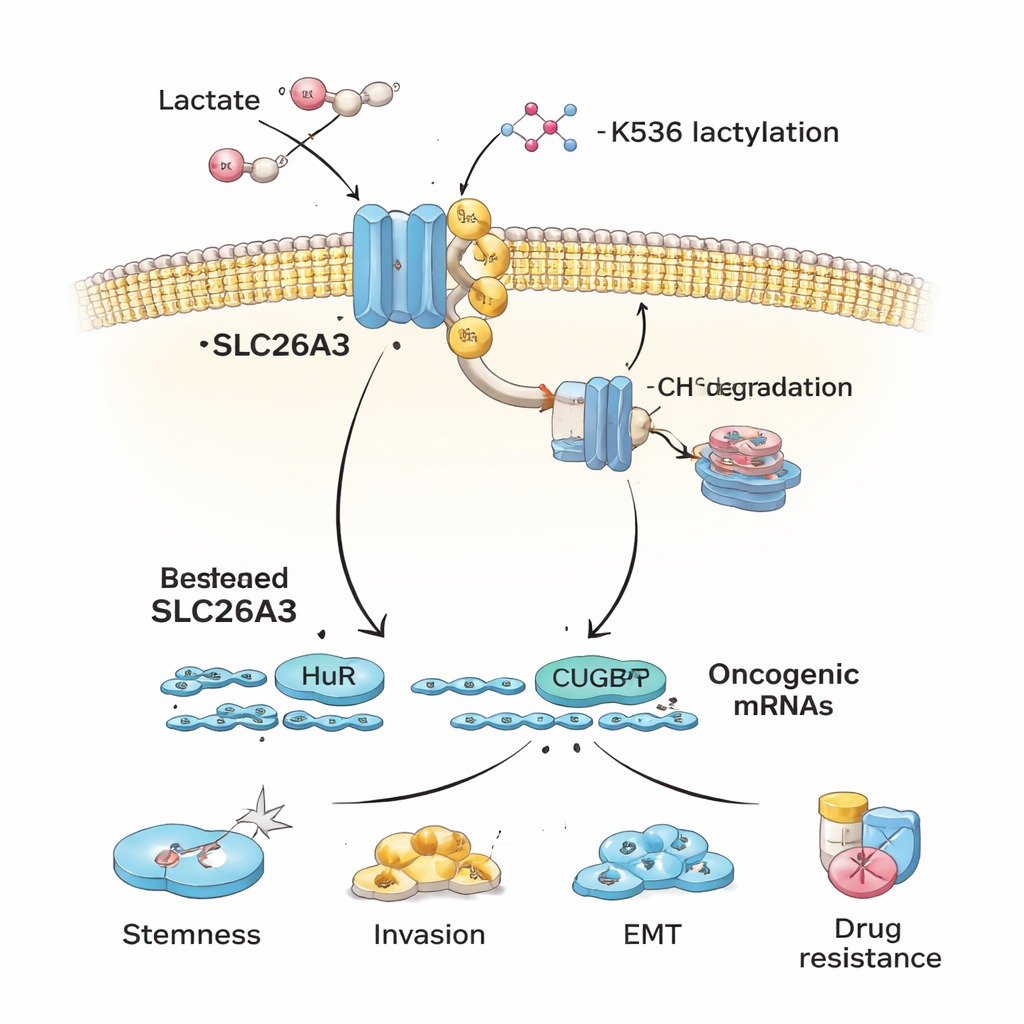
Bu Hastalar İçin Ne Anlama Geliyor
Gündelik ifadeyle, bu çalışma kolorektal tümörlerin koruyucu kapı bekçisi SLC26A3’ü kimyasal olarak “etiketleyip” yok eden ekşi, laktik asit açısından zengin bir banyoda geliştiğini gösteriyor. Bu kapı bekçisi kaybolduğunda, kanser hücreleri daha kolay kök hücre benzeri özellikler edinir, yayılır ve tedaviye direnç gösterir; bu süreç hücre içindeki güçlü RNA düzenleyiciler tarafından desteklenir. Tümör asiditesini tamponlamak, laktat işleme yollarını engellemek veya SLC26A3’ü geri kazanmak, bu kötü huylu geri besleme döngüsünü zayıflatmaya ve standart tedavilerin etkinliğini artırmaya yardımcı olabilir. Bu yaklaşımlar hâlâ titiz klinik denemeler gerektirse de, tümörün kimyasal çevresini yönetmenin kolorektal kanseri kontrol altına almada yeni ve umut verici bir yolu açtığını gösteriyor.
Atıf: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Anahtar kelimeler: kolorektal kanser, tümör mikroçevresi, laktilasyon, kanser kök hücreleri, kemoterapi direnci