Clear Sky Science · tr
DNA-PKcs, kanser hücrelerinde CTLA-4 tükenmesiyle indüklenen senesansı yönlendiriyor
Kanserin Büyüme Düğmesini Durma Sinyaline Çevirmek
Bağışıklık temelli kanser ilaçları sıklıkla tümörlere saldırıda vücudu desteklemek için bağışıklık hücrelerinde bulunan CTLA-4 adlı moleküle odaklanır. Bu çalışma şaşırtıcı bir dönemeç gösteriyor: CTLA-4 aynı zamanda kanser hücrelerinin içinde de bulunuyor ve gizli bir büyüme yardımcısı gibi davranabiliyor. Bilim insanları bu içsel CTLA-4’ü melanom hücrelerinden kasıtlı olarak çıkardıklarında, kanser hücreleri çoğalmayı kesti ve uzun süreli bir “emeklilik” durumu olan hücresel senesansa geçti. Bu beklenmedik rolün anlaşılması, CTLA-4’ü sadece bağışıklık hücrelerinde değil, kanser hücrelerinin içinde hedefleyerek tümörleri yavaşlatma veya küçültme yolları açıyor.
Hücreler Kontrolsüz Büyüme Yerine Emekliliği Seçtiğinde
Hücreler normalde bölünür, onarır ve onarılamayacak kadar hasar gördüklerinde ya ölür ya da büyümeyi kalıcı şekilde durduran senesansa girerler. Senesanslı hücreler genellikle daha büyük olur, şekil değiştirir ve laboratuvarda tespit edilebilen belirli belirteçler üretir. Araştırmacılar fare ve insan melanom hücrelerinde içsel CTLA-4’ü azalttıklarında hücrelerin daha büyük hale geldiğini, büyüme hızının keskin şekilde düştüğünü ve özel boyama testleriyle saptanan enzimler ile hücre döngüsünü engelleyen p16 ve p21 gibi proteinler dahil klasik senesans sinyallerinin yükseldiğini gördüler. Bu değişiklikler hem CTLA-4 geçici olarak susturulduğunda hem de gen düzenleme araçlarıyla kalıcı olarak ortadan kaldırıldığında gözlendi.
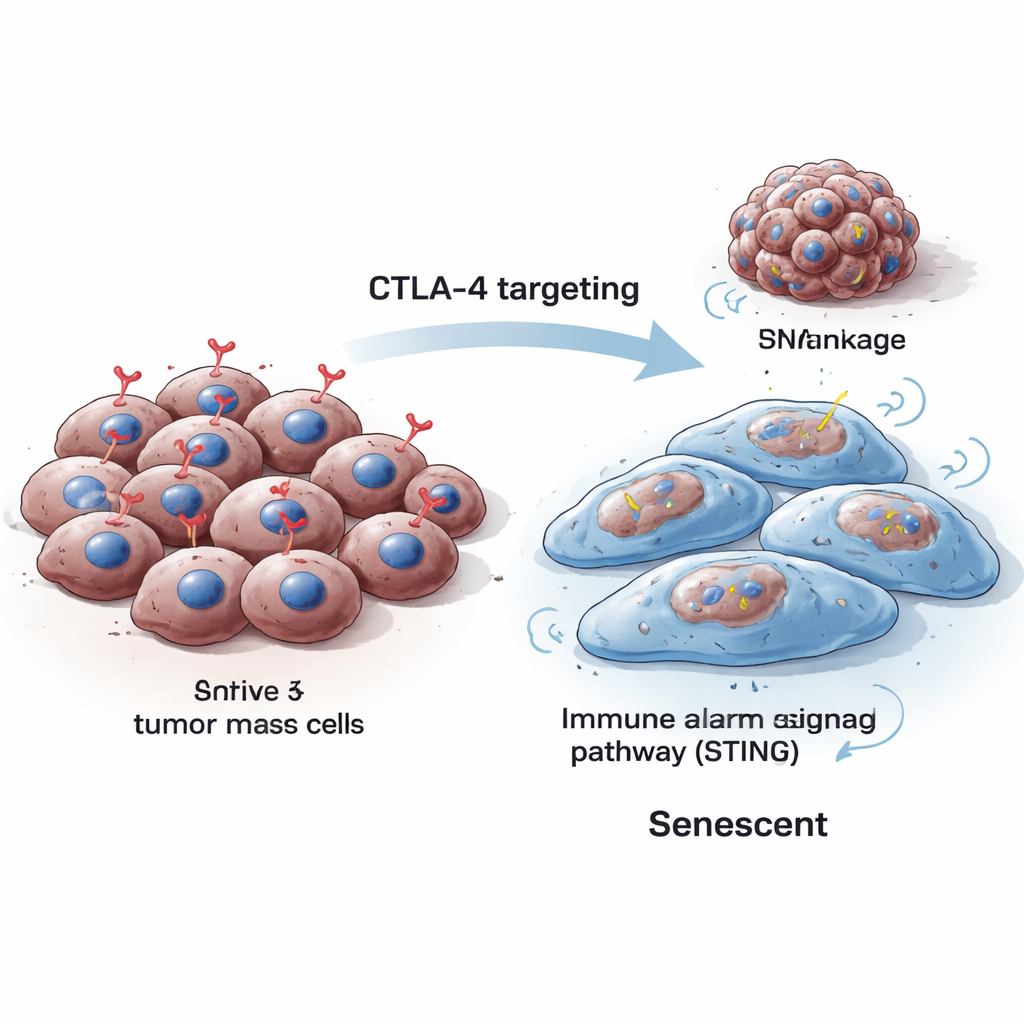
Genetik Planın Çatlakları Bir Durma Noktasına Yol Açar
CTLA-4 kaybının kanser hücrelerini neden senesansa ittiğini anlamak için ekip, bu hücrelerin bölünme sırasında DNA’yı nasıl yönettiğine baktı. CTLA-4 tükenmesinin, kromozomların bölünme sırasında düzgün ayrılmasına yardımcı olan Aurora B adlı proteinin seviyelerini azalttığını keşfettiler. Aurora B düştüğünde hücreler genomik kararsızlık geliştirdi: mikronükleus adı verilen küçük ekstra DNA içeren yapılar ortaya çıktı ve DNA hasarı belirteçleri arttı. Bu tür DNA stresi, hücreleri kontrolsüz büyüme yerine senesansa itmesiyle bilinir. Önemli olarak, Aurora B’nin geri kazandırılması bu mikronükleusları azaltmaya yardımcı oldu ve CTLA-4 kaybını doğrudan hatalı kromozom yönetimi ve DNA hasarıyla ilişkilendirdi.
DNA Hasarı İçsel Bir Alarm Ağını Tetikliyor
CTLA-4 tükenmiş hücrelerdeki kırık ve yanlış yerleşmiş DNA gözden kaçmadı. Bu durum bir DNA hasarı sensörü olan DNA-PKcs’yi aktive etti ve bu da hücre içindeki yabancı DNA’ya yanıt veren yerleşik alarm sistemi STING yolunu tetikledi. STING açıldıktan sonra TBK1 ve IRF3 dahil aşağı akış moleküllerini sinyalledi ve aynı zamanda başka bir önemli büyüme kontrol yolu olan AKT yolunu da güçlendirdi. Bu sinyal kombinasyonu büyümeyi teşvik etmek yerine güçlü bir hücre döngüsü freni olan p21’i artırdı ve senesans durumunu pekiştirdi. Bilim insanları DNA-PKcs’yi engellediklerinde STING aktivasyonu ve senesans özellikleri büyük ölçüde azaldı; bu da DNA-PKcs’nin bu alarm rölesinin merkezinde yer aldığını gösterdi.
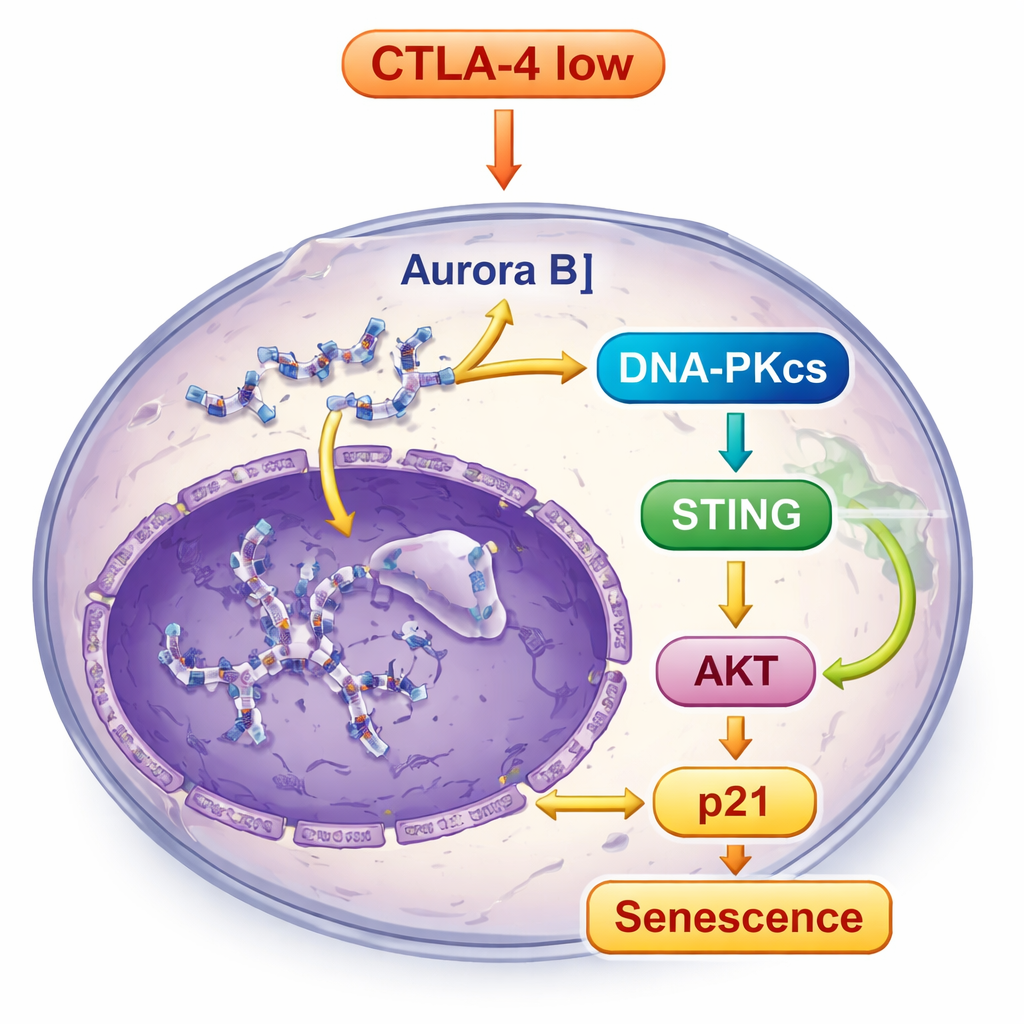
Hücre Kültüründen Canlı Hayvanlardaki Tümörlere
Labaratuvar kapları hikâyenin yalnızca bir kısmını anlatır, bu yüzden araştırmacılar CTLA-4 kaybının farelerde gerçek tümörleri etkileyip etkilemeyeceğini test ettiler. CTLA-4’lü veya CTLA-4’süz melanom hücrelerini aynı hayvanın karşı taraflarına implant ettiler. CTLA-4 eksik tümörler daha yavaş büyüdü, daha az ağırlığa sahipti ve hacim olarak CTLA-4 içeren karşıtlarından daha küçüktü. Bu CTLA-4’den yoksun tümörler ayrıca daha güçlü senesans boyaması ve daha yüksek DNA hasarı ile STING yolu aktivasyonu gösterdi. Büyük kamu veri tabanlarındaki hasta kanser verilerinin analizi de bu bağlantıyı destekledi: birkaç kanser türünde CTLA-4 ekspresyonu genellikle DNA-PKcs ve diğer DNA onarım bileşenleriyle ters ilişkiliydi ve bu bulgular insan hastalığındaki laboratuvar sonuçlarını yankıladı.
Gelecekteki Kanser Tedavileri İçin Anlamı
Genel olarak çalışma, kanser hücreleri içindeki CTLA-4’ün genetik kararlılığı korumaya ve hücre bölünmesini sürdürmeye yardımcı olduğunu gösteriyor. CTLA-4 kaldırıldığında kromozomlar kararsızlaşıyor, DNA kırıkları birikiyor ve DNA-PKcs ve STING merkezli içsel bir alarm yolunun aktifleşmesi hücreleri kalıcı büyüme durdurmasına itiyor. Bir bilim dışı okuyucu için bunun anlamı şu: tümör hücrelerinde CTLA-4’ü kapatmak, kanserleri tehlikeli, hızlı büyüyen davranıştan uzaklaştırıp daha güvenli, “emekli” bir duruma yönlendiriyor. Bu bulgular, gelecekteki kanser tedavilerinin yalnızca bağışıklık hücrelerindeki CTLA-4’ü bloke ederek bağışıklık sistemini serbest bırakmakla kalmayıp, aynı zamanda CTLA-4’ü kanser hücrelerinin içinde doğrudan etkisiz hale getirip senesansı kanser büyümesini durdurmak için bir araç olarak kullanacak şekilde tasarlanabileceğini öne sürüyor.
Atıf: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Anahtar kelimeler: hücresel senesans, melanom, CTLA-4, DNA hasarı, STING yolu