Clear Sky Science · tr
TET2’nin sitoplazma‑çekirdek taşınması: kolorektal kanser ilerlemesinde içsel bir fren
Kanser Hücreleri Kendi Frenlerini Nasıl Taşır
Kolorektal kanser, dünya çapında en yaygın kanserlerden biridir ve tümör hücreleri çevre dokuya invaze etmeyi ve diğer organlara yayılmayı öğrendikçe sıklıkla ölümcül hale gelir. Bu çalışma, bu kanser hücrelerinin birçoğunun aslında ilerlemelerini yavaşlatabilecek içsel bir “fren sistemine” sahip olduğunu ortaya koyuyor — TET2 adı verilen bir protein; bu protein hücrenin çekirdeğine girdiğinde ilerlemeyi yavaşlatabiliyor. Bu yerleşik frenin nasıl açılıp kapandığının anlaşılması, tümör büyümesini sadece kanser hücrelerini yok etmeye çalışmak yerine kontrol altında tutmanın yeni yollarını açabilir.
Tümör Hücreleri İçinde Kritik Bir Proteinin Hareketini İzlemek
Araştırmacılar, DNA üzerindeki belirli kimyasal işaretleri kaldırarak hangi genlerin açık ya da kapalı olduğunu kontrollemeye yardımcı olan TET2 proteinine odaklandı. Yüzlerce kolorektal kanser hastasından alınan doku örneklerinde TET2’nin tümör hücreleri içindeki konumunu izlediler. Dört ana desen buldular: çoğunlukla çekirdekte, çoğunlukla sitoplazmada veya birine güçlü biçimde eğilimli. Tümörlerinde daha fazla TET2 çekirdekte olan hastaların genellikle daha uzun yaşadığı, oysa TET2’yi sitoplazmada tutan hastaların daha kötü seyrettiği görüldü. Kanserler klinik evre ilerledikçe çekirdeksel TET2’nin daha nadir hale gelmesi, bu çekirdeksel korumanın kaybının tümörlerin daha agresif hâle gelmesinin bir parçası olduğunu düşündürüyor.
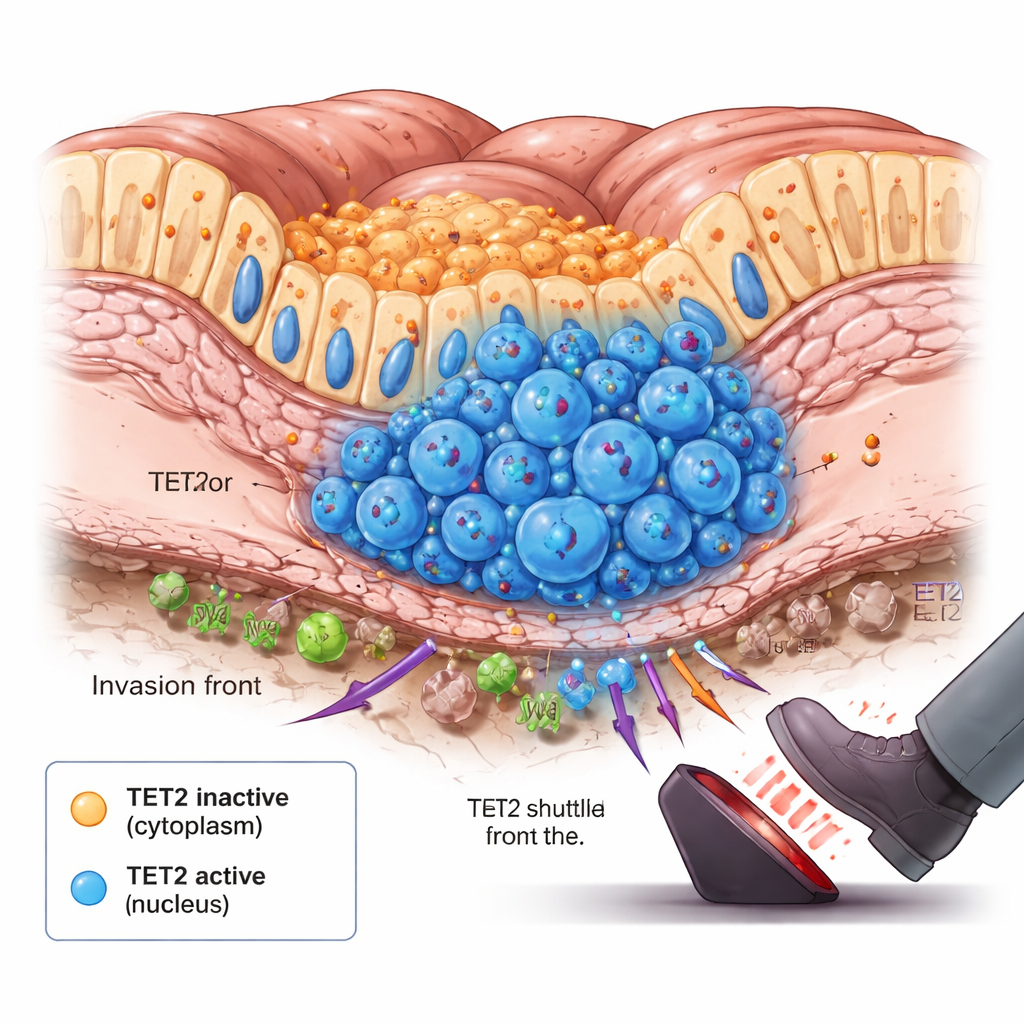
Tümörün Ön Hattı ve Değişim Anı
Daha derine indiklerinde ekip şaşırtıcı bir şey fark etti: yeni yayılmaya başlayan tümörlerde, TET2’nin çekirdeğe taşındığı hücrelerde hafif bir artış vardı. Bu hücreler, kanser hücrelerinin ilk olarak daha derin dokuya doğru ittiği bağırsak örtüsünün altındaki invazyon hattında kümelenmişti. Hayvan deneyleri ve tümör büyümesini taklit eden uzun süreli hücre kültürü modelleri de zaman içinde benzer bir desen gösterdi. Erken aşamada TET2 sitoplazmada kalıyordu ve büyük ölçüde inaktifti. Tümörler büyüdükçe ve iç bölgeler oksijen ve besinlerden mahrum kaldıkça, hücre içi sinyaller belirli alt popülasyonlarda TET2’nin çekirdeğe taşınmasını tetikledi. Oraya ulaştığında TET2 DNA metilasyon işaretlerini kaldırmaya ve tümör büyümesini yavaşlatmaya başladı; kanser tehlikeli bir eşik aştığında acil durum freni gibi davrandı.
“Git” Sinyalleri Birlikte Bir Freni de Tetiklediğinde
Kolorektal tümörler sıklıkla iki güçlü “git” programına dayanır: hücrelerin daha hareketli ve invaziv hale gelmesine yardımcı olan epitel–mezenkim geçişi (EMT) adlı şekil değiştirme süreci ve büyüme ile hayatta kalmayı destekleyen WNT sinyal yolu. Bu yollar genellikle kanserde tamamen zararlı olarak görülür. Ancak bu çalışma, EMT ve WNT güçlü şekilde aktive olduğunda TET2’yi çekirdeğe de yönlendirmeye yardımcı olduklarını gösteriyor. Hücre kültürlerinde ilaçlar ve genetik araçlar kullanılarak yapılan deneylerde, EMT veya WNT’nin açılmasının daha fazla hücrenin TET2’yi çekirdeğine taşımasına yol açtığı; bu yollar bloke edildiğinde ise tersinin gerçekleştiği gösterildi. Çekirdekte aktif hale gelen TET2 ise EMT ve WNT ile ilişkili genleri baskılayarak hücre göçünü azalttı ve çoğalmayı yavaşlattı. Başka bir deyişle, tümörlerin büyümesine yardımcı olan aynı sinyaller, içsel bir karşı gücü de uyandırıyor.
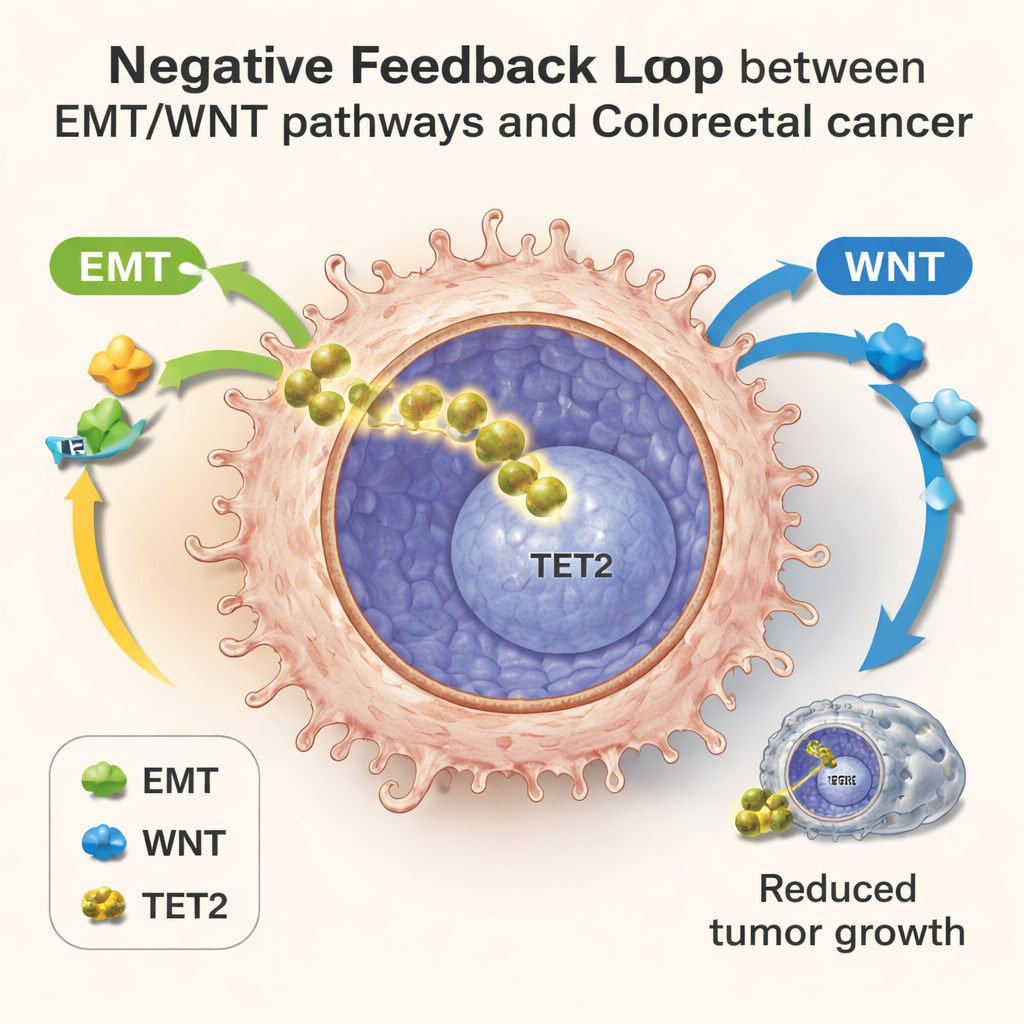
Tek Hücreler Gizli Bir Geri Besleme Döngüsünü Ortaya Koyuyor
Bu çekişmeyi ayrıntılı şekilde haritalamak için ekip, binlerce bireysel hücrede hangi genlerin aktif olduğunu okuyan tek hücre RNA dizilemesini kullandı. Laboratuvarda yetiştirilen kolonilerde, fare tümörlerinde ve kolorektal kanser hastalarından alınan örneklerde, hücrelerin bir ilerleme zaman çizgisi boyunca yayıldığını gördüler. Erken hücreler normal enerji kullanımı ve zayıf EMT/WNT aktivitesi gösterirken; daha sonraki hücreler metabolik yeniden yapılanma, güçlü EMT/WNT sinyalleri ve ardından artan TET2 hedef genleri sergiledi. Bu daha ileri adımlarda, daha yüksek TET2 aktivitesine sahip hücrelerde invazyonla ilgili genlerin daha düşük olduğu ve yayılmaya başlamış tümörler arasında bile daha iyi hasta sonuçlarıyla ilişkilendirildiği görüldü. Bu desen, negatif bir geri besleme döngüsü fikrini destekliyor: metabolik stres ve EMT/WNT aktivasyonu TET2’yi çekirdeğe itiyor ve çekirdeksel TET2 de bu aynı agresif programları sınırlıyor.
Gelecekteki Kanser Tedavileri İçin Anlamı
Uzman olmayanlar için temel mesaj şudur: kolorektal kanser ilerlemesi basit bir “açık/kapalı” anahtarı değildir. Bunun yerine, yerleşik, gecikmeli bir güvenlik mekanizması vardır: tümör hücreleri daha invaziv hâle geldikçe, çekirdekte TET2’yi de aktive ederler; bu da onları kısmen dizginler. Zamanla birçok tümör çekirdeksel TET2’yi kaybederek veya onun etkilerini ezerek bu mekanizmadan kaçıyor. TET2’yi çekirdekte tutmanın veya aktivitesini artırmanın yollarını bulmak — muhtemelen EMT veya WNT’yi düzenleyen ilaçlarla kombinasyon halinde — doktorların bu doğal freni güçlendirerek kanserin yayılmasını yavaşlatmasına olanak verebilir. Dışarıdan sadece kanser hücrelerini yok etmeye çalışmak yerine, gelecekteki tedaviler bu içsel kontrol sistemini geri kazandırıp güçlendirmek üzerine çalışabilir.
Atıf: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Anahtar kelimeler: kolorektal kanser, TET2, epigenetik, EMT WNT sinyalizasyonu, kanser ilerlemesi