Clear Sky Science · tr
Gelişimsel transkripsiyon faktörü PAX6’nın anormal devamı JNK3 sinyali yoluyla nöronal hücre ölümünü destekler
Bu araştırma görme için neden önemli
Glaukom, görsel bilgiyi gözden beyne taşıyan sinir hücrelerinin (nöronların) yavaşça ölmesi nedeniyle kalıcı körlüğün önde gelen nedenlerinden biridir. Birçok tedavi göz içi basıncını düşürür, ancak basınç iyi kontrol altındayken bile görme kaybı yaşanabilir. Bu çalışma daha derin bir soruyu soruyor: bu retinal sinir hücrelerini stres altındayken ölmeye ne karar verdirir ve hücre çekirdeğindeki gen kontrol düzeyinde bu kararı kapatabilir miyiz?
Saldırı altındaki stresli bir retina
Glaukom ve ilişkili göz hastalıklarının merkezinde, gözün çıktı nöronları olan retinal ganglion hücrelerinin (RGC) yavaş kaybı yatar. Bu hücreler, aşırı uyarılan NMDA reseptörleri ve zararlı kalsiyum aşırı yüklenmesi de dahil olmak üzere birçok stres türüne karşı savunmasızdır. Araştırmacılar, göze az miktarda NMDA enjekte edilen ve RGC’leri seçici olarak yaralayan, diğer retinal katmanları büyük ölçüde koruyan iyi yerleşmiş bir fare modelini kullandılar. Bu tedavinin göz içi basıncını değiştirmediğini, ancak RGC’lerde mitokondriden sitokrom c salınımı ve TUNEL-pozitif çekirdeklerin görünmesi gibi programlı hücre ölümü tipik belirtilerine yol açtığını doğruladılar.
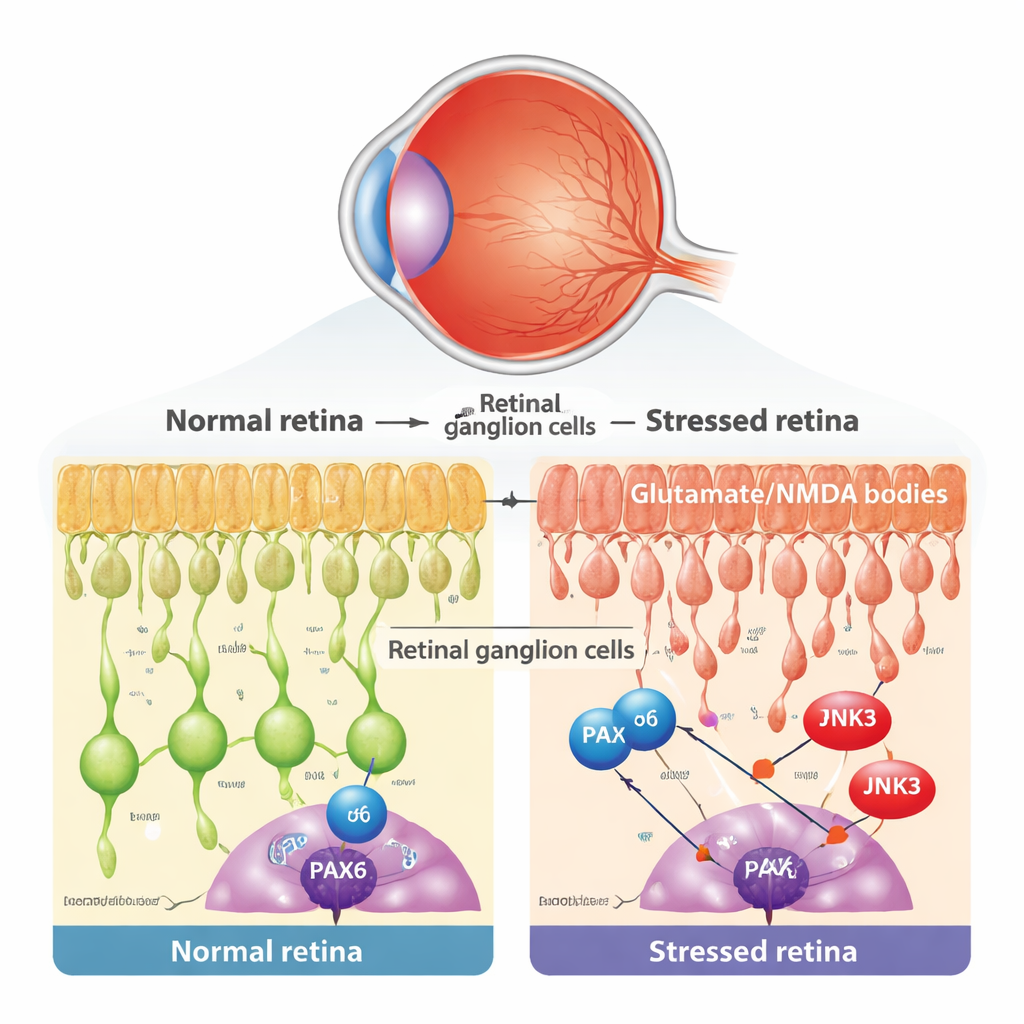
Emekli olmaya dirençli bir gelişim geni
Erken gelişimde, PAX6 adı verilen bir gen düzenleyici gözün baş mimarı olarak görev yapar; farklı retinal hücrelerin nasıl doğduğunu ve bağlandığını yönlendirir. Geleneksel görüşe göre bu tür gelişim programları erişkinlikte büyük ölçüde kapanır. Fare ve insan retinalarından elde edilen tek hücre RNA dizileme verilerini yeniden analiz ederek ekip, PAX6’nın olgun RGC’lerde ve belirli interneuronlarda güçlü ve seçici olarak korunduğunu buldu. Mikroskobik boyama ile, RGC’lerin bulunduğu katmanda PAX6’nın büyük ölçüde komşu amakrin hücreler yerine ganglion hücrelerinde bulunduğunu gösterdiler. Bu, erişkin hastalıkta eski bir gelişim programının ele geçirilip dejenerasyonun sürükleyicisine dönüştürülebileceği ilginç olasılığını gündeme getirdi.
Koruyucudan cellatlığa: PAX6 rol değiştiriyor
PAX6’nın RGC’lerin stres altında hayatta kalmasına mı yoksa ölmelerine mi yardımcı olduğunu test etmek için bilim insanları gen terapisi benzeri bir yaklaşım kullandılar. Retinaya PAX6’yı özgül olarak baskılayan küçük bir RNA taşıyan viral bir vektör teslim ettiler ve ardından gözleri NMDA’ya maruz bıraktılar. Kontrol tedavisi alan gözlerle karşılaştırıldığında, PAX6 azaltılmış retinelerde apoptotik RGC sayısı ve mitokondri hasarı çok daha azdı; bu da bu modelde tam ölmek için PAX6’nın gerekli olduğunu gösterdi. Genom çapında RNA dizileme, özellikle mitokondri hasarı ve kaspaz aktivasyonu ile ilgili birçok pro-ölüm geninin normal farelerde NMDA ile güçlü şekilde indüklendiğini, ancak PAX6 susturulduğunda bu yanıtın zayıflatıldığını ortaya koydu. Başka bir deyişle, PAX6 RGC’leri uçuruma iten bir gen ağını etkinleştirmeye yardımcı oluyor.
PAX6 anahtarını çeviren stres kinazı
Stres PAX6’yı miktarını artırmadan nasıl etkinleştiriyor? Ekip, ağırlıklı olarak nöronlarda bulunan stres duyarlı bir enzim olan JNK3’e odaklandı. NMDA yaralanması altında JNK3, RGC çekirdeğine taşındı ve fiziksel olarak PAX6 ile ilişki kurdu. Saflaştırılmış proteinler kullanılarak yapılan biyokimyasal "deney tüpü" deneyleri, JNK3’ün doğrudan PAX6’ya fosfat grubu ekleyebildiğini ve bu reaksiyonun bir JNK inhibitörü ile engellendiğini gösterdi. Jnk3 geni olmayan farelerde, NMDA artık aynı PAX6 fosforilasyon desenini üretmiyordu. Kromatin haritalama (ChIP-seq) ve hedefe yönelik DNA-bağlanma testleri, stres altında fosforile PAX6’nın JNK3 ile birlikte Bax ve Gadd45a gibi kilit pro-apoptotik genlerin kontrol bölgelerine daha güçlü bağlandığını ve bunların aktivitesini artırdığını ortaya koydu. PAX6 susturulduğunda veya JNK3 genetik olarak kaldırıldığında, bu bağlanma ve buna karşılık gelen pro-ölüm gen aktivasyonu keskin biçimde azaldı.
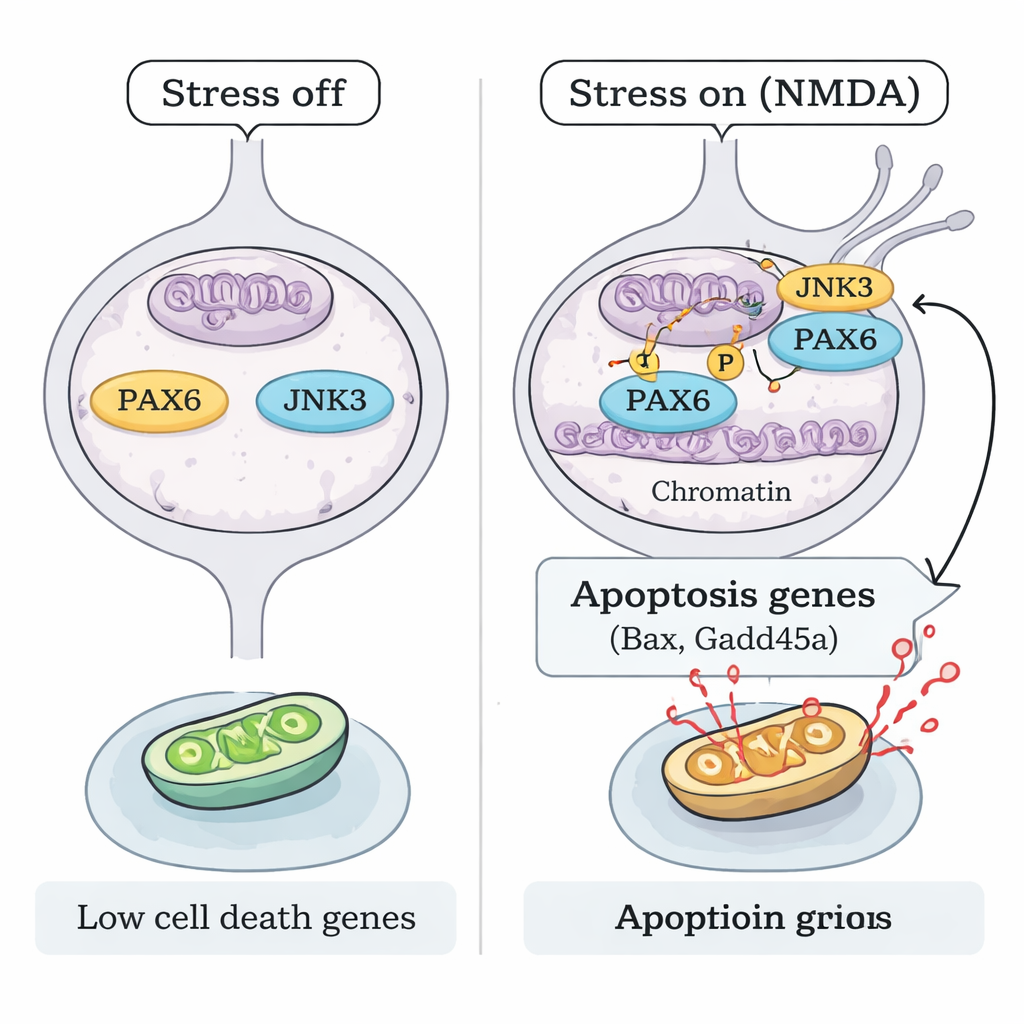
Görmeyi korumak için ölüm programını kapatmak
Son olarak, araştırmacılar bu JNK3–PAX6 eksenini engellemenin görme için kritik hücreleri korumaya yetip yetmeyeceğini sordular. Hem PAX6 susturulmuş farelerde hem de JNK3 eksik farelerde, NMDA maruziyeti sonrası RGC’ler belirgin şekilde korundu; daha az hücre ölümü ve daha sağlıklı retinal yapı gözlendi. Bu, açık bir mekanistik modele işaret ediyor: eksitotoksik stres altında JNK3, kalıcı olarak ifade edilen PAX6’yı fosforile ederek onu gelişimsel bir yapıcıdan erişkin RGC’lerde güçlü bir hücre-ölüm gen programı aktivatörüne dönüştürüyor. Bu bağlantıyı—PAX6’yı susturarak veya JNK3’ü devre dışı bırakarak—kesmek birçok nöronun hayatta kalmasını sağlıyor. Hastalar açısından, bu çalışma gelecekteki glaukoma tedavilerinin göz içi basıncını düşürmenin ötesine geçerek retinal nöronların yaşayıp yaşamamaya karar veren genetik anahtarları doğrudan hedefleyebileceğini öneriyor.
Atıf: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
Anahtar kelimeler: glaukom, retinal ganglion hücreleri, PAX6, JNK3, nörodejenerasyon