Clear Sky Science · tr
Sec8: anti-RNA virüslere karşı savunmada RIG-I’in yeni bir pozitif düzenleyicisi
Hücrelerimiz Sinsi Virüsleri Nasıl Tespit Ediyor
Grip ve yeni ortaya çıkan hayvan kökenli virüsler dahil birçok tehlikeli virüs genetik materyalini RNA olarak taşır. Hücrelerimiz, bu istilacıları hızla fark edip antiviral yanıt başlatabilmek için içsel alarm sistemlerine güvenir. Bu makale, Sec8 adıyla az bilinen bir hücresel proteini inceliyor ve bu proteinin, ana viral algılayıcılardan biri olan RIG‑I’in bizi koruyacak kadar uzun süre canlı ve aktif kalmasını sessizce sağlamakta merkezi bir rol oynadığını gösteriyor.
Tehdit Altındaki Hücresel Bir Hırsız Alarmı
RIG‑I, hücre içini viral RNA parçaları açısından devriye gezen moleküler bir “hırsız alarmı” gibidir. Şüpheli RNA’yı algıladığında şekli değişir, etkinleşir ve nihayetinde tip I interferonlarını tetikleyen sinyaller gönderir—bunlar yakın hücrelerin enfeksiyona karşı direnç kazanmasına ve bağışıklık savunmalarının aktive olmasına yardımcı olan güçlü uyarı molekülleridir. Aşırı aktif bir alarm zararlı iltihaba veya otoimmün hastalığa yol açabileceğinden hücreler RIG‑I seviyesini sıkı biçimde kontrol eder. Bir dizi başka protein, RIG‑I’e küçük ubikitin zincirleri ekleyerek onu hücresel “parçalayıcı” olan proteazoma götürebilir. Aktif RNA virüs enfeksiyonu sırasında RIG‑I’in zamanından önce yok edilmesine karşı hangi ek hücresel faktörlerin koruma sağladığı şimdiye dek belirsizdi.
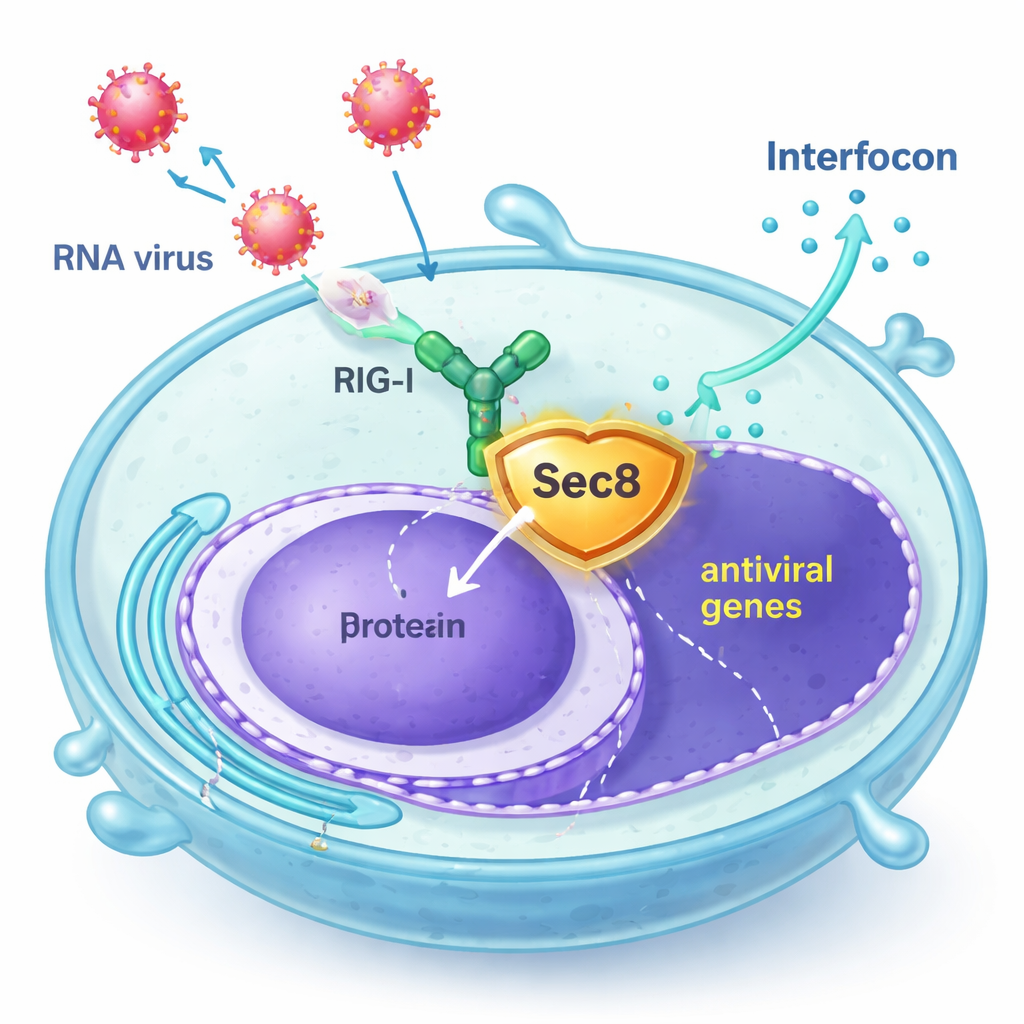
Sec8 Koruma İçin Devreye Giriyor
Yazarlar, salgı veziküllerinin hücre yüzeyi ile kaynaşmasına yardımcı olan sekiz proteinli bir kompleksin parçası olarak bilinen Sec8’in, aslında antiviral sinyalleşmeyi artırdığını keşfettiler. İnsan hücre hatlarında ve birinci el fare bağışıklık hücrelerinde Sec8 düzeyi arttırıldığında, veziküler stomatit virüsü (VSV) ve Sendai virüsü gibi RNA virüsleriyle enfeksiyon sonrasında veya sentetik viral RNA’ya maruz kalındığında interferon‑ilgili genlerin daha güçlü şekilde aktifleştirildiği görüldü. Tersine, Sec8 azaltıldığında interferon ve interferon uyarılan genlerin üretimi düştü ve hücreler viral çoğalmaya karşı daha az dirençli hale geldi. Bu bulgular Sec8’in yalnızca salgıda değil, antiviral alarm yolunda pozitif bir düzenleyici olarak görev yaptığını düşündürdü.
Hücresel Parçalayıcıyı Engellemek
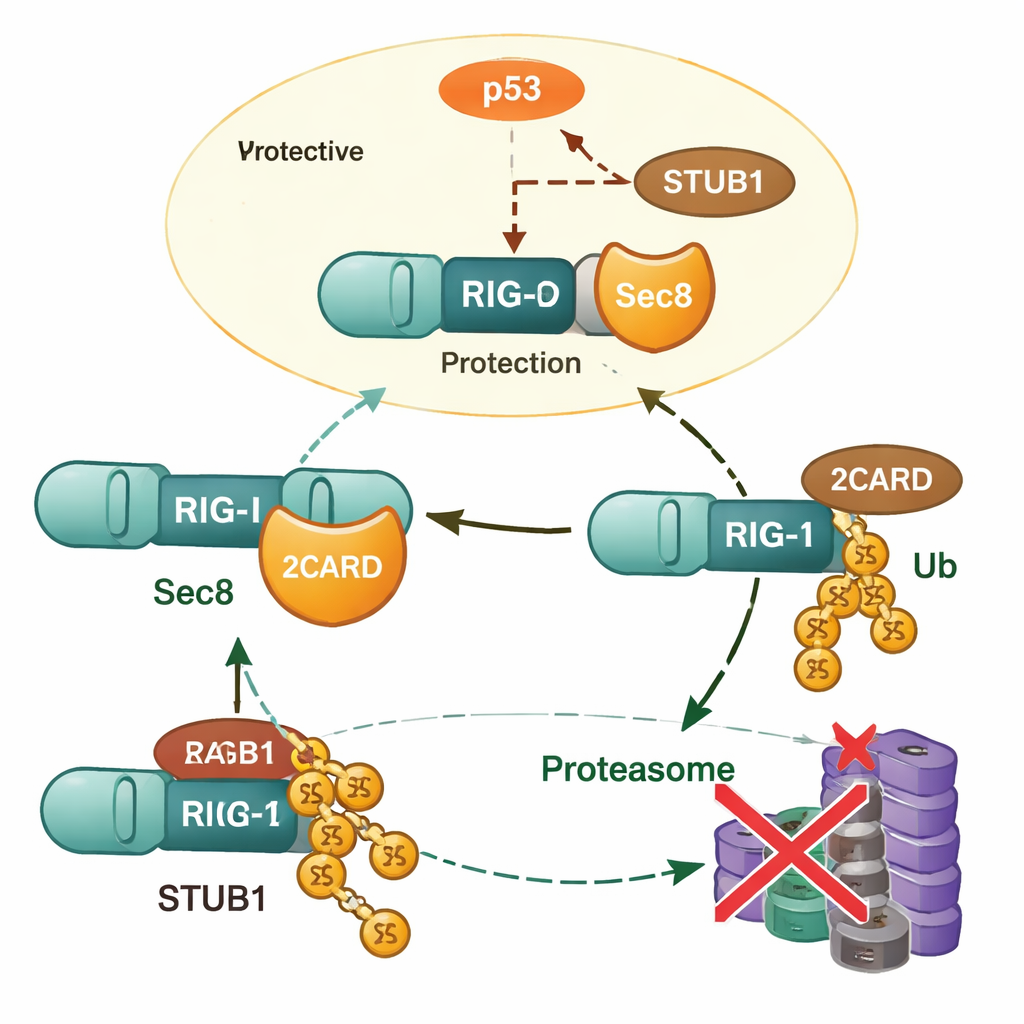
Daha derine inildiğinde araştırmacılar Sec8’in RIG‑I’nin gen ekspresyonunu artırmadığını; bunun yerine RIG‑I proteinini yok olmaktan koruduğunu buldular. Sec8 ortadan kaldırıldığında RIG‑I seviyeleri daha hızlı düştü ve bu kayıp, proteazomu bloke eden ilaçlarla önlenebiliyordu; bu da hücrenin protein geri dönüşüm mekanizmasını işaret ediyordu. Ekip, başka bir protein olan STUB1’i, K48‑bağlantılı belirli bir ubikitin zincirini RIG‑I’e lizine 190 olan bir amino asit üzerinde takan ana “etiketleyici” olarak tanımladı. Bu etiket RIG‑I’i yok edilmek üzere işaretliyor. Sec8 bu süreci iki yoldan bozuyor: RIG‑I’in aynı aktifleştirme bölgesine bağlanmak için STUB1 ile fiziksel olarak rekabet ediyor ve ayrıca hücrenin ürettiği STUB1 miktarını da azaltıyor.
Sec8, p53 ve Etiketleyicinin Kontrolü
Sec8’in STUB1 üretimini nasıl azalttığını açıklamak için yazarlar gen düzenlemesine yöneldiler. STUB1 geninin çekirdek açma anahtarını (promotor) oluşturan kısa bir DNA dizisini belirlediler ve ünlü tümör baskılayıcı protein p53’ün bu bölgeye bağlanıp STUB1 seviyelerini yükselttiğini gösterdiler. Sec8, p53’ün hem miktarını hem de aktifleştirici fosforilasyonunu azaltıyor, böylece p53 artık STUB1 üretimini etkili biçimde tetikleyemiyor. p53 bloke edildiğinde veya STUB1 susturulduğunda, Sec8 kaybının interferon üretimi ve viral büyüme üzerindeki zararlı etkileri büyük ölçüde geri döndü. Bu, Sec8’i p53’ten STUB1’e ve nihayetinde RIG‑I kararlılığına uzanan düzenleyici zincirin tepesine yerleştiriyor.
Petri Kabından Canlı Organizmalara
Araştırma ekibi daha sonra Sec8 geninden belirli bağışıklık hücrelerinde yoksun olacak şekilde tasarlanmış farelerde Sec8’in önemini test etti. VSV ile enfekte edildikten sonra bu hayvanlar daha az interferon üretti, dalak, karaciğer ve akciğer gibi organlarda daha yüksek viral yük taşıdı ve kontrol farelerine göre daha kötü akciğer hasarı, daha fazla kilo kaybı ve daha düşük hayatta kalma gösterdi. Bu in vivo sonuçlar, Sec8’in önemsiz bir oyuncu değil, tüm organizmada RNA virüs enfeksiyonuna karşı kayda değer bir koruyucu olduğunu doğruladı.
Gelecek Tedaviler İçin Neden Önemli
Basitçe ifade etmek gerekirse, bu çalışma Sec8’in antiviral sensör RIG‑I için bir koruma görevi gördüğünü gösteriyor. Etiketleyici protein STUB1’i kontrol altında tutarak ve doğrudan RIG‑I’i hücresel parçalaycıya gönderilmekten koruyarak Sec8, hücrelerin zamanında bir interferon yanıtı oluşturmasına ve RNA virüslerini daha iyi kontrol etmesine olanak tanır. Yeni tanımlanan p53–STUB1–RIG‑I ekseninin anlaşılması, RIG‑I’i stabilize eden veya Sec8’in koruyucu işlevlerini taklit eden gelecek antiviral stratejilerinin yolunu açabilir ve bu da RNA kaynaklı geniş bir virüs yelpazesine karşı savunmamızı güçlendirebilir.
Atıf: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Anahtar kelimeler: doğal bağışıklık, RNA virüsleri, RIG-I, ubikitinleme, interferon sinyallemesi