Clear Sky Science · tr
Metabolizmanın ötesi: kanserde laktat ve laktilasyonun düzenleyici ve terapötik etkilerini keşfetmek
Şekerden çıkan bir “atık ürün”ün kanser için neden önemi var
On yıllar boyunca, aşırı çalışan kasların yanmasına neden olan madde laktat hücresel çöp olarak görülüyordu. Bu derleme makale, kanserde laktatın asla atık olmadığını gösteriyor. Laktat yakıt, kimyasal bir sinyal ve hatta tümör hücrelerinin yaşayıp yaşamayacağına karar verebilen bir anahtar görevi görüyor. Bu gizli rolü anlamak, sağlıklı dokuları korurken kanser hücrelerinin kendi kendini yok etmesini sağlayacak yeni yollar açabilir.
Kanser hücrelerini yeniden kablolayan şeker kestirmesi
Kanser hücreleri “tatlı dişleri” ile kötü şöhrete sahiptir. Oksijen bol olsa bile, glikozu mitokondrilerde tam olarak yakmak yerine onu hızla laktata dönüştürmeyi tercih ederler; bu değişim Warburg etkisi olarak bilinir. Bu strateji tümörlerin yüksek hızda enerji ve yapı taşları üretmesini sağlar. Ortaya çıkan laktat seli özel taşıyıcılar aracılığıyla dışarı pompalanır ve büyümeyi destekleyen, düşük oksijen ya da kemoterapi gibi strese uyum sağlamaya yardımcı olan asidik, besin açısından zengin bir tümör mikroçevresi oluşturur.
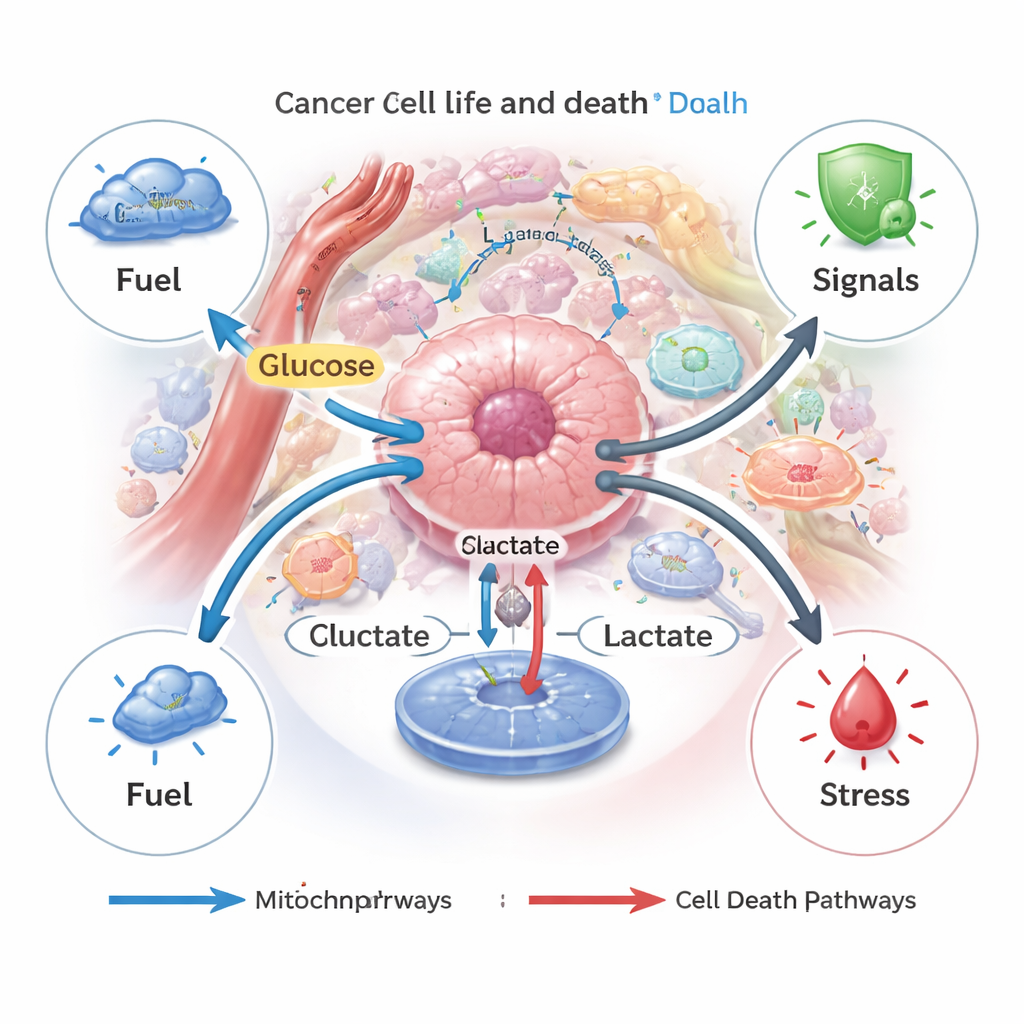
Laktat: farklı hücre ölümü türleri için bir düğme
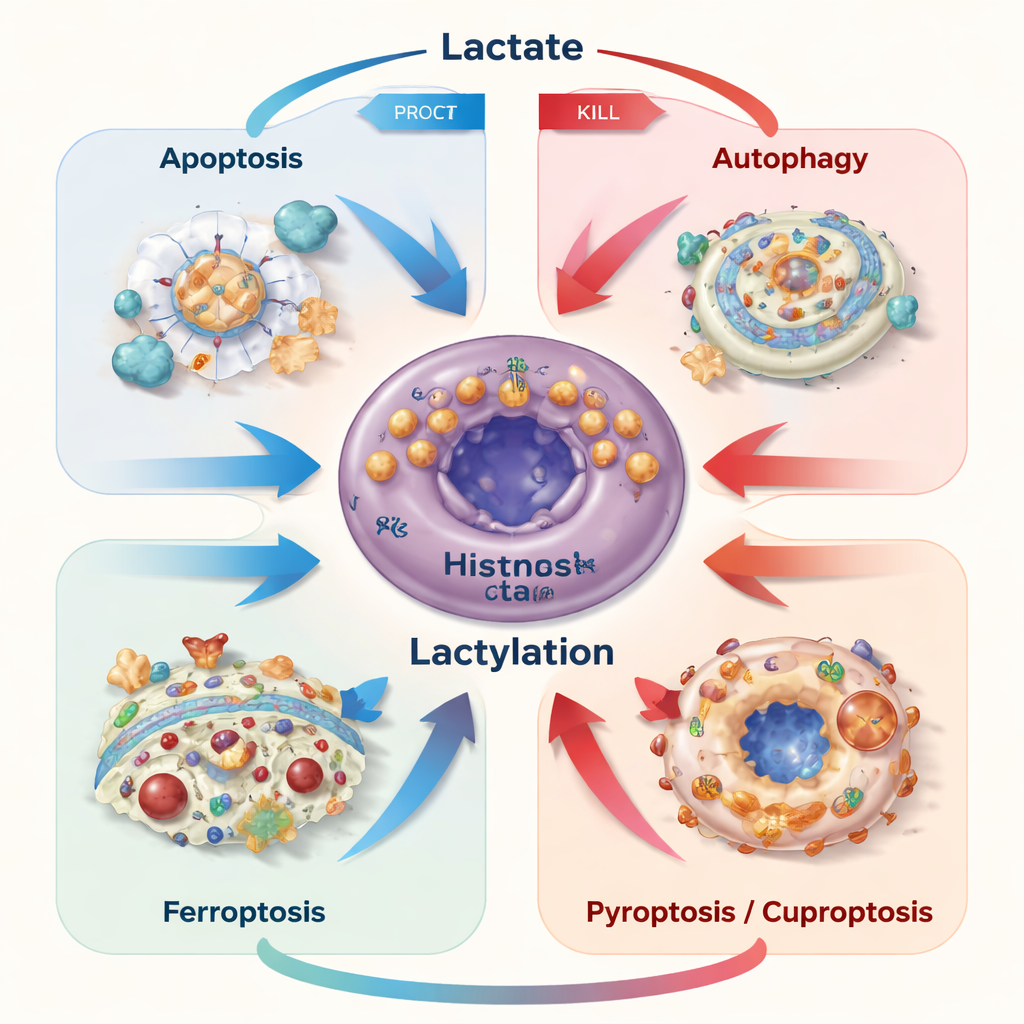
Vücudumuzdaki hücre ölümü genellikle sıkı bir şekilde kontrol edilir ve hasarlı veya tehlikeli hücrelerin uzaklaştırılmasına yardımcı olur. Kanser hücreleri genellikle bu programlardan kaçınır. Yazarlar, laktatın hem birkaç düzenlenmiş ölüm yolunu engelleyebildiğini hem de tetikleyebildiğini anlatıyor—apoptoz (hücre “intiharı”), otofaji (kendi kendini sindirme), ferroptoz (demir kaynaklı membran hasarı), piroptoz (iltihaplı patlama) ve kuportoz (bakır kaynaklı çöküş) gibi. Kanser hücreleri ılımlı miktarda laktat ürettiğinde veya içe aldığında bunu yakıt ve hayatta kalma sinyali olarak kullanma eğilimindedir; kemoterapi, besin yoksunluğu veya hedefe yönelik ilaçlardan koruyan yolları etkinleştirirler. Ancak laktat hücre içinde birikirse—örneğin ihracı bloke edilirse—oluşan asit stresi ve mitokondri hasarı anahtarı tersine çevirip hücreleri apoptoz veya ferroptoz yönünde itebilir.
Laktilasyon: laktat proteylere yazdığında
Son zamanlarda çarpıcı bir keşif, laktatın küçük bir kimyasal etikete dönüştürülüp proteinlerdeki lizin kalıntılarına eklenebilmesi; bu değişiklik laktilasyon olarak bilinir. Enzimler bu etiketlerin “yazanları” ve “silicileri” olarak görev yapar; hem DNA ile ilişkili histonları hem de birçok diğer proteini süslerler. Bu işaretler hangi genlerin açıldığını, enzimlerin nasıl davrandığını ve temel düzenleyicilerin ne kadar kararlı olduğunu değiştirir. Kanserde laktilasyon, hayatta kalma ile kendini yok etme arasındaki dengeyi ince ayarlar. Örneğin apoptozu engelleyen proteinleri artırabilir, otofaji aracılığıyla geri dönüşümü yükseltebilir, demir kontrolünü sıkılaştırıp antioksidanları artırarak hücreleri ferroptozdan koruyabilir veya hücrelerin bakır duyarlı proteinleri nasıl işlediğini değiştirerek kuportoz gibi yeni ölüm biçimlerini etkileyebilir.
Metabolizma ile ölüm programları arasında çift yönlü bir konuşma
İlişki tek yönlü değildir: hücre ölüm yolları da tümörlerin şekeri nasıl kullandığını ve laktat üretimini yeniden biçimlendirir. Erken apoptoz veya mitofaji (mitokondrilerin seçici olarak uzaklaştırılması) sırasında mitokondriler hasar gördüğünde hücreler genellikle hızlı glikolize geri döner ve laktat çıkışını artırır. Kanserle ilişkili fibroblastlar gibi çevredeki destek hücreleri benzer şekilde yeniden kablolanıp yakındaki tümör hücrelerini besleyen laktat fabrikalarına dönüşebilir. Ferroptoz gibi diğer ölüm türleri ise genellikle glikolizi baskılar ve dolayısıyla laktat düzeylerini düşürür. Sonuç, metabolizma ile ölüm mekanizmalarının tümör evrilirken ve tedaviye yanıt verirken sürekli olarak birbirine uyum sağladığı dinamik bir geri besleme döngüsüdür.
Zayıflığı bir tedavi stratejisine çevirme
Laktat ve laktilasyon bağlama göre ya kanser hücrelerini koruyabilir ya da öldürebileceğinden, yazarlar terapilerin sadece laktat üretimini engellemekten daha fazlasını yapması gerektiğini savunuyor. Bunun yerine gelecekteki tedaviler laktat akışlarını seçici olarak yönlendirebilir, taşıyıcılarını ayarlayabilir veya belirli laktilasyon işaretlerini hedefleyerek kanser hücrelerini kenara itip asidik ortam tarafından felç olmuş anti‑tümör bağışıklık hücrelerini yeniden enerjiyle doldurabilir. Lokal laktat veya pH seviyelerine yanıt veren akıllı ilaç taşıma sistemleri ve nanoterapötikler bu hassasiyeti uygulamanın yolları olarak ortaya çıkıyor. Basitçe ifade etmek gerekirse, makalenin mesajı bir zamanlar metabolik çöp gibi görünen şeyin aslında kanser hücresi kaderi üzerinde güçlü bir kontrol düğmesi olduğu—ve bu düğmeyi doğru şekilde çevirmeyi öğrenmenin mevcut tedavileri çok daha etkili kılabileceğidir.
Atıf: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Anahtar kelimeler: laktat, laktilasyon, kanser hücre ölümü, tümör metabolizması, ferroptoz