Clear Sky Science · tr
Kemik rejenerasyonunda HIF-1α ve BMAL1: hipoksi yanıtı ile sirkadiyen ritim arasındaki etkileşim
Kırık Kemikler Beklediğinizden Daha İyi Nasıl İyileşir
Bir kemiğimiz kırıldığında veya bir diş çekildiğinde, vücudumuz sessizce son derece iyi planlanmış bir onarım sürecini başlatır. Yaralanmış bölgenin derinlerinde oksijen düzeyi düşer ve içsel gündüz‑gece saatimiz işlemeye devam eder. Bu makale, düşük oksijonu algılayan HIF‑1α ile çekirdek saat proteini BMAL1 adlı iki anahtar unsurun iltihap, yeni doku oluşumu ve nihai mukavemetin geri kazanımı sırasında kemik hücrelerini nasıl birlikte yönlendirdiklerini inceliyor. Bu ortak çalışmanın anlaşılması; kırıklar, osteoporoz, artrit ve hatta diş implantları için tedavilerin iyileştirilmesine yardımcı olabilir.
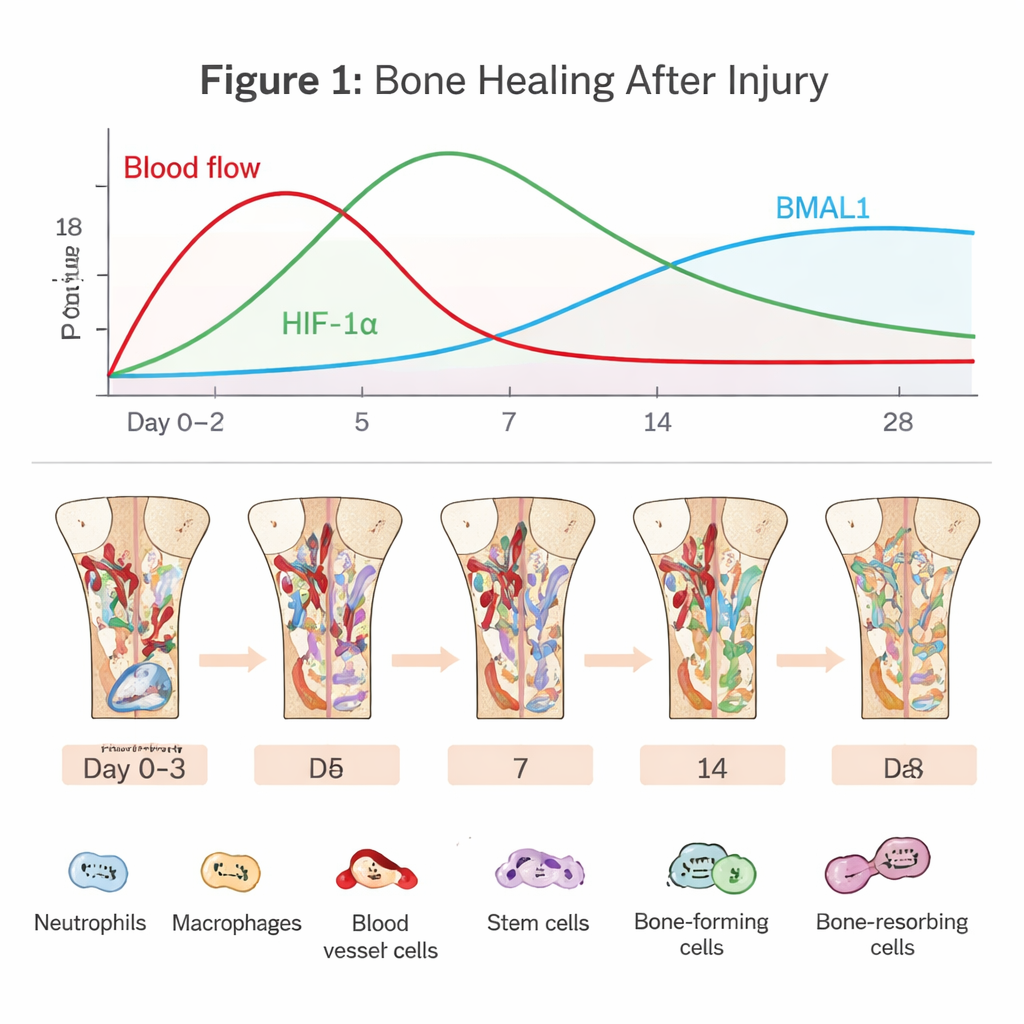
İyileşen Bir Kemin İçindeki Gizli Drama
Kemik rejenerasyonu kan damarları yırtıldığı anda başlar. Bir pıhtı oluşur, oksijen kaynağını büyük ölçüde kısıtlar ve zorlu, düşük‑oksijenli bir alan yaratır. Nötrofiller ve makrofajlar gibi bağışıklık hücreleri, artıkların temizlenmesi ve mikroplara karşı savunma için hızla bölgeye akın eder. Aynı zamanda kemik iliği kök hücreleri ve damar hücreleri bölgeyi yeniden inşa etmek üzere çağrılır. Bu erken “iltihap fazı” çift taraflıdır: kısa ve zamanında bir iltihap atılımı onarımı başlatırken, çok uzun sürerse veya aşırı olursa iyileşme duraksayabilir veya başarısız olabilir. Makale, bu dar yolun aşılmasının büyük ölçüde hücrelerin oksijeni ve zamanı nasıl algıladığına bağlı olduğunu vurgular.
Hücreler Düşük Oksijonu Nasıl Avantaja Çevirir
Oksijenin az olduğu kırık bölgesinde HIF‑1α proteini kararlı hale gelir ve hücrelerin uyum sağlamasına yardımcı olan genleri aktive eder. Endotelyal hücreleri yeni damarlar oluşturması için teşvik ederek taze oksijen ve besinlerin hasarlı bölgeye ulaşmasını sağlar. Ayrıca hücre metabolizmasını, oksijen az olsa bile enerji üretebilen glikolize kaydırır. Kök hücreler ve kemik oluşturan osteoblastlar için ılımlı HIF‑1α aktivasyonu çoğalmayı, göçü ve kemik büyümesini artırabilir; kısmen kan damarları oluşumunu yeni kemikle bağlayan VEGF gibi faktörleri yükseltmesiyle. Ancak hipoksi çok şiddetli veya uzun süreliyse stres molekülleri ve reaktif oksijen türleri birikir, osteoblastları ölüme sürükleyebilir ve kemik rezorbe eden osteoklastları uyarabilir. Bu nedenle aynı hipoksik sinyal, yoğunluğu ve süresine bağlı olarak iyileşmeyi ya destekleyebilir ya da sabote edebilir.
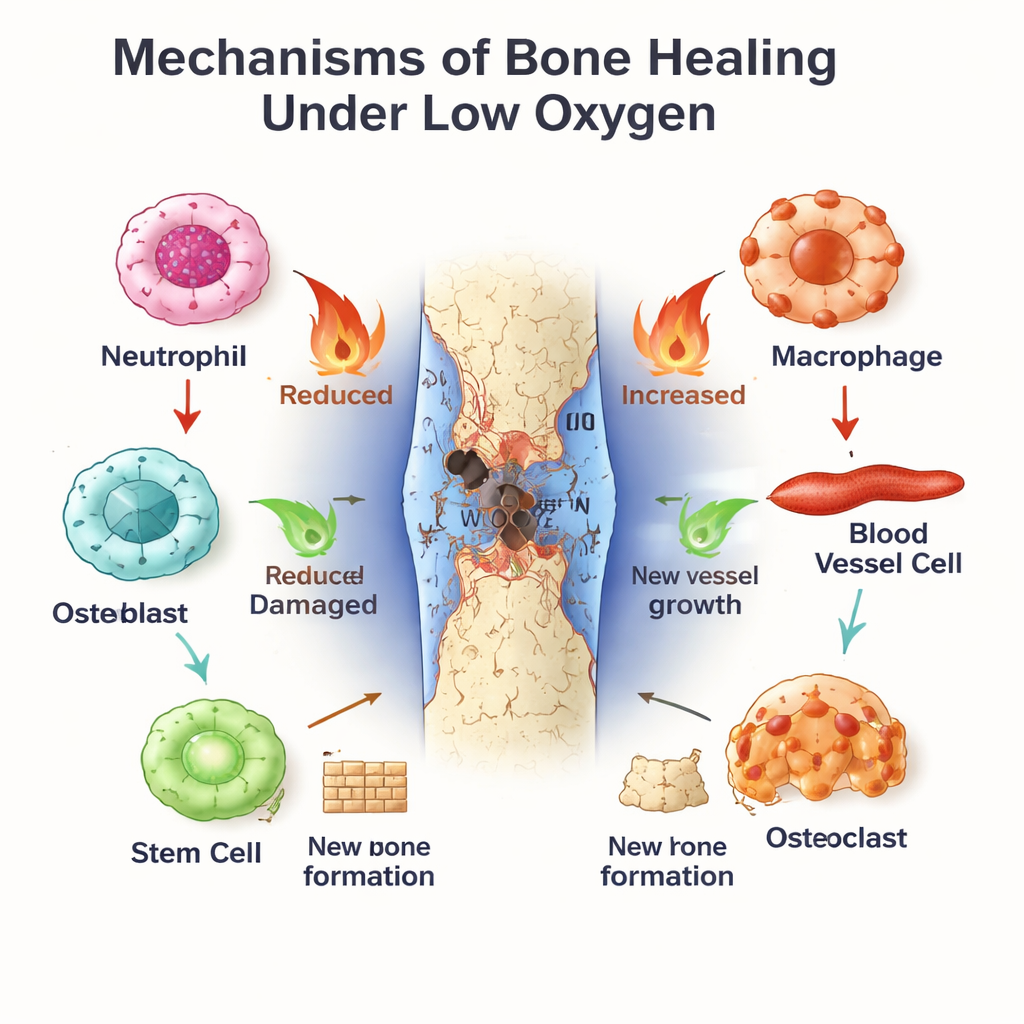
Vücudun İç Saati: Kemik Onarımının Yönetmeni
Eş zamanlı olarak işleyen sirkadiyen saat neredeyse her hücrede bulunan moleküler bir zaman tutucudur. Merkez bileşenlerden biri olan BMAL1, bağışıklık aktivitesinde, damar davranışında ve kök hücre farklılaşmasında günlük ritimleri belirlemeye yardımcı olur. Nötrofiller ve makrofajlar, yaralanmaya ne kadar güçlü yanıt verdikleri ve ne kadar hızlı yaşlandıkları ya da iltihaplı (M1 benzeri) durumdan iyileştirici (M2 benzeri) duruma geçtikleri açısından günün farklı zamanlarında farklılık gösterir. Damar hücrelerinde ve kemik iliği kök hücrelerinde BMAL1; Wnt ve TGF‑β/SMAD gibi büyüme yollarını ayarlayarak sağlıklı çoğalmayı ve düzenli kemik oluşumunu destekler. BMAL1 bozulduğunda—genetik defektler, vardiyalı çalışma veya metabolik hastalıklar nedeniyle—kemikler kitle kaybı yaşama eğilimindedir, kök hücreler tükenir ve kemik oluşumu ile yıkımı arasındaki denge kayba doğru kayar.
Oksijen Algılama ile Vücut Saatinin Konuşması
Derlemenin merkezinde HIF‑1α ile BMAL1 arasındaki ortaya çıkan “etkileşim” vardır. Bu iki protein benzer yapılar paylaşır ve fiziksel olarak etkileşime girerek DNA’ya bağlanan ve örtüşen gen setlerini kontrol eden karışık çiftler oluşturabilirler. Her biri diğerinin üretimini ve stabilitesini etkileyebilir, böylece gündüz‑gece döngüsünün zamanlamasını hücrelerin hipoksiye yanıt verme biçimine bağlayan geri besleme döngüleri oluşur. Birlikte hücresel redoks dengesini—zararlı reaktif oksijen türlerinin oluşumu ile antioksidan kapasitenin ne kadar olduğu arasındaki dengeyi—yönetirler ve hücrelerin oksijen bağımlı solunuma mı yoksa oksijensiz glikolize mi daha çok güveneceğine karar veren kritik enzimleri ortak düzenlerler. Bu ortak kontrol, kırık ortamının yapıcı yeniden inşayı mı yoksa aşırı iltihap ve kemik rezorpsiyonunu mu destekleyeceğini belirlemeye yardımcı olur.
Bu Hastalık ve Tedavi İçin Ne Anlama Geliyor
Aynı HIF‑1α–BMAL1 ortaklığı birçok kemikle ilişkili durumda gözlemlenir. Vardiya çalışanlarında bozulmuş uyku ve ışığa maruziyet muhtemelen BMAL1’i değiştirir, oksidatif stresi artırır ve HIF‑1α tarafından yönlendirilen onarımı engelleyerek osteoporoza katkıda bulunur. Diyabette yüksek kan şekeri hem saat fonksiyonunu hem de hipoksi sinyalini zayıflatır, damar büyümesini ve kök hücre kaynaklı kemik oluşumunu baltalar. Osteoartritte kondrositlerde BMAL1 kaybı ritimlerini ve HIF‑1α ile koruyucu ilişkilerini bozar, kıkırdak bozulmasını hızlandırır. Titanyum implantların çevresinde kontrollü hipoksi ve sağlıklı bir sirkadiyen ritim daha iyi osseointegrasyonu destekliyormuş gibi görünmekte; bu da gelecekteki implant kaplamalarının hem HIF‑1α’yı hem de BMAL1’i nazikçe aktive edecek şekilde tasarlanabileceğini düşündürmektedir. Genel olarak makale, başarılı kemik rejenerasyonunun sadece hangi hücrelerin bulunduğuna değil, bu hücrelerin oksijeni ve zamanı nasıl okuduğuna da bağlı olduğunu ve bu diyalogu hedeflemenin daha hızlı, daha güçlü iyileşme için yeni yollar açabileceğini sonucuna varmaktadır.
Atıf: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Anahtar kelimeler: kemik rejenerasyonu, sirkadiyen ritim, hipoksi, osteoporoz, kırık iyileşmesi