Clear Sky Science · tr
GABAerjik interneuronların disfonksiyonu, PPT1 eksikliğine bağlı farelerde epileptiform aktiviteyle ilişkili değişmiş nöral ağ salınımlarının temelini oluşturur
Beyin Ritmleri Bozulduğunda
Nöbetler sadece ani beyin aktivite fırtınaları değildir; sıklıkla nöronların birbirleriyle iletişim kurma biçimlerindeki ince değişikliklerden gelişirler. Bu çalışma nadir bir çocukluk beyin bozukluğu olan CLN1 hastalığını inceliyor ve etkisi geniş sonuçlar doğuran basit bir soruyu soruyor: PPT1 adı verilen tek bir enzim eksik olduğunda beynin iç “ritim düzenleyicilerinde” ne olur? Araştırmacılar fareleri zaman içinde izleyerek, inhibisyondaki küçük erken kusurların nasıl nöbetlere ve yaygın beyin hasarına dönüşebileceğini ortaya koyuyor.
Beyin Dengesinin Bekçileri
Beynimiz iki geniş nöron türüne dayanır. Hipokampüsteki piramidal nöronlar gibi eksitatör hücreler aktiviteyi ilerletir. İnhibisyonu sağlayan interneuronlar ise fren gibi davranarak bu aktiviteyi kontrol eder ve beynin elektriksel ritimlerini şekillendirir. Bunlar arasında parvalbumin-pozitif (PV+) interneuronlar ve somatostatin-pozitif (SST+) interneuronlar iki önemli gruptur. Theta ve gamma gibi ritmik beyin dalgalarını üretmeye ve koordine etmeye yardımcı olurlar; bu dalgalar öğrenme ve hafıza gibi işlevleri destekler. CLN1 hastalığında çocuklar, normalde proteinlerden yağ gruplarını kaldıran PPT1 enzimini kaybeder. Yazarlar, hastalarda görülen aynı mutasyona sahip bir fare modeli kullanarak bu kaybın interneuronları ve onların kontrol ettiği beyin ritimlerini nasıl etkilediğini incelediler.
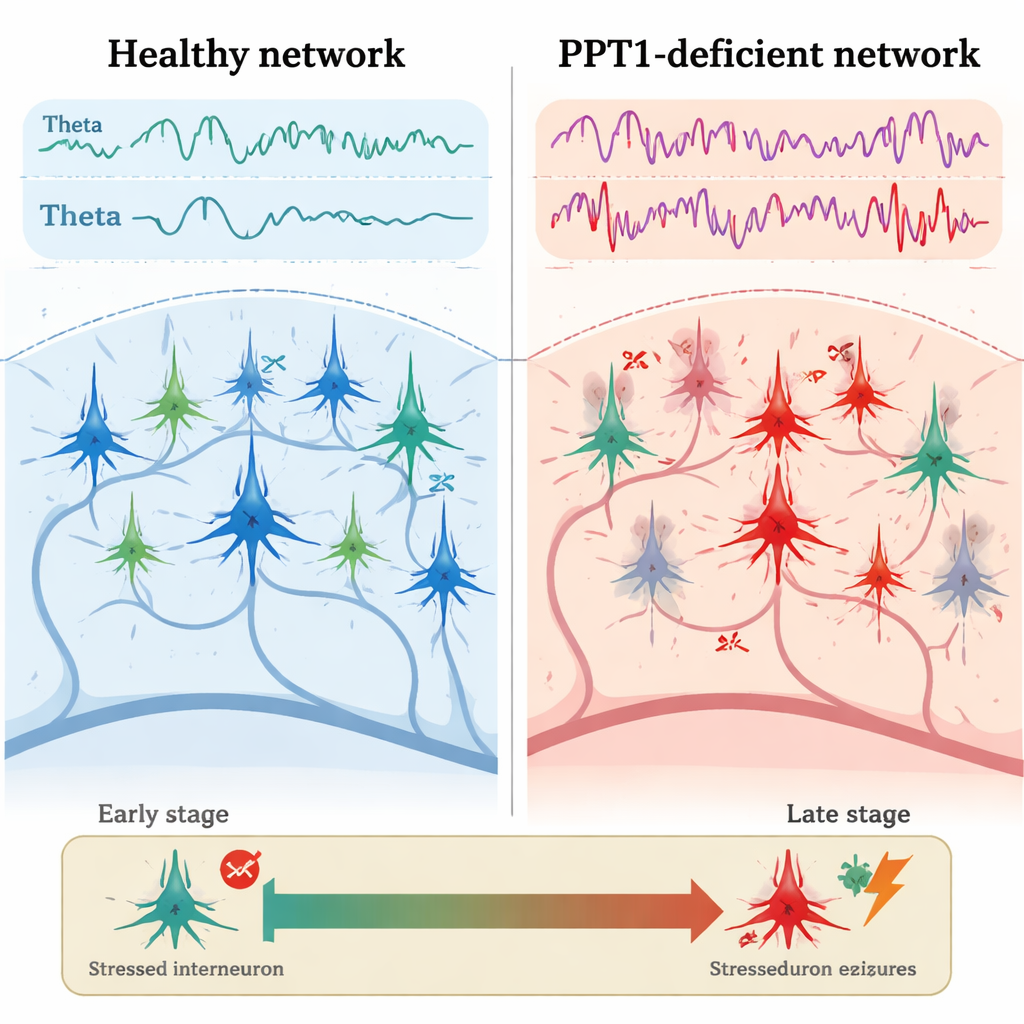
İnhibitör Sistemde Erken Çatlaklar
Yaklaşık üç-dört aylık genç yetişkin mutant farelerde ilk belirgin sorun PV+ interneuronlarda ortaya çıktı. Hipokampüsten yapılan elektrofizyolojik kayıtlar, bu inhibitör hücrelerin sağlıklı farelere göre daha az ateşlendiğini gösterirken, yakınlardaki piramidal nöronlar daha hızlı ve spike’lar arasındaki duraklamalar daha kısa olacak şekilde ateşlendiler. Mikroskopi, birçok PV+ interneuronda programlı hücre ölümünün ana yürütücülerinden biri olan kaspaz-3 aktivasyonunun bulunduğunu ortaya koydu; buna karşın toplam hücre sayıları henüz azalmamıştı. Aynı zamanda theta ve gamma dalgalarının gücü artmıştı ve kalsiyum görüntüleme, hayvanlar hareket ederken hipokampal nöronlarda daha güçlü aktivite gösterdi. Kritik olarak, daha yavaş dalgaların daha hızlı olanları organize etmesine dayanan normal theta–gamma “çapraz-konuşması” zayıflamıştı; bu da ağ aktivitesinin hassas zamanlamasında erken bir bozulmaya işaret ediyordu.
Bozulmuş Ritmlerden Nöbet Patlamalarına
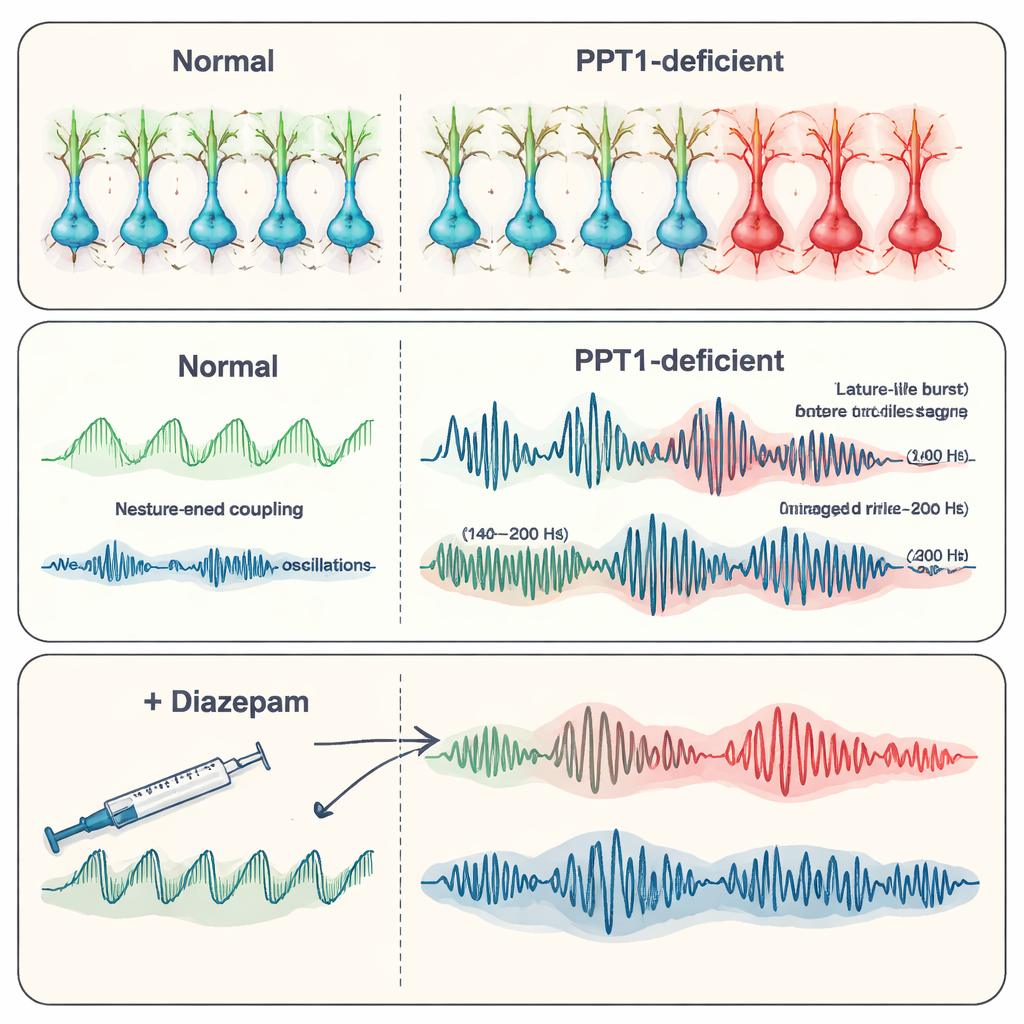
Altı-yedi aylık olduğunda tablo daha da kötüleşti. Birçok PV+ interneuron kaybolmuştu ve artık SST+ interneuronlarda da kaspaz-3 aktivasyonu belirtileri görülüyordu. Hipokampüsten yapılan kayıtlar spontan epileptiform deşarjları—nöbetlerle ilişkili kısa, anormal aktivite patlamalarını—gösterdi. Ekip, normalde hafıza depolamaya yardımcı olan hızlı osilasyonlar olan yüksek frekanslı “ripple”lara odaklandı. Mutant farelerde fizyolojik ripple’lar (yaklaşık 140–200 hertz) daha seyrek fakat amplitüd olarak daha büyük hale gelirken, epilepsiyle sıkı ilişki gösteren daha hızlı “patolojik” ripple’lar (200–500 hertz) güçlenmiş ve daha yaygın hale gelmişti. Bu değişimler birlikte, inhibitör kontrol başarısız oldukça düzenli, hafıza ile ilgili ritimlerden kaotik, nöbet eğilimli desenlere doğru bir kaymaya işaret ediyordu.
Nöronlar Yıpranıyor ve Diazepam Müdahale Ediyor
Hastalık ilerledikçe hipokampüsün kendisi dejenerasyona uğramaya başladı. Nöronlardaki kalsiyum sinyalleri azaldı, Golgi boya ile dendritik ağaçlar daha ince ve daha az dallanmış olarak görüldü ve sinapsların oluştuğu küçük dikenciklerin sayısı azaldı. CA1 ve CA3 gibi kilit hipokampal bölgelerdeki nöron sayımları yaygın hücre kaybını doğruladı ve elektrik kayıtlarında daha az aktif ünite tespit edilebildi. Araştırmacılar sonra GABA inhibitör kimyasının etkisini güçlendiren yaygın bir anti-nöbet ilacı olan diazepamı test ettiler. Daha yaşlı mutant farelerde diazepam, epileptik deşarjların sıklığını azalttı ve alttaki reseptör kaybını onarmasa da ripple davranışı dahil daha normal osilatuar desenleri kısmen geri getirdi. Bu, kalan inhibe edici sinyalleri güçlendirmenin ağılı en azından geçici olarak yatıştırabileceğini öne sürüyor.
Bu Bulgular Neden Önemli
Herkes için özet mesaj şudur: CLN1 hastalığı sadece hücrelerde biriken atığın bir sorunu değildir. PPT1 kaybı bir zincirleme reaksiyon başlatır: önce uzmanlaşmış inhibitör interneuronlar stres altına girer ve başarısız olmaya başlar, bu da aşırı aktif piramidal nöronları serbest bırakır ve beynin ritimlerini bozar. Zamanla bu dengesizlik nöbetlere ve nihayetinde geniş çaplı hücre ve bağlantı kaybına yol açar. Çalışma, hastalığın erken döneminde bir fırsat penceresine işaret ediyor: PV+ interneuronları korumak veya kurtarmak—örneğin kaspaz aktivasyonunu engelleyerek—ilerideki nöbetleri ve dejenerasyonu önleyebilir. Diazepam CLN1’i tedavi edemese de, bu modelde anormal ritimleri baskılama yeteneği, inhibisyonun yeniden sağlanmasının epilepsi ve ilişkili beyin bozukluklarında güçlü bir strateji olabileceği fikrini destekliyor.
Atıf: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
Anahtar kelimeler: epilepsi, internöronlar, hipokampüs, beyin salınımları, lizozomal depo hastalığı