Clear Sky Science · tr
Otozomal Dominant Alzheimer hastalığı mutasyonlarına sahip İsveçli ailelerde erken fonksiyonel değişiklikler ve plazma GFAP
Bu çalışma aileler için neden önemli
Alzheimer hastalığı çoğu zaman aniden ortaya çıkıyormuş gibi hissedilir, oysa gerçekte zararlı beyin değişiklikleri yıllarca sessizce birikir. Kalıtsal ("otozomal dominant") Alzheimer mutasyonlarını taşıyan nadir ailelerde, bilim insanları semptomların ne zaman başlamasının muhtemel olduğunu tahmin edebilir ve bu erken değişiklikleri izleyebilir. Bu çalışma, böyle mutasyonlara sahip İsveçli aileleri takip ederek, bellek sorunları ortaya çıkmadan çok önce beyin enerji kullanımı, düşünme yetenekleri ve beyin destek hücrelerinin (GFAP) kan işaretçisinin nasıl değiştiğini ve bu değişimlerin genlere göre nasıl farklılık gösterdiğini anlamayı amaçladı.
Yüksek riskli ailelerde hastalık saatini takip etmek
Otozomal dominant Alzheimer hastalığı (ADAD) taşıyanlarda semptomların genellikle öngörülebilir bir yaşta ortaya çıkması nedeniyle araştırmacılar "tahmini semptom başlangıcına yıllar"ı (EYO) hesaplayabiliyor—bir kişinin beklenen ilk hastalık belirtilerine kaç yıl kala veya kaç yıl sonra olduğu. Araştırma ekibi APP veya PSEN1 gen mutasyonlarına sahip İsveçli ailelerden 45 yetişkini ve ayrıca mutasyonu olmayan akrabalarını inceledi. Ortalama yedi yılı aşkın bir süre boyunca katılımcılara beynin ne kadar şeker kullandığını ölçen beyin taramaları (FDG PET), ayrıntılı düşünme ve hafıza testleri ve bir alt grupta astrositler reaktif olduğunda salınan bir protein olan GFAP için kan testleri uygulandı. Bu tasarım, bilim insanlarının farklı biyolojik değişiklikleri tek bir zaman kesitinde karşılaştırmaktansa paylaşılan bir hastalık zaman çizelgesine göre sıralamasına olanak tanıdı.
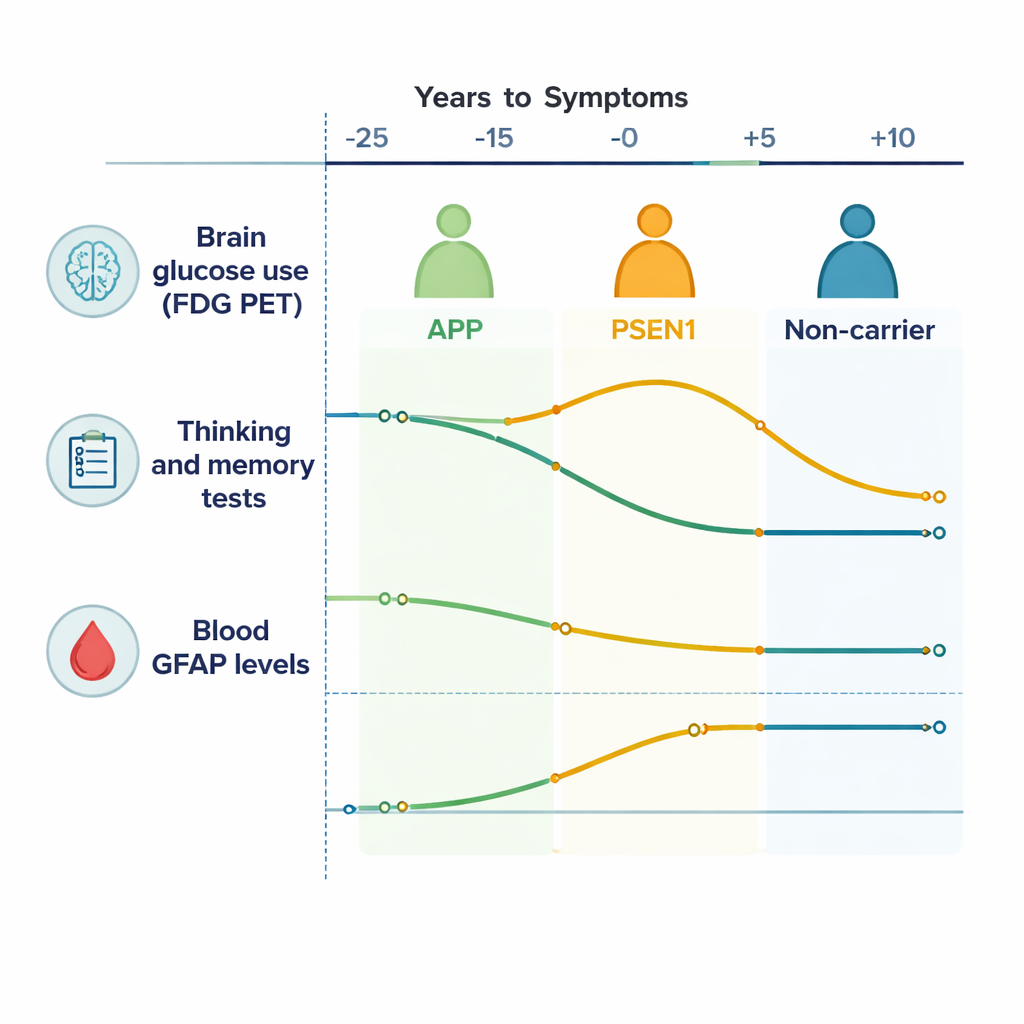
Zaman içinde beyin enerjisi ve düşüncenin izlenmesi
Beynin dış katmanları (korteks) genelinde Alzheimer mutasyonu taşıyan kişiler, mutasyonu olmayan aile üyelerine göre FDG PET sinyalinde kademeli bir düşüş gösterdi; bu da beyinlerinin zamanla daha az şeker kullandığını, yani beyin hücrelerinin işlevinin zayıfladığını gösteriyor. Kaudat ve talamus gibi beynin derinindeki subkortikal bölgeler de özellikle APP mutasyonluları tarafından yönlendirilerek aktivite azalması gösterdi. Episodik bellek ve zihinsel esneklik dahil olmak üzere bir dizi alanda düşünme ve hafıza testleri beklenen semptom başlangıcından yaklaşık 10–15 yıl önce kötüleşmeye başladı. Başka bir deyişle, kişiler günlük yaşamda hâlâ normal hissetse ve işlev görse bile duyarlı testler ve taramalar beyinlerinin zaten daha fazla çalıştığını ve daha verimsiz hale geldiğini ortaya koydu.
Farklı Alzheimer genleri için farklı desenler
Öne çıkan bir bulgu, iki ana mutasyon grubunun—APP ve PSEN1—aynı yolları izlemediğiydi. PSEN1 taşıyıcılarında, araştırmacılar beklenen semptom öncesi yaklaşık 20–10 yıllık erken bir dönemde beynin bazı bölgelerinde alışılmadık derecede yüksek şeker kullanımı ("hipermetabolizma") ve daha iyi test performansı gözlemledi; bunun ardından daha sonra düşüş oldu. Bu muhtemelen beyin ve destek hücrelerinin, artan hasarla başa çıkmak için aktiviteyi geçici olarak artırdığı bir telafi aşamasını yansıtıyor. Buna karşılık APP taşıyıcıları bu erken sıçramayı göstermeyip daha doğrudan, kademeli bir metabolizma düşüşü sergiledi. Bu gene özgü desenler, kalıtsal formlarda bile "Alzheimer hastalığı"nın tek bir biyolojik hikâye olmadığını, altta yatan mutasyona bağlı olarak farklı şekilde gelişen ilişkili süreçler ailesi olduğunu öne sürüyor.
Bir kan testi erken beyin stresini ne gösteriyor
Basit bir kan örneğinden ölçülen GFAP, astrositlerin erken Alzheimer değişikliklerine nasıl yanıt verdiğine dair bir pencere sundu. GFAP düzeyleri hem mutasyon taşıyıcılarında hem de taşımayanlarda beklenen semptom yaşına yaklaşırken genelde kararlı bir artış eğilimi gösterdi, ancak GFAP, beyin metabolizması ve biliş arasındaki ilişkiler gene özgüydü. APP taşıyıcılarında daha yüksek GFAP, derin beyin bölgelerindeki düşen şeker kullanımı ve çoğu bilişsel testte kötüleşme ile ilişkilendi; bu da astrosit aktivasyonunun erken hasar ve fonksiyon kaybıyla yakından bağlantılı olduğunu düşündürüyor. PSEN1 taşıyıcılarında bu bağlantılar daha zayıf veya yoktu; bu da aynı klinik bunama son noktasına ulaşan farklı biyolojik yolları işaret ediyor.
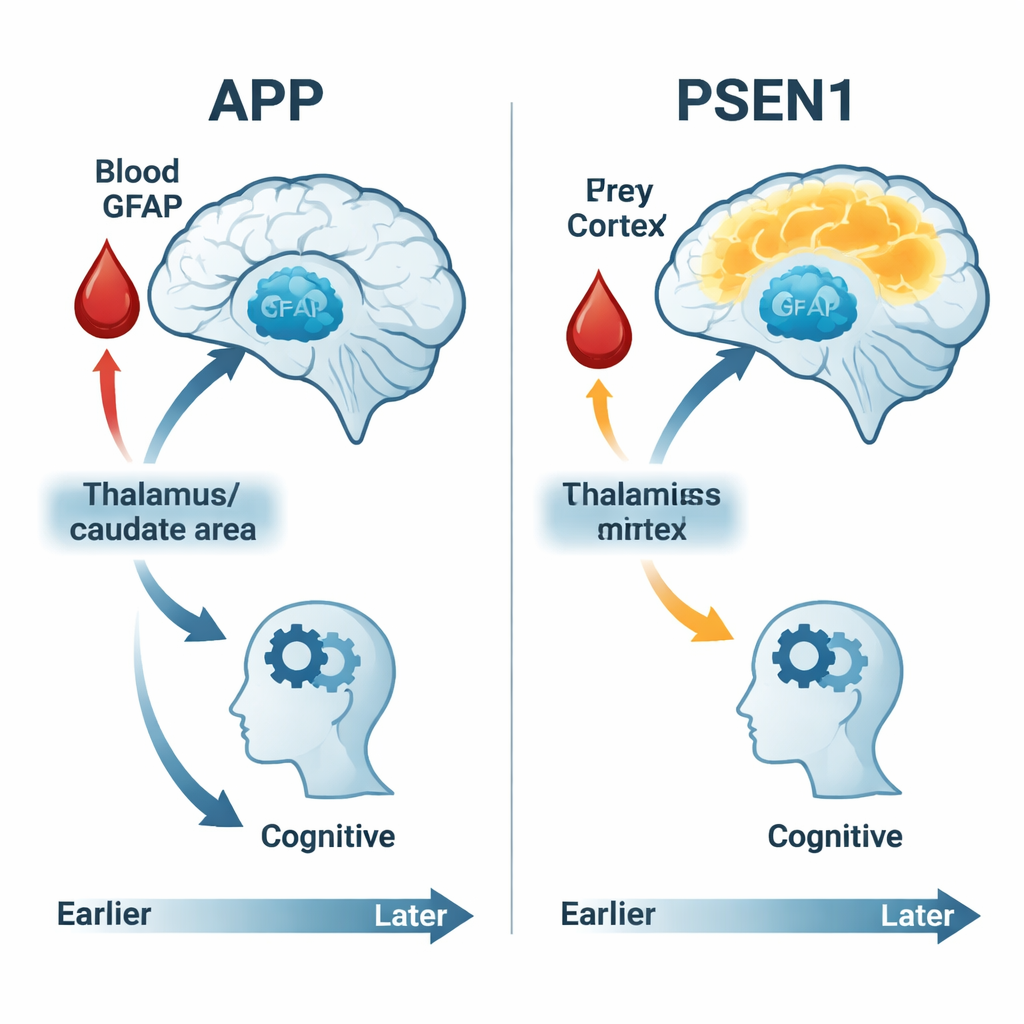
Erken tespit ve tedavi için ne anlama geliyor
Bir okuyucu için temel mesaj şudur: bu yüksek riskli ailelerde Alzheimer ile ilişkili değişiklikler belirgin bellek kaybından onlarca yıl önce başlıyor—ve herkes için aynı görünmüyor. Beynin şeker kullanımını gösteren taramalar, ince ayrıntılı bilişsel testler ve GFAP gibi tek bir kan biyobelirteci birlikte beynin ne zaman zorlanmaya başladığını ve bu zorluğun ne kadar hızlı ilerlediğini açığa çıkarabilir. Önemli olarak, farklı genetik Alzheimer formlarına sahip kişiler farklı değişim dizileri sergiliyor: bazıları erken bir aşırı aktif dönem geçiriyor, bazıları ise düzenli bir düşüş gösteriyor ve astrosit stresinin kan belirteci bazı gruplarda hasarla diğerlerine göre daha güçlü ilişki kuruyor. Bu ayrımları tanımak, gelecekteki ilaçların ve klinik çalışmaların doğru kişilere doğru zamanda yönlendirilmesine yardımcı olabilir ve semptomlar insanların bağımsızlığını elinden almadan Alzheimer’ı daha erken yakalamak için GFAP gibi kan testlerinin vaatlerini destekler.
Atıf: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Anahtar kelimeler: otozomal dominant Alzheimer hastalığı, GFAP kan biyobelirteci, beyin glukoz metabolizması, astrositler ve nörodejenerasyon, erken Alzheimer tespiti