Clear Sky Science · tr
Sindin18.2-spesifik IL-7/XCL1 zırhlı CAR-T hücrelerinin sindirim sistemi kanserlerindeki etkinliği ve immünomodülatör etkisi: preklinik ve klinik analiz
Bağışıklık Sistemi Sindirim Kanserlerine Karşı Döndürüyor
Mide ve pankreas kanserleri, kısmen cerrahi, kemoterapi ve radyasyona sıkça direnç göstermeleri nedeniyle en ölümcül tümörler arasındadır. Bu çalışma, vücudun kendi bağışıklık hücrelerini güçlendirerek katı tümörlere girmelerini, orada hayatta kalmalarını ve takviye kuvvet çağırmalarını sağlayan yeni bir yaklaşıma odaklanıyor. Kanserle savaşan T hücrelerini yardımcı bağışıklık sinyalleri salgılayacak şekilde yeniden tasarlayarak araştırmacılar, tümörlere doğrudan saldırmanın ötesinde, kanserin düşmanca ortamı içinde kalan diğer bağışıklık bileşenlerini de uyandırmayı amaçlıyorlar.
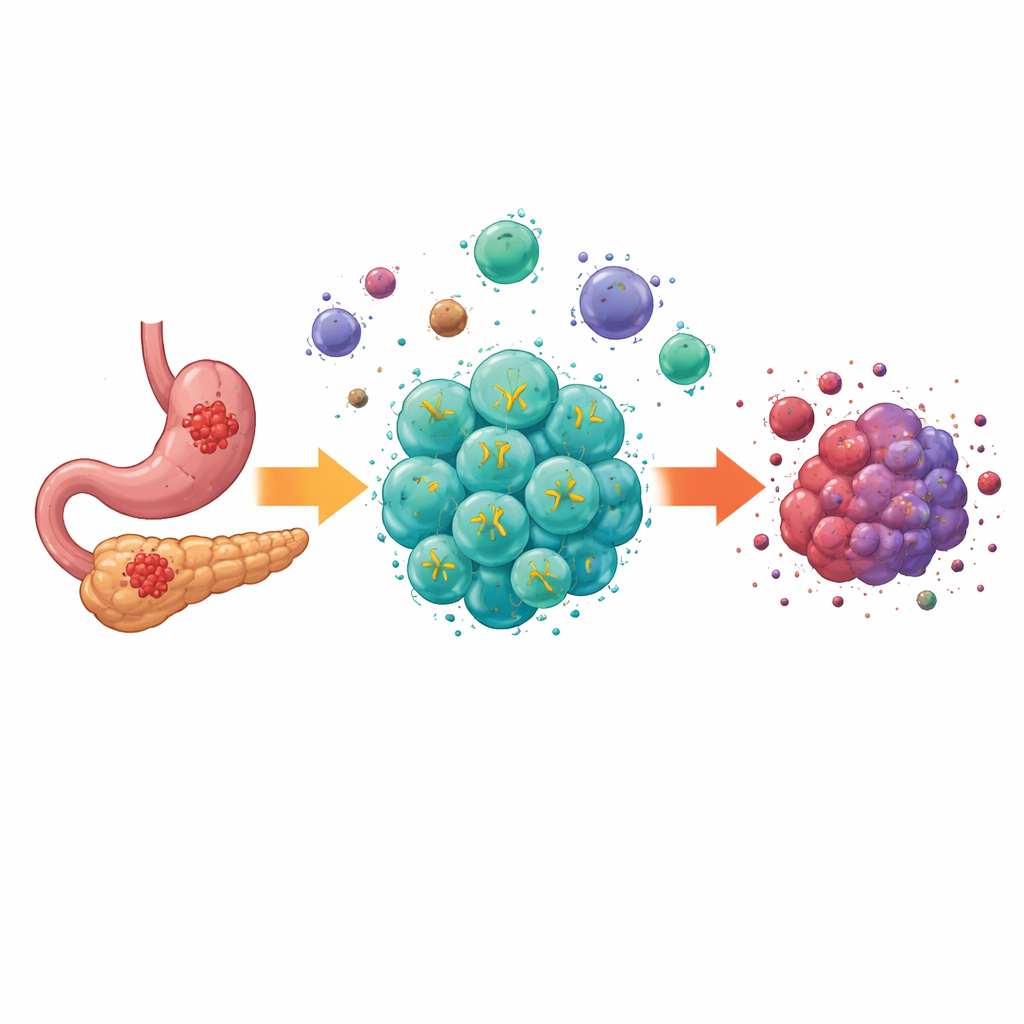
Katı Tümörlerin Tedavisinin Neden Zor Olduğu
Klasik CAR-T hücreleri kan kanserlerinde çarpıcı sonuçlar verdi ve başka seçeneği olmayan bazı hastaları tedavi etti. Ancak sindirim sistemi gibi katı tümörler ek zorluklar getirir. Bu tümörlerde hücreler bölgeden bölgeye değişir, tümör içi besin ve oksijen yetersizdir ve baskılayıcı hücrelerle sinyal moleküllerinin karışımı bağışıklık saldırılarını azaltır. Daha önceki nesil CAR-T hücreleri sindirim kanseri hücrelerindeki hedef molekülleri tanıyabilse de, genellikle bu zorlu ortamda çoğalamamış, uzun süre kalamamış ve işlevlerini sürdürememiş, bu da gerçek dünyadaki etkilerini kısıtlamıştır.
Mühendislikli T Hücreleri İçin Daha Akıllı Bir Tasarım
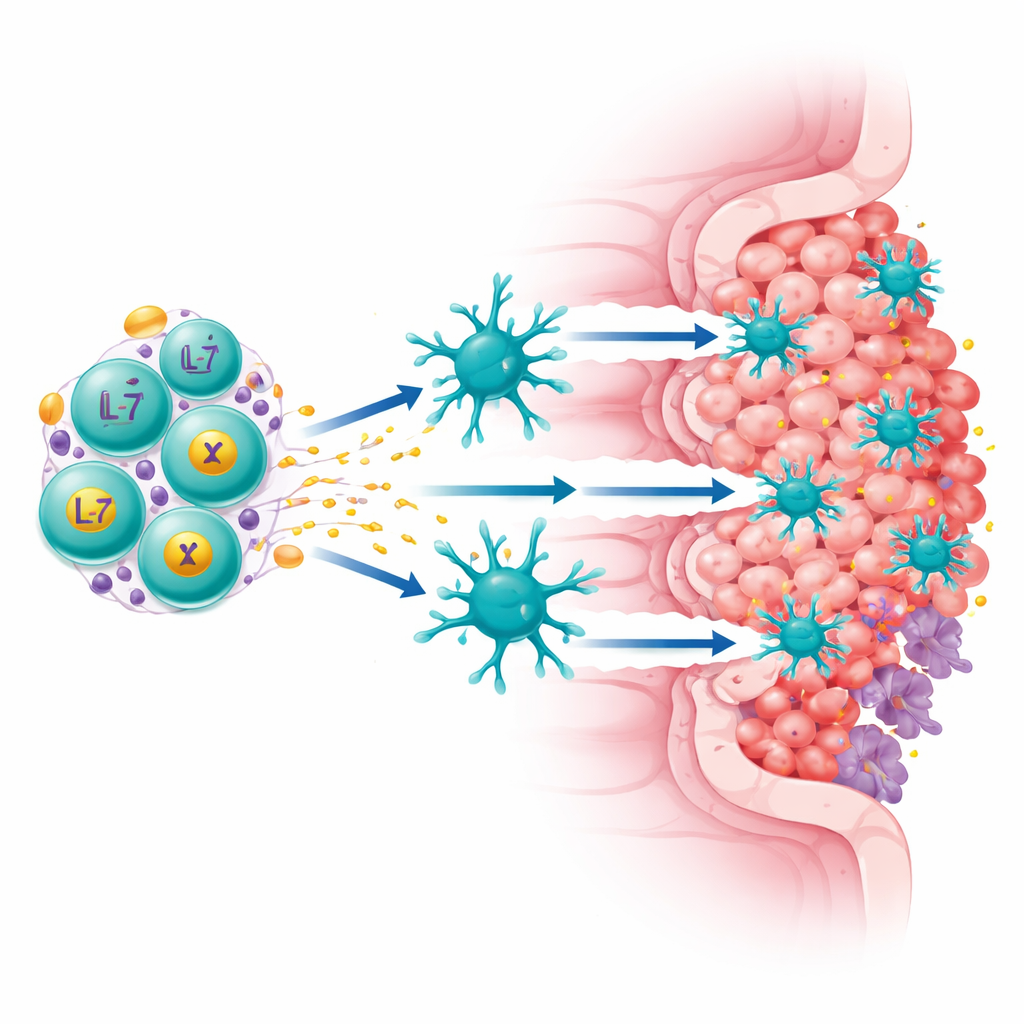
Araştırma ekibi, birçok mide ve pankreas kanseri hücresinde yüksek düzeyde bulunan ancak normal dokularda büyük ölçüde yok olan Claudin18.2 adlı proteine odaklandı. Onlar, iki işi aynı anda yapan “dördüncü nesil” bir CAR-T hücresi tasarladı: tümör hücrelerindeki Claudin18.2’yi tanımak ve sürekli olarak iki bağışıklık güçlendirici faktör, IL-7 ve XCL1 salgılamak. IL-7 T hücrelerinin hayatta kalmasına ve uzun ömürlü, kök-benzeri bir durumda kalmalarına yardımcı olurken, XCL1 nadir ama güçlü bir bağışıklık hüceti türü olan cDC1’i çekici bir işaret gibi işe yarar; cDC1 öldürücü T hücrelerini etkinleştirmede özellikle iyidir. ExCAR-T veya RD07 olarak adlandırılan bu geliştirilmiş hücreler yalnızca gördüklerini öldürmekle kalmayıp tümörün bağışıklık ortamını yeniden şekillendirmek üzere tasarlandı.
Preklinik Modellerde Güçlü Tümör Kontrolü
Sindirim kanserleri fare modellerinde ExCAR-T hücreleri IL-7 ve XCL1 içermeyen geleneksel CAR-T hücrelerine göre daha iyi performans gösterdi. Laboratuvar ortamında, mühendislikli hücreler daha fazla kanser hücünü öldürdü ve daha çok uzun ömürlü, bellek-benzeri T hücresi içerdi. Claudin18.2-pozitif tümör taşıyan hayvanlarda ExCAR-T tedavisi tümörleri daha derin küçülmelerle sonuçlandırdı ve standart CAR-T hücrelerine göre sağkalımı uzattı. Geliştirilmiş hücreler kanda daha iyi genişledi ve ek bağışıklık hücrelerini çeken sinyaller dahil olmak üzere daha geniş bir bağışıklık aktivasyonu tetikledi; aynı zamanda tümör yayılımıyla ilişkili faktörleri azalttı. Çarpıcı biçimde, ExCAR-T ile tedavi edilip iyileşen fareler, artık Claudin18.2 hedefini taşımayan kanser hücrelerine karşı ikinci bir saldırıyı reddetti; bu, tedavinin dar, tek hedefli bir yanıttan ziyade kalıcı, tüm tümöre yönelik bağışıklık belleği başlattığını gösteriyor.
Hastalarda Erken Klinik Deneme Sonuçları
Bu veriler cesaret verici olduğundan, araştırmacılar ileri evre mide, gastroözofageal bileşke veya pankreas kanseri olan ve standart tedavilerle başarısız olmuş 12 kişide RD07’nin ilk insan çalışmasını başlattı. Yan etkiler genel olarak yönetilebilirdi: en ciddi sorunlar infüzyon öncesi kemoterapinin yol açtığı kan sayımı düşüşleri idi ve yalnızca hafif sitokin salınım reaksiyonları görüldü; ciddi beyinle ilgili toksisiteler yaşanmadı. Değerlendirilebilen 10 hasta arasında 7’sinde ölçülebilir tümör küçülmesi ve 2’sinde kısmi yanıt elde edildi. Tümörlerinde orta ila yüksek düzeyde Claudin18.2 gösteren hastalar özellikle iyi sonuç aldı; bu hastaların her biri en az hastalığın stabilizasyonunu yaşadı ve bazıları beklenenden aylarca daha uzun yaşadı. Bu yanıt verenlerde modifiye T hücreleri kanda daha güçlü genişledi ve kan IL-7 ile XCL1 düzeyleri tedavinin tasarımına uygun şekilde daha yüksek seviyelere ulaştı.
Tümörün Bağışıklık Mahallesine İç Bakış
RD07’nin insanlarda nasıl çalıştığını anlamak için ekip, tedavi öncesi ve sonrası tümör örneklerini tek hücre çözünürlüğünde inceledi. Yanıt veren hastalarda Claudin18.2-pozitif kanser hücrelerinin payının azaldığını gördüler; bu, terapinin hedeflediği noktaya vurduğunu doğruluyor. Aynı zamanda, aktif öldürücü hücreler ve dokuya yerleşik bellek hücreleri de dahil olmak üzere çeşitli T hücre klonlarında bir patlama görüldü; bu, vücudun daha geniş bir bağışıklık saldırısı başlattığını düşündürüyor. Uzmanlaşmış dendritik hücreler artmış aktivite belirtileri ve çoğalan T hücrelerle daha güçlü etkileşimler gösterdi; bu, XCL1’in onları tümöre çekmesi ile tutarlı. Bir hastanın tümör diliminin görüntüleme çalışmaları, tedavi sonrası daha az tümör ve baskılayıcı miyeloid hücre, daha fazla T ve B hücresi ve dokunun bağışıklık açısından zengin bölgelere yeniden örgütlendiğini ortaya koydu; bunlar daha “sıcak”, daha enflamatuar bir mikroçevrenin ayırt edici işaretleri.
Geleceğin Kanser Bakımı İçin Ne Anlama Gelebilir
Preklinik ve erken klinik bulgular birlikte ele alındığında, RD07’nin yalnızca kansere yönelik başka bir hedefli ilaç eklemekten fazlasını yaptığı görülüyor. Tümör tanıma ile dahili bağışıklık desteğini birleştirerek bu mühendislikli T hücreleri daha uzun süre hayatta kalabilir, kilit partner hücreleri çekebilir ve hastanın kendi bağışıklık sistemini orijinal hedef kaybolsa bile kanseri kontrol altında tutacak şekilde eğitebilir. Deneme küçük ve ağır ön işlem görmüş hastalarda yürütülmüş olsa da, tutarlı tümör küçülmesi, kabul edilebilir güvenlik ve derin bağışıklık yeniden yapılanması ümit verici. Daha büyük çalışmalarda doğrulanırsa, bu yaklaşım, tümör içindeki bağışıklık ekosistemini güçlendirmenin, kanser hücrelerine yapılan ilk vuruş kadar önemli hale geldiği sindirim sistemi kanserlerinin tedavisinde yeni bir bölüm açabilir.
Atıf: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
Anahtar kelimeler: CAR-T hücre tedavisi, sindirim sistemi kanseri, Tümör mikroçevresi, Claudin18.2, immünoterapi