Clear Sky Science · tr
M6A ile değiştirilmiş circArhgap26, plakofilin-1 palmitoilasyonunu baskılayarak kalp iskemi–reperfüzyon hasarını hafifletir
Kalp krizi sonrası kalbi korumanın önemi
Bir kişi kalp krizi geçirdiğinde, hekimler tıkalı damarı hızla açıp kan akışını yeniden sağlamaya çalışır. Bu kurtarıcı adım hayat kurtarır, ancak bir yanı da vardır: kanın ani geri dönüşü kalbe daha fazla zarar verebilir; buna iskemi–reperfüzyon hasarı denir. Burada özetlenen çalışma, kalp hücrelerinin içinde beklenmedik bir doğal savunmacıyı araştırıyor—circArhgap26 adı verilen dairesel bir RNA parçası—ve bu molekülün kalp kasını bu ikincil hasar dalgasından korumaya yardımcı olduğunu gösteriyor. Bu küçük molekülün nasıl çalıştığını anlamak, kalp hastaları için yeni tedavilere ve kan testlerine işaret edebilir.
Kalbin genetik metnindeki gizli bir halka
Çoğumuz genleri düz DNA ve RNA dizileri olarak düşünürüz, ama hücreler aynı zamanda sıra dışı şekilde kararlı ve birçok hücresel süreci hassaslaştırabilen halka biçimli RNA molekülleri, yani dairesel RNA’lar üretir. Araştırmacılar, kalp hasarı sırasında değişen dairesel RNA’ları fare kalplerinde aradı ve kan akışı kesilip geri geldiğinde düzeyi keskin biçimde düşen circArhgap26’ya odaklandı. Bu dairesel RNA’nın kapalı bir halka oluşturduğunu, ağırlıklı olarak hücre sıvısı bölmesinde bulunduğunu ve protein yapmak için bir şablon görevi görmediğini doğruladılar. Bunun yerine, başka moleküllerle etkileşime girerek bir kalp hücresinin stres sonrası yaşayıp yaşamayacağını etkileyen bir düzenleyici gibi görünmektedir. 
Dairesel RNA’nın kalbi koruduğunun kanıtı
CircArhgap26’nın gerçekte ne yaptığını görmek için ekip fare kalplerinde düzeylerini artırıp azalttı. Virüs kullanarak özellikle kalp kası hücrelerinde circArhgap26’yı yükselttiklerinde, koroner arterin geçici olarak tıkanıp kan akışının yeniden sağlandığı hayvanlarda kalp pompalama gücü daha iyi, hasarlı bölgeler daha küçük ve ölen hücre sayısı daha az oldu. Kan ve kalp dokusundaki klasik hasar belirteçleri de daha düşüktü. Dairesel RNA susturulduğunda ise tersi görüldü: indüklenmiş bir kalp krizi olmasa bile kalbin fonksiyonu kötüleşti ve hücre ölümü arttı; iskemi–reperfüzyon eklendiğinde bu sorunlar daha da şiddetlendi. Benzer koruyucu etkiler laboratuvarda insan kalp benzeri hücrelerde de görüldü; bu da mekanizmanın fareler ile insanlar arasında korunmuş olabileceğini düşündürüyor.
Baskı altında tutulan zararlı bir eşlikçi protein
Daha derine inen araştırmacılar circArhgap26’nın bu korumayı nasıl sağladığını sordular. Biyokimyasal avlama teknikleri kullanarak, bunun plakofilin‑1 (PKP1) adındaki yapısal bir proteinle doğrudan bağlandığını buldular; bu protein hücrelerin birbirine ne kadar sıkı bağlandığını ve programlı hücre ölümüne ne kadar yatkın olduklarını etkileyebilir. Yaralı kalplerde ve stres altındaki kalp hücrelerinde PKP1 düzeyleri yükseldi ve daha kötü hasarla ilişkilendirildi. PKP1 susturulduğunda kalp hasarı ve hücre ölümü azaldı; tersine, PKP1 üretimi zorlanırsa sonuçlar daha kötüleşti. CircArhgap26 artırıldığında, PKP1 proteininin miktarı gen aktivitesi değişmemesine rağmen düştü; bu da kontrol noktasının RNA mesajı üretildikten sonra olduğunu gösteriyor. Deneyler, circArhgap26’nın PKP1’in normalde onu stabilize eden bir yağlı modifikasyon süreci olan palmitoilasyonla etkileşime girerek PKP1 protein bozunmasını hızlandırdığını gösterdi.
Hücre ölümü sinyalleri üzerinde moleküler bir çekişme
Palmitoilasyon, bir enzim ailesi tarafından gerçekleştirilir; özellikle ZDHHC1 adlı bir üyenin PKP1’e yağ grupları ekleyip onu daha uzun ömürlü hale getirdiği bulundu. CircArhgap26, PKP1’e ZDHHC1’in kullandığı aynı bölgede bağlanarak moleküler bir çekişme yaratır. Dairesel RNA kazanınca, PKP1 daha az yağ etiketi alır, daha az stabil olur ve daha hızlı temizlenir. Bunun bir sonucu vardır: PKP1 normalde APAF1 adlı başka bir proteinin üretilmesini, onun RNA’sının bir kontrol segmentiyle etkileşerek artırır. APAF1, kaspaz‑9 ve kaspaz‑3 enzimlerini aktive eden ölüm mekanizmasının kilit bir parçasıdır; bu enzimler hücre ölümünün merkez yürütücüleridir. Daha az stabil PKP1 ile APAF1 protein üretimi düşer, ölüm sinyali kaskadı zayıflar ve kalp hücreleri yeniden sağlanan kan akışının stresine karşı hayatta kalma olasılığı artar. 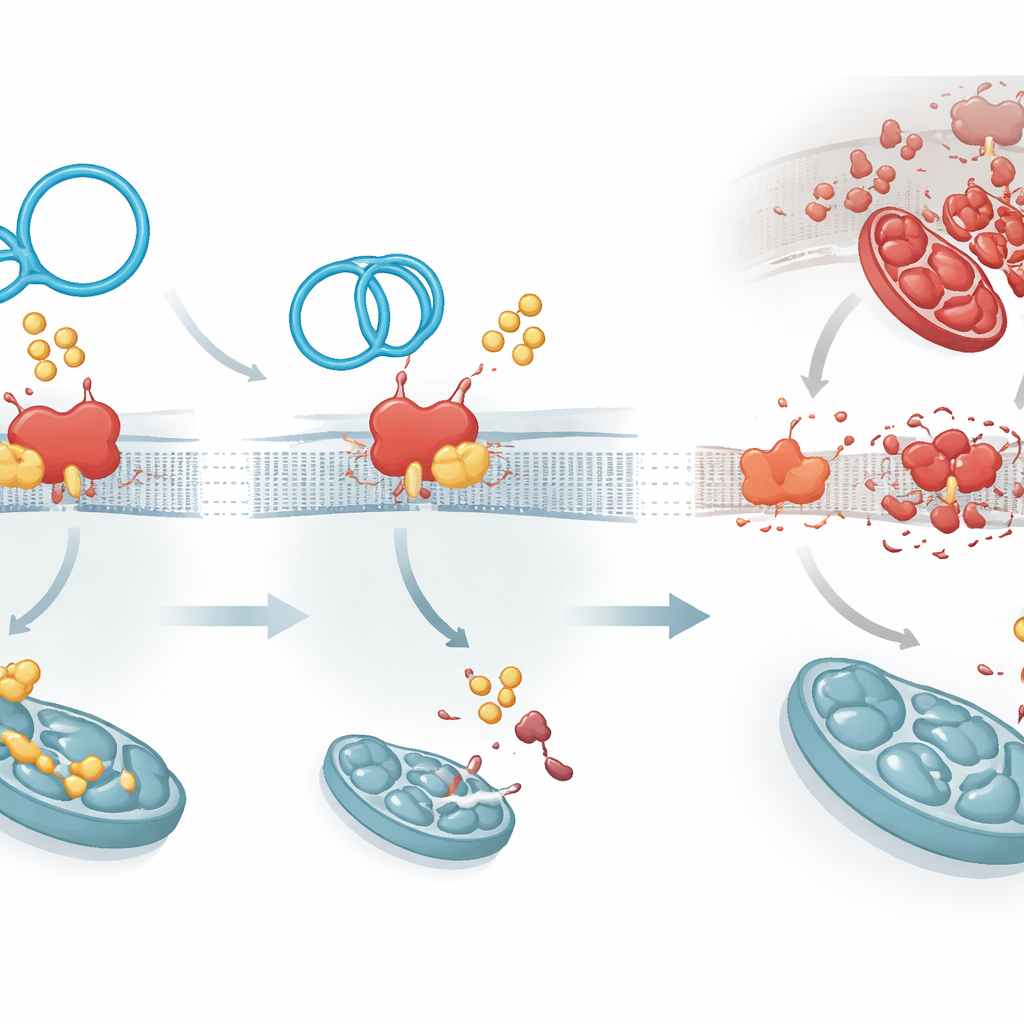
Daireyi ince ayarlamak ve hasta vaatleri
Araştırma ayrıca circArhgap26’nın kendisinin hasar sırasında nasıl azaltıldığını da ortaya koyuyor. m6A olarak adlandırılan yaygın bir kimyasal işaret, stres altındaki kalplerde bu dairesel RNA üzerinde birikir. YTHDF2 adlı bir “okuyucu” protein bu işareti tanır ve circArhgap26’nın parçalanmasını teşvik ederek kalbin doğal savunmasını tam ihtiyaç duyulduğu anda zayıflatır. Önemli olarak, bu dairesel RNA’nın insan versiyonu farekine yüksek benzerlik gösterir ve arter açma girişimleri yapılan hastaların kanında, sağlıklı gönüllülere kıyasla belirgin şekilde daha düşüktür. Bu bulgular birlikte, circArhgap26’yı eski haline getirmek veya taklit etmenin hem kan temelli bir risk belirteci hem de yeni bir tedavi olabileceğini düşündürür. Basitçe söylemek gerekirse, çalışma, kalp hücreleri içinde ölümcül zincirlemeyi etkisiz hale getirerek reperfüzyon hasarına karşı koruyucu rol oynayan küçük bir dairesel molekülü ortaya koyuyor.
Atıf: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Anahtar kelimeler: iskemi reperfüzyon hasarı, dairesel RNA, kalp krizi, kardiyomiyot apoptozu, RNA tabanlı tedavi