Clear Sky Science · tr
Kemo-fototermal sinerji, ferroptoz yoluyla antitumör bağışıklığı ateşliyor
Vücudun Isısını ve Işığını Kanser Savaşçısına Dönüştürmek
Kemoterapi ilaçları tümörleri küçültebilir, ancak genellikle ağır yan etkilere sahiptir ve her zaman kanserin geri gelmesini engellemezler. Bu çalışma, mevcut bir ilaç olan doksetakselin, onu ısıya duyarlı küçük parçacıklar içine paketleyip yakın kızılötesi ışıkla aktive ederek daha güçlü ve akıllı çalışmasını sağlamanın yeni bir yolunu araştırıyor. Amaç yalnızca tümör hücrelerini daha hassas şekilde öldürmek değil; aynı zamanda bağışıklık sistemini uyandırıp kanseri vücut genelinde tanımasını ve gelecekteki nüksleri önlemesini sağlamak. 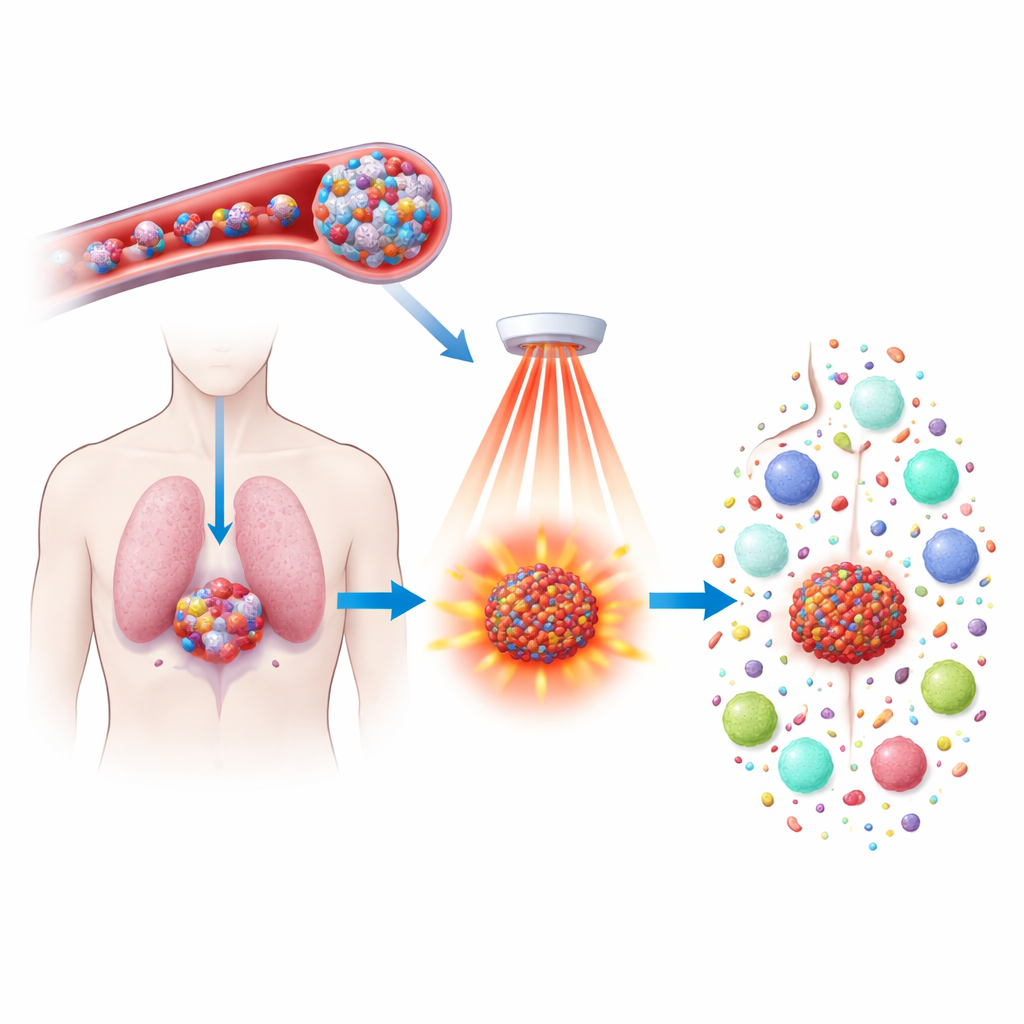
Nereye Gideceğini Bilen Minik Kuryeler
Araştırmacılar, ferrosen içeren bir polimerden yeni bir nanoparçacık türü geliştirdiler; ferrosen, tümör içinde normal dokulara göre daha yüksek miktarda bulunan hidrojen peroksit ile kuvvetle reaksiyona giren bir demir taşıyıcı moleküldür. Bu polimerler, doksetaksel ile IR808 adlı ışık emen bir boyayı taşıyabilen, suda çözünür küreler halinde kendiliğinden bir araya gelir. Kan dolaşımına verildiklerinde parçacıklar yeterince küçük ve kararlıdır, tümörlere dolaşıp sızar; sızıntılı kan damarları ve yüksek hidrojen peroksit düzeyleri parçacıkları zayıflatarak yüklerini yavaşça serbest bırakmaya başlar. Bu tasarım tedaviyi tümörlere yoğunlaştırırken sağlıklı organlara verilen zararları sınırlar.
Yerel Hasarı Işıkla Güçlendirmek
Dokuya güvenle nüfuz edebilen yakın kızılötesi ışık daha sonra tümör bölgesine yönlendirilir. Nanoparçacıkların içindeki IR808 bu ışığı soğurur, ısıya dönüştürür ve aynı zamanda kimyasal olarak reaktif oksijen türleri üretir. Tümörün ürettiği hidrojen peroksit ile ışık kaynaklı oksidanların birleşimi parçacıkların daha hızlı parçalanmasına ve ilaç yüklerini tam gereken yerde boşaltmasına neden olur. Aynı zamanda ferrosen içindeki demir, bu oksidanları hücre zarlarının yağlı bileşenlerine saldıran özellikle agresif formlara dönüştürmeye yardımcı olur. Bu hedeflenmiş kimyasal ve termal saldırı, doksetaksel veya yalnızca ışık tedavisine kıyasla öldürme gücünü keskin şekilde artırır. 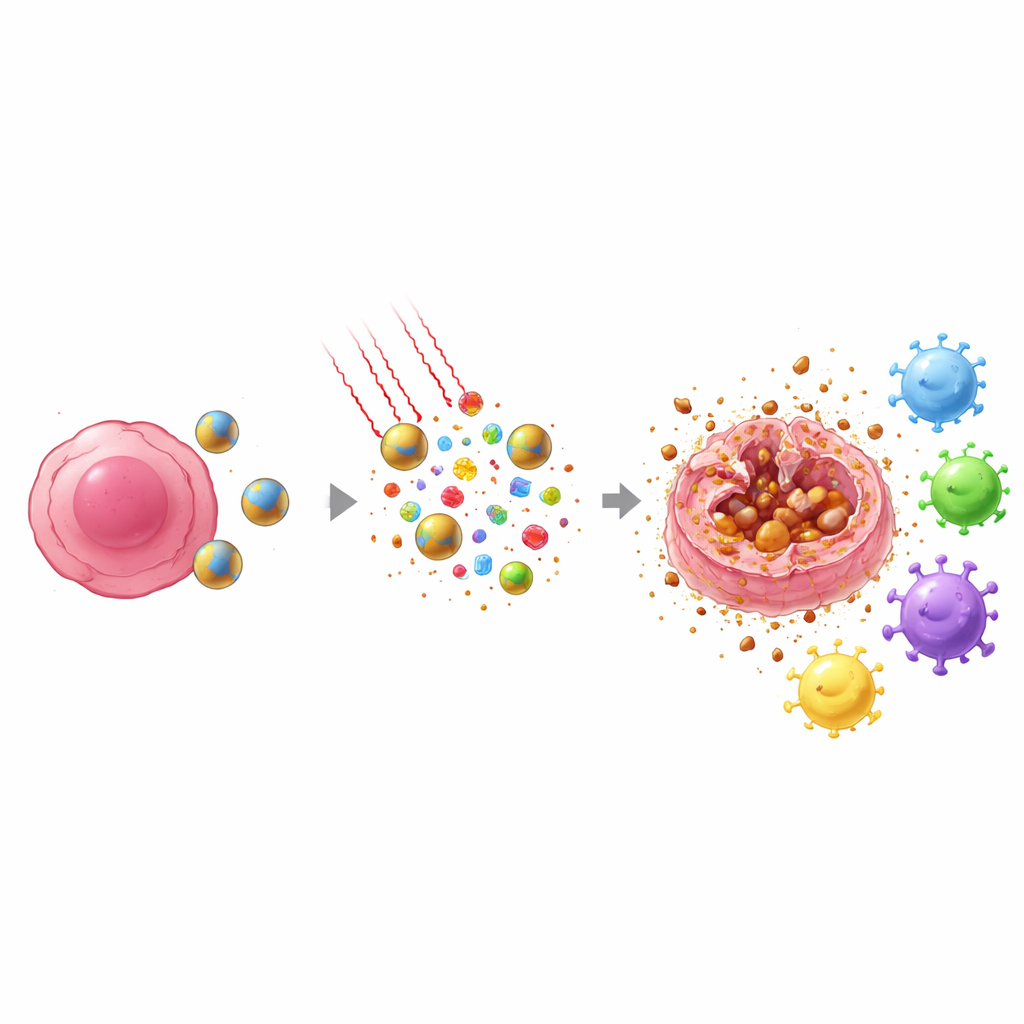
Bağışıklık Sistemini Sinyalleyen Kontrollü Bir Yanma
Önemli olarak, bu tedavi altında tümör hücrelerinin ölme biçimi sıradan kemoterapiden farklıdır. Hücreler sessizce düzenli parçalara ayrılmak yerine çoğu zaman ferroptoz adı verilen bir süreç geçirir; bu, demir kaynaklı ve lipidlere zarar veren, hücrenin dış zarının yırtıldığı bir ölüm biçimidir. Bu olduğunda hücreler çevrelerine içsel alarm sinyalleri ve tümöre özgü parçacıklar salar. Aynı zamanda doksetaksel, HMGB1 adlı önemli bir nükleer proteini hücre kenarına doğru iterek serbest bırakılmaya hazırlar. Isı, oksidanlar ve ilacın etkisi birlikte, yakınlardaki immün gözcüler—dendritik hücreler—tarafından algılanıp lenf düğümlerine taşınabilecek bir tehlike ve antijen sinyali patlaması yaratır.
Yerel Saldırından Bütün Vücut Savunmasına
Fare tümör modellerinde bu kombine kemo‑fototermal tedavi, yalnızca ısıtılan tümörleri tek başına herhangi bir bileşenden daha etkili şekilde küçültmekle kalmadı, aynı zamanda bağışıklık ortamını da değiştirdi. Tümörlerde hem tümör içinde hem de drenaj yapan lenf düğümlerinde daha olgun dendritik hücreler ve daha fazla sayıda öldürücü T hücresi gözlendi. Bazı immün yetenekli farelerde birincil tümörler yalnızca iki tedavi döngüsünden sonra kayboldu. Bilim insanları daha sonra uzak bölgelerde veya karşı tarafta yeni tümörler yerleştirdiklerinde, bu ikincil büyümeler yavaşladı veya baskılandı; bu da hayvanların kansere özgü bir bağışıklık belleği geliştirdiğini gösteriyor. T hücresi tükenmesini engelleyen bir kontrol‑nokta bloke edici antikoru eklemek akciğer metastazlarını daha da azalttı ve sağkalımı uzattı; bu da yerel tedavinin modern immünoterapilerle birleştirilebileceğini düşündürüyor.
Geleceğin Kanser Bakımı İçin Neden Önemli
Bir uzman olmayan için temel çıkarım şudur: Bu yaklaşım doksetakseli keskin olmayan sistemik bir zehirden, akıllı, çok aşamalı bir anti‑kanser stratejisinin parçasına dönüştürüyor. İlacı, tümörün kendi kimyasına yanıt veren ışıkla aktive edilen, demir içeren nanoparçacıklar içinde paketleyerek tedavi tümörlerin içinde daha fazla hasar verirken sağlıklı dokuları koruyor. Tetiklediği belirli hücre ölümü deseni tümörün içinden bir aşı gibi davranarak bağışıklık sistemine kanseri tanımayı ve hatırlamayı öğretiyor. Bu bulgular insanlara tercüme olabilirse, bu tür kemo‑fototermal sistemler dirençli “soğuk” tümörleri immün temelli tedavilere çok daha iyi yanıt veren “sıcak” tümörlere dönüştürmeye yardımcı olabilir; bu da nüksü azaltma ve uzun vadeli kontrolü iyileştirme potansiyeli taşır.
Atıf: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Anahtar kelimeler: kanser nanoterapisi, fototermal tedavi, ferroptoz, kanser immünoterapisi, doksetaksel taşıma