Clear Sky Science · tr
İletken koordinasyon nanozimi proilaçları, tümör yerinde aşılaması için piroptoz, kuproptoz ve ferroptozu hassas şekilde tetikliyor
Tümörleri Kendi Aşılarına Dönüştürmek
Kanser tedavisi genellikle tümör hücrelerini doğrudan öldürmeyi hedefler; ancak ya bir tümör kendi aşısına dönüştürülebilse? Bu çalışma, vücutta güvenle taşınan, yalnızca tümör içinde etkinleşen ve ardından bağışıklık sistemini güçlü şekilde uyaran bir şekilde kanser hücrelerini ölüme zorlayan akıllı bir nanoparçacık “proilaç”ı anlatıyor. Sonuç, yalnızca primer tümörlerin küçülmesi değil, aynı zamanda vücudun uzak tümörleri ve metastazları da hedef alacak şekilde eğitilmesi oluyor.
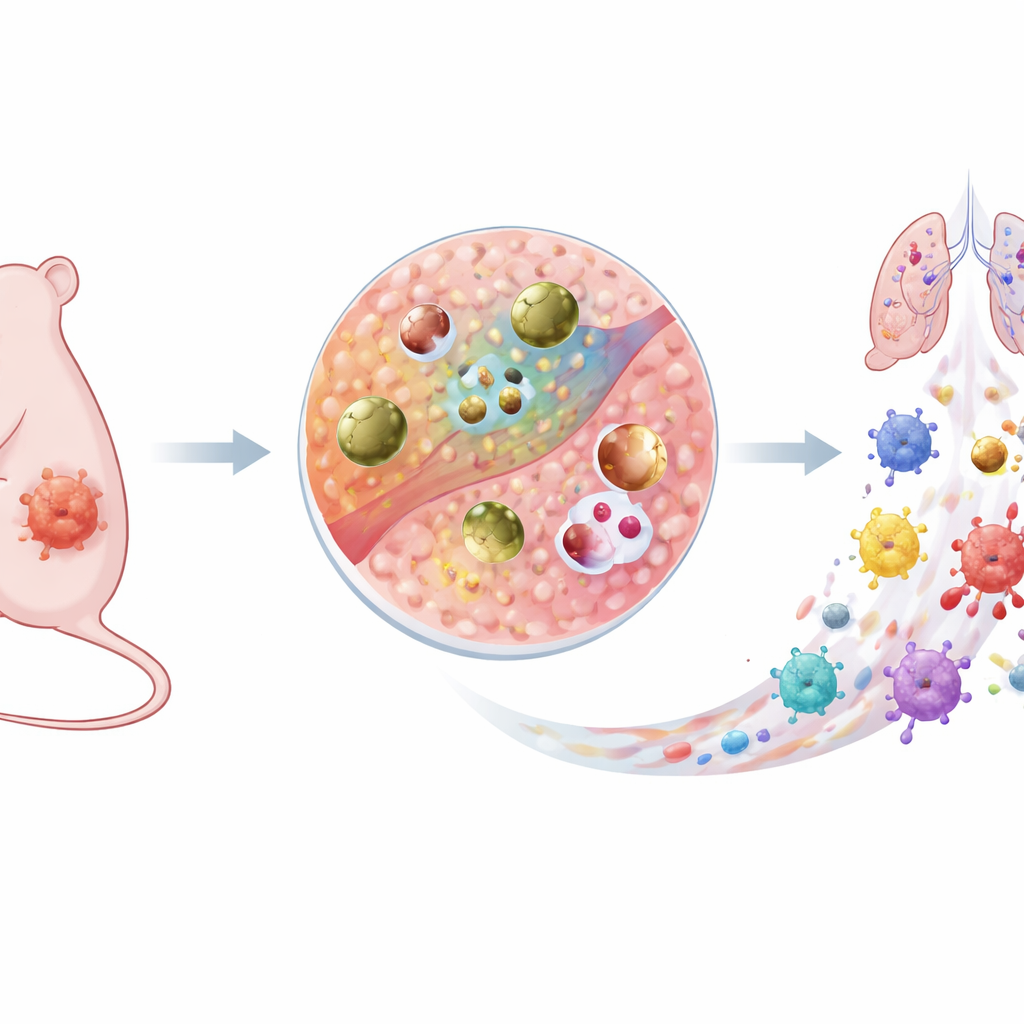
Yeni Türden Akıllı Bir Kanser Silahı
Araştırmacılar, dolaşım sırasında uykuda bir ilaç gibi davranan ve tümöre ulaştığında agresif bir kanser savaşçısına dönüşen Cu–DHN adlı küçük bir bakırlı partikül geliştirdiler. Bu yapı, bakır iyonları, zararsız bir öncü molekül (1,5-dihidroksinaftalin, yani DHN) ve sistein amino asidinden bir araya geliyor. Bir iletken koordinasyon ağı oluşturuyorlar; yani elektronlar parçacık içinde kolayca hareket edebiliyor. Bu içsel “elektron otoyolu”, yalnızca yüzey değil tüm nanoparçacığın kimyasal reaksiyonlara katılmasına izin veriyor. Kritik olarak, Cu–DHN tümör mikroçevresinin alışılmadık kimyasına yanıt verecek şekilde tasarlandı; burada antioksidan glutatyon ve hidrojen peroksit her ikisi de anormal derecede yüksektir.
Tümör Kimyası Nasıl Açma Düğmesini Çevirir
Tümörlerin içinde Cu–DHN yapay bir enzim gibi davranır. Glutatyon ve hidrojen peroksit birlikte var olduğunda, önce glutatyonu kullanarak bakır iyonlarını yüksek reaktivite durumuna resetler, sonra hidrojen peroksiti kullanarak sürekli bir yüksek agresiflikte oksidan (hidroksil radikalleri) patlaması üretir. Bu oksidanlar çifte etki yapar: hücresel bileşenlere zarar verir ve partikül içinde kilitli zararsız DHN’yi güçlü bir antikanser bileşiği olan juglon’a dönüştürür. Juglon ise tümörün kendi antioksidan savunmasını baskılar ve hidrojen peroksit düzeylerini daha da artırır; böylece yalnızca tümörün sağladığı kimyasal girdilerle başlatılabilen, tümörde sınırlı kalan kendini güçlendiren bir oksidatif stres döngüsü oluşur.
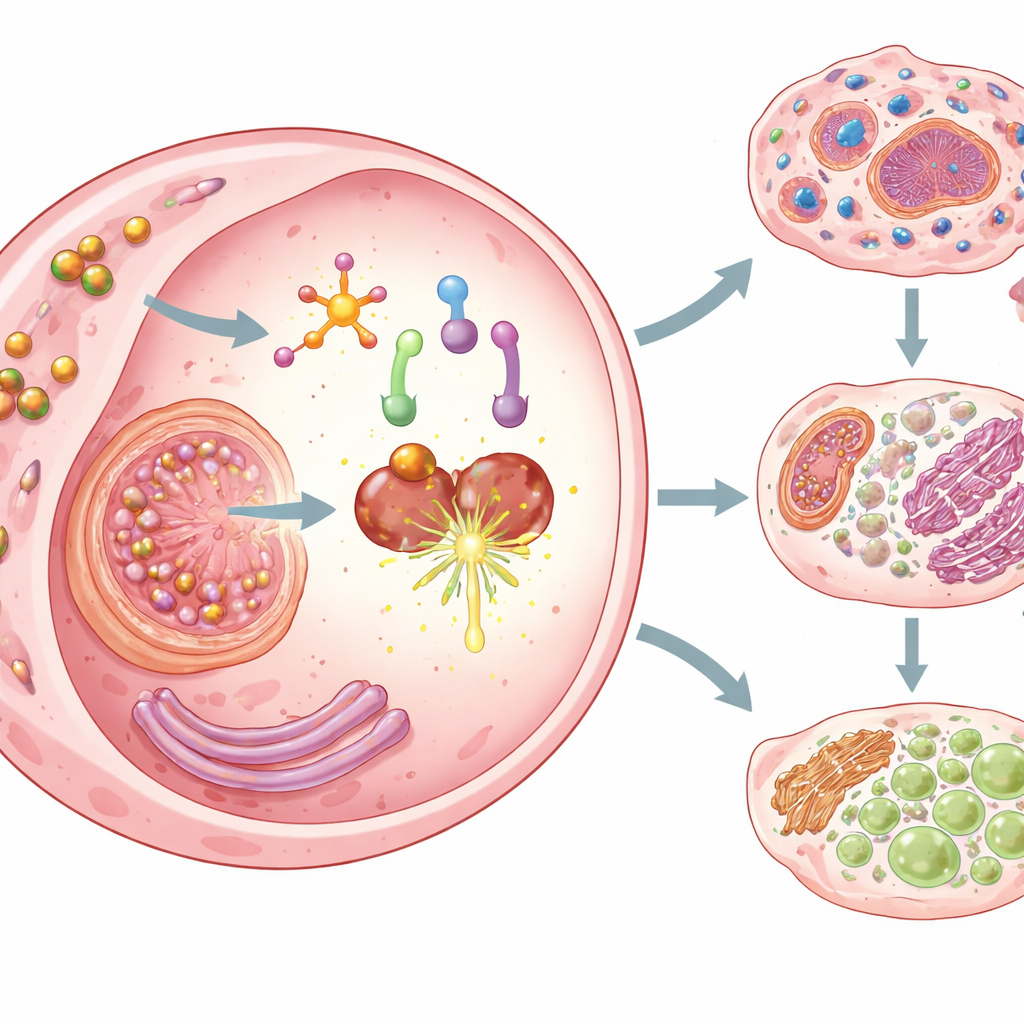
Üç Tür Kanser Hücresi Ölümünü Tetikleme
Etkinleştiğinde Cu–DHN sadece kanser hücrelerini zehirlemekle kalmaz. Bağışıklık sistemi tarafından özellikle iyi görülen üç düzenlenmiş hücre ölümü biçimini tetikler. Birincisi, juglon bir gözenek oluşturan protein olan gasdermin D’nin epigenetik susturulmasını tersine çevirir ve inflamatuar bir sensör kompleksini aktive eder; böylece hücreler membranı patlatan ve içeriği dışarı saçan dramatik, kabarcıklı bir ölüm biçimi olan piroptoza girer. İkincisi, nanoparçacıklarla taşınan bakırın kanser hücreleri tarafından verimli şekilde alınması, kritik metabolik mekanizmalarda bakırın toksik birikimine bağlı olan kuproptoza yol açar. Üçüncüsü, glutatyonu tüketip koruyucu bir enzim olan GPX4’ü işlevsiz hale getirerek Cu–DHN ferroptozu, yani lipid peroksidasyonuna dayalı ölümü teşvik eder. Bu modların birleşimi, kanser hücrelerinin yalnızca etkin şekilde öldürülmesini sağlamakla kalmaz, aynı zamanda özellikle immünojenik bir şekilde ölmelerini garanti eder.
Yerel Saldırıdan Bütün Vücut Savunmasına
Piroptoz ve eşlik eden oksidatif hasar, tümör hücrelerinin bir dizi alarm sinyali salmasına neden olur: tümörle ilişkili antijenler, ATP ve HMGB1 gibi tehlike molekülleri ve yüzeydeki stres belirteçleri. Agresif meme kanseri fare modellerinde, primer tümöre verilen tek bir Cu–DHN enjeksiyonu, yakın lenf düğümlerindeki dendritik hücrelerin güçlü aktivasyonuna ve tümör avcısı CD8 T hücrelerinin süratle artışına yol açtı. Bu bağışıklık hücreleri daha sonra vücudun diğer tarafındaki tedavi edilmemiş tümörlere ve akciğerlere giderek yeni tümörlerin ve metastatik nodüllerin büyümesini yavaşlattı veya neredeyse engelledi. CD8 T hücrelerinin bloke edilmesi bu korumayı büyük ölçüde ortadan kaldırdı; bu da Cu–DHN’nin primer tümörü bağışıklık sistemine başka yerdeki kanseri tanımayı ve yok etmeyi öğreten yerinde bir aşıya dönüştürdüğünü doğruluyor.
Daha Güvenli Bir Profil ile Güçlü Etkiler
Piroptoz tabanlı tedavilerle ilgili önemli bir endişe, aynı gözenek oluşturan proteinleri taşıyan normal dokulara zarar verme riskidir. Juglon aktif formunda doğrudan verildiğinde farelerde belirgin karaciğer, böbrek ve kan toksisitesi görülür. Buna karşılık, Cu–DHN sağlıklı dokularda etkisiz kalır; çünkü bu dokular parçacığı aktive etmek için gereken kimyasal tetikleyicilerin kombinasyonuna sahip değildir. Farelerde Cu–DHN aktif juglon’un tümör öldürücü ve anti-metastatik gücüyle eşdeğerken organ hasarı, kan anormallikleri ve kilo kaybından kaçındı. Basitçe özetlersek, bu çalışma iletken bir nanoparçacığın vücutta sessiz kalmasını, yalnızca tümör içinde uyanmasını, kanser hücrelerini bağışıklığı uyaran bir biçimde ölmeye zorlamasını ve böylece hassas, kendi içinde tamamlanmış bir kanser aşısı platformu görevi görmesini nasıl sağlayabileceğini gösteriyor.
Atıf: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
Anahtar kelimeler: kanser immünoterapisi, nanomedisin, piroptoz, kanser aşıları, tümör mikroçevresi