Clear Sky Science · tr
KDM5B’nin ubiquitin aracılı stabilizasyonu, over kanserinde çift özgüllükte fosfataz 4’ün baskılanması yoluyla kemorezistansı tetikliyor
Neden bazı over kanserleri kemoterapiye yanıt vermeyi bırakır
Over kanserli pek çok kadın başlangıçta sisplatin gibi platin bazlı ilaçlara iyi yanıt verir, ancak tümörler daha sonra tedaviye yanıt vermeyen şekilde geri dönebilir. Bu çalışma, kanser hücrelerinin ilaç dirençli hale gelmesine yardımcı olan gizli bir moleküler devreyi ortaya koyuyor. Spesifik bir “epigenetik anahtarın” nasıl açılıp kapandığını ortaya koyarak, araştırmacılar hangi tümörlerin terapiye direnç göstereceğini tahmin etmenin ve bunları mevcut ilaçlara yeniden duyarlı hale getirmenin yeni yollarına işaret ediyor.
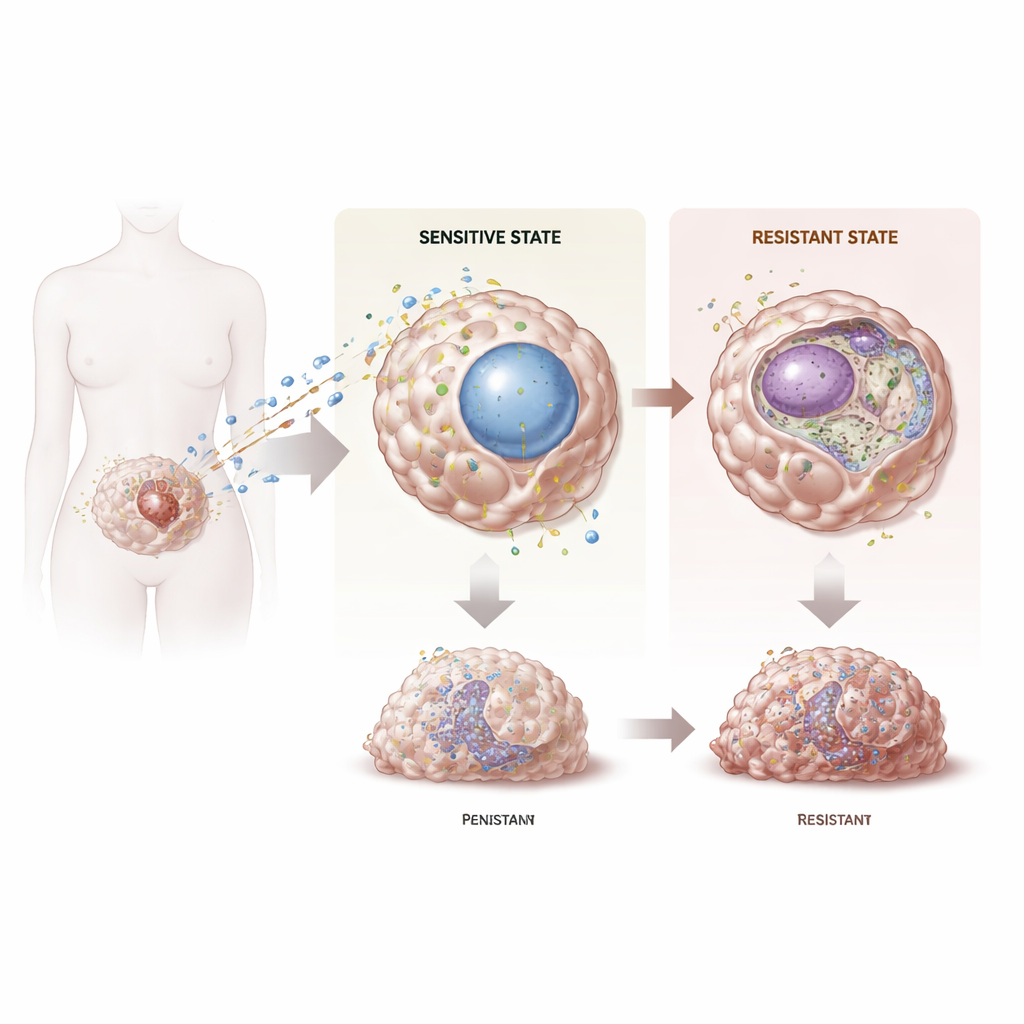
Ölümcül bir kanserin inatçı geri dönüşü
Over kanseri, genellikle geç evrede saptanması ve kemoterapi direncinin yaygın olması nedeniyle en öldürücü jinekolojik kanserlerden biridir. Hastaların yüzde 80’e varan kısmı başlangıçta platin bazlı kemoterapiden yarar görse de çoğu, artık yanıt vermeyen tümörlerle nüks eder; bu da sınırlı seçenek ve kötü sağkalım demektir. Son çalışmalar, DNA’nın nasıl paketlendiği ve okunduğundaki—epigenetik—değişikliklerin kanser hücrelerinin tedaviye uyum sağlamasına yardımcı olabileceğini gösterdi. Yazarlar, histon proteinlerinden kimyasal işaretleri kaldırarak gen aktivitesini ince ayarlayan KDM5 adı verilen enzim ailesine odaklandı. Bu ailenin hangi üyelerinin platin direncinde kilit rol oynayabileceğini sordular.
Tek bir enzim direnç lehine dengeyi kaydırıyor
Büyük kanser genomik veritabanlarını tarayıp birden çok over kanseri hücre hattını test ederek ekip, bir KDM5 üyesi olan KDM5B’nin dirençli tümörlerde öne çıktığını keşfetti. KDM5B seviyeleri nüks eden over kanserlerinde, metastatik lezyonlarda ve sisplatine artık yanıt vermeyen hücre hatlarında daha yüksekken, yakın akrabası KDM5A aynı paterni göstermiyordu. Araştırmacılar dirençli hücrelerden selektif olarak KDM5B’yi uzaklaştırdıklarında, bu hücreler yeniden sisplatine karşı savunmasız hale geldi ve daha fazla programlı hücre ölümü yaşadı. Orijinalde duyarlı hücrelere ekstra KDM5B eklemek tam ters etkiyi yaratarak kemoterapiyle öldürülmelerini zorlaştırdı. Bu sonuçlar birkaç bağımsız hücre modeli ve insan over tümörleri taşıyan farelerde tutarlı olarak KDM5B’yi kemorezistansın sürücüsü olarak gösterdi.
Büyüme sinyallerinin susturulmuş freni
Daha derine inen yazarlar, KDM5B’nin hangi genleri kapattığını ve bunun tümör hücrelerinin hayatta kalmasına nasıl yardımcı olduğunu sordular. RNA dizileme ve kromatin haritalama kullanarak, KDM5B’nin doğrudan DUSP4 adlı bir geni baskıladığını buldular; DUSP4 normalde MAPK yolu olarak bilinen önemli bir büyüme ve stres yanıtının frenini sağlayan bir rol oynar. KDM5B, DUSP4 promotörüne bağlanır ve “açık” işaretleri silerek DUSP4 seviyelerini düşürür, böylece MAPK sinyaline uygulanan fren serbest kalır. DUSP4 düşük olduğunda MAPK aktivitesi artar, hücre büyümesini teşvik eder ve hücrelerin sisplatinin neden olduğu DNA hasarına karşı dayanmasına yardımcı olur. DUSP4’ü geri kazanmak bu direnci tersine çevirir; DUSP4’ün silinmesi ise KDM5B’nin uzaklaştırılmasının faydasını iptal eder—hem hücre kültürlerinde hem de fare tümörlerinde. Hasta verileri de bu bulguları yansıtıyor: yüksek KDM5B ve düşük DUSP4 seviyelerine sahip tümörler daha kötü sağkalım ile ilişkilendiriliyor.
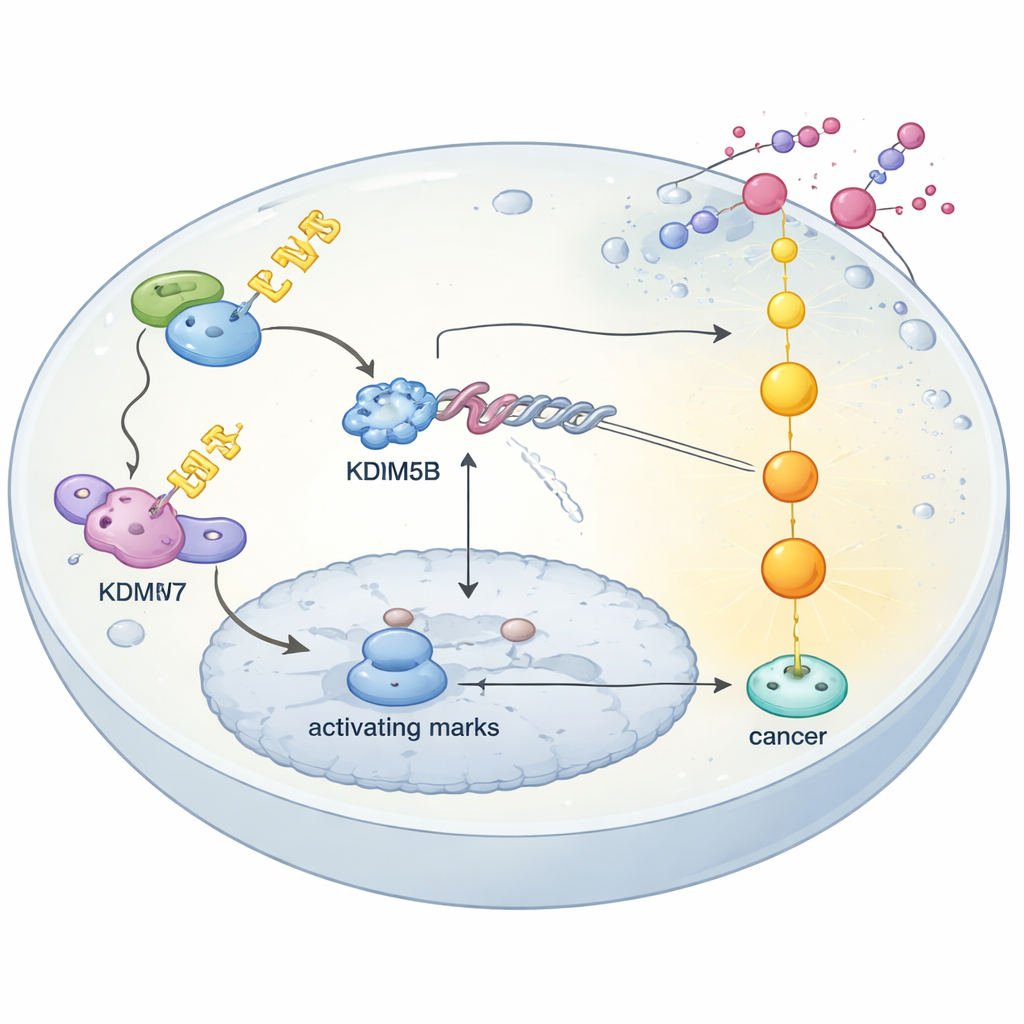
Protein kalite kontrolü ilaç yanıtını şekillendiriyor
Çalışma ayrıca kanser hücrelerinin KDM5B’yi ilk aşamada nasıl stabilize ettiğini gösteriyor. Hücre içinde birçok protein sürekli olarak yok edilmek üzere işaretlenir veya ubiquitin zincirlerine dayanan kalite kontrol sistemi tarafından korunur. Araştırmacılar USP7 adlı bir enzimin, bu etiketleri kaldırarak KDM5B’yi koruduğunu ve onun yıkımını önlediğini gösteriyor. USP7 genetik olarak veya küçük moleküllü bir inhibitörle engellendiğinde KDM5B seviyeleri düşer ve dirençli over kanseri hücreleri sisplatine yeniden duyarlı hale gelir. Buna karşılık, FBXW7 adlı bir proteinin etrafında kurulu bir E3 ligaz kompleksi, KDM5B’yi yalnızca başka bir enzim olan HIPK1 onu belirli bir bölgede fosforile ettikten sonra tanır ve yok edilmek üzere işaretler. Bu FBXW7–HIPK1 yolunun bozulması KDM5B’yi daha stabil hale getirir. Genel olarak, USP7’nin koruyucu rolü FBXW7’nin tasfiye rolünü aştığında direnç ortaya çıkar; bu durum KDM5B’nin birikmesine ve DUSP4’ün kapalı kalmasına izin verir.
İnatçı tümörleri alt etmenin yeni yolları
Bu USP7–KDM5B–DUSP4–MAPK eksenini haritalayarak yazarlar, over kanseri hücrelerinin sisplatine nasıl direnç geliştirdiğine dair tutarlı bir açıklama sunuyor. Uzman olmayanlar için ana mesaj, sorunun sadece daha fazla mutasyon değil, aynı zamanda gen kontrolü ve protein yıkımının yeniden kablolanması olduğudur. Çalışma birkaç test edilebilir strateji öneriyor: KDM5B, USP7 ve DUSP4 seviyelerini platin tedavisine kötü yanıt verecekleri öngörmek için biyobelirteç olarak kullanmak; sisplatini KDM5B veya USP7 inhibitörleriyle ya da KDM5B yıkımını artıran ilaçlarla birleştirerek ilaç duyarlılığını geri kazandırmak. Bu yaklaşımlar henüz klinik doğrulama gerektirse de, bazı dirençli over kanserlerini yeniden tedavi edilebilir hâle getirmek için ümit verici bir plan sunuyor.
Atıf: Yoo, J., Kim, G.W., Jeon, Y.H. et al. Ubiquitin-mediated stabilization of KDM5B drives chemoresistance via repression of dual-specificity phosphatase 4 in ovarian cancer. Sig Transduct Target Ther 11, 89 (2026). https://doi.org/10.1038/s41392-026-02601-y
Anahtar kelimeler: over kanseri, sisplatin direnci, epigenetik düzenleme, KDM5B, MAPK sinyalleşmesi