Clear Sky Science · tr
DUSP6 yokluğu, AP-1 sinyalleşmesinin canlandırılması yoluyla tümör CD58 kaybından kaynaklanan CAR T hücresi yorgunluğunu giderir
Neden Kanserle Savaşan Hücreleri Güçlendirmek Önemli
CAR T hücreleri olarak adlandırılan mühendislik ürünü bağışıklık hücreleri belirli kan kanserlerinin tedavisinde devrim yarattı, ancak birçok hasta tümörlerin saldırıdan kaçmayı öğrendiği için yine de relapse oluyor. Bu çalışma, bazı tümörlerde CAR T hücrelerini içeriden sessizce devre dışı bırakan gizli bir zayıflığı ortaya koyuyor ve hassas bir genetik müdahalenin bu hücrelerin dayanıklılığını, enerji sağlanmasını ve öldürme gücünü nasıl geri kazandırabileceğini gösteriyor. Okuyucu için bu, gelecek nesil hücre terapilerinin daha kalıcı ve daha etkili hale gelmesine nasıl yol açabileceğine dair bir pencere sunuyor.
Tümör Hücrelerinde Eksik Bir Tutacak
CAR T hücrelerinin iyi çalışabilmesi için hedefleriyle sağlam bir temas kurmaları gerekir. Birçok tümör hücresi, bağışıklık hücrelerinin tutunmasına ve sıkı bir temas bölgesi oluşturmasına yardımcı olan CD58 adlı bir yüzey molekülü sergiler. Önceki çalışmalar, kanserler CD58’i kaybettiğinde CAR T hücrelerinin bu teması kurmakta zorlandığını ve daha az etkili hale geldiğini göstermişti. Bu çalışmada araştırıcılar daha derin bir soru sordu: bu mekanik temas sorunundan öte, CD58 kaybı CAR T hücrelerinin iç biyolojisini zaman içinde performanslarını düşürecek şekilde nasıl yeniden düzenliyor?
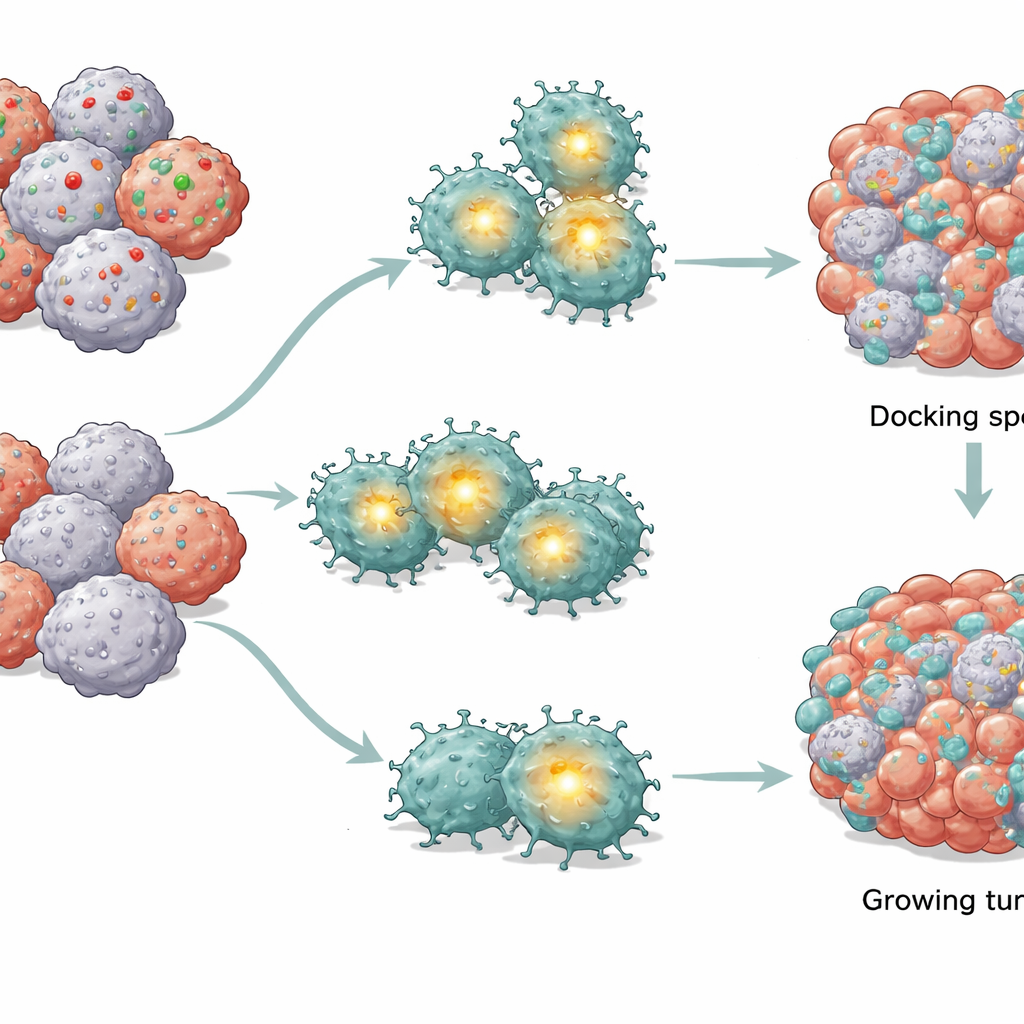
CAR T Hücrelerinin İçinde Kısalan Bağlantılar
Normal tümörlerle karşılaşanlarla CD58 eksik tümörlerle karşılaşan CAR T hücrelerini karşılaştırarak ekip, T hücrelerinin içindeki önemli bir kontrol merkezi olan AP-1’in seçici olarak zayıfladığını, diğer ana sinyal yollarının ise büyük ölçüde sağlam kaldığını buldu. AP-1, aktivasyon ve hayatta kalma ile ilgili genleri açan bir protein grubudur. AP-1 aktivitesi düştüğünde, CAR T hücreleri içsel bir enerji krizinin karakteristik işaretlerini gösterdi: daha az ve daha küçük mitokondri (enerji santralleri), oksijen tüketme ve şeker kullanma yeteneğinin azalması ve mitokondri zarları arasındaki elektriksel potansiyelin kaybı. Aynı zamanda zararlı reaktif oksijen molekülleri birikti. Bu değişiklikler birlikte, dışardan ölüm sinyalleri olmasa bile CAR T hücrelerini kendi mitokondri hasarına dayalı bir kendini yok etme programına itti.
İçsel Bir Freni Kapatmak
AP-1’in neden bu kadar baskılanmış olduğunu anlamak için araştırıcılar aşırı aktif olabilecek moleküler “frenler” için yukarı akışa baktılar. CD58-negatif tümörlerle karşılaşan CAR T hücrelerinin birkaç fosfatazı—sinyal yollarını kapatan enzimleri—artırdığını, özellikle DUSP6 adında birini buldular. Bu enzimleri ilaçlarla ve ardından hassas gen düzenleme ile bloke ederek, DUSP6’in kaldırılmasının AP-1 aktivitesini en güçlü şekilde canlandırdığını keşfettiler. DUSP6 düzenlenmiş CAR T hücreleri daha iyi çoğaldı, daha fazla mitokondri oluşturdu, yakıtı daha verimli yaktı, daha fazla kanser öldürücü molekül üretti ve özellikle CD58 eksik tümör hücreleriyle tekrarlanan meydan okumalarda apopitoza daha az yatkın oldu.
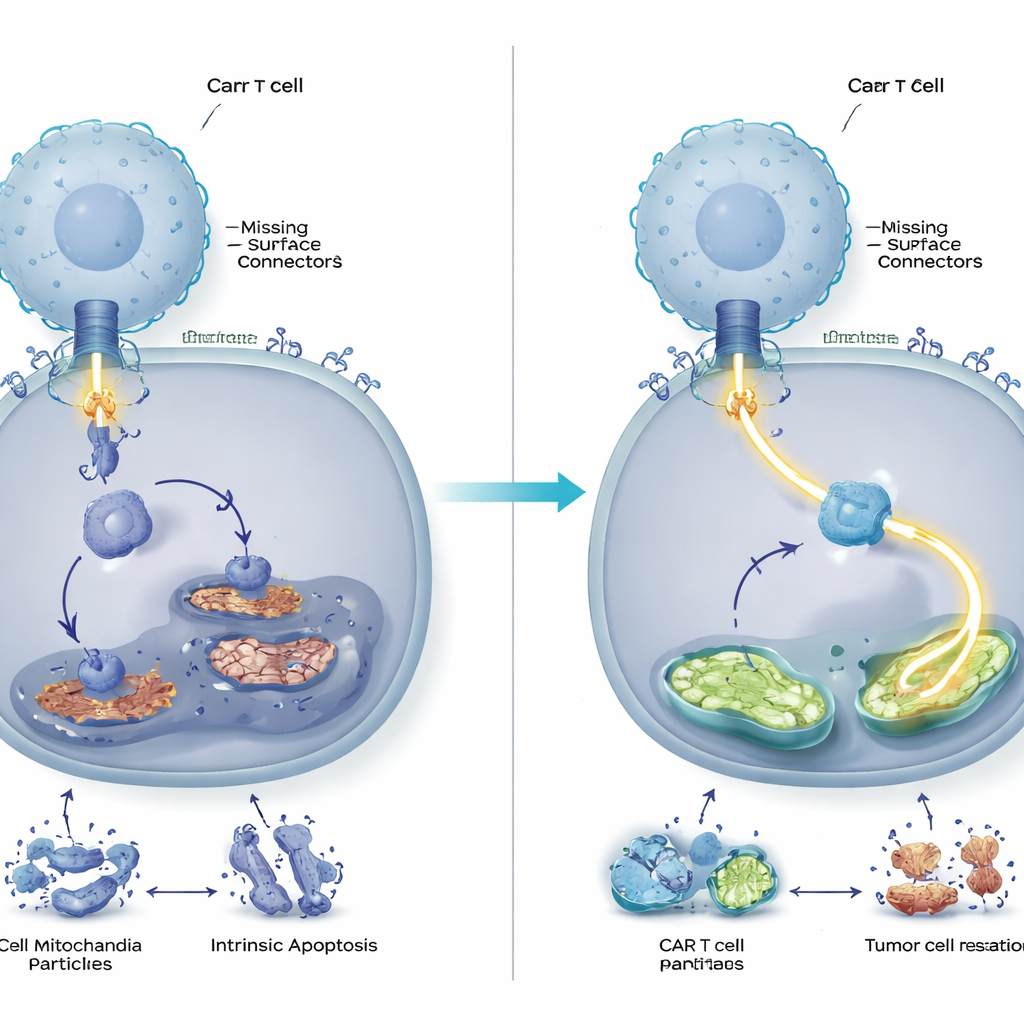
Hayvanlarda Daha Güçlü, Daha Uzun Süreli Tümör Kontrolü
Ekip daha sonra bu moleküler ayarın canlı sistemlerde fark yaratıp yaratmadığını test etti. CD58’i ya olan ya da olmayan insan kanser hücreleri taşıyan farelerde, DUSP6 eksik CAR T hücreleri tümörleri geleneksel CAR T hücrelerinden daha etkili temizledi ve daha uzun süre kontrol altında tuttu. Mühendislik yapılan hücreler daha güçlü çoğaldı, tükenme belirteçleri daha az görüldü ve önemli bağışıklık haberci moleküllerini daha yüksek seviyelerde salgıladı. DUSP6 kaldırılmasının yararları yalnızca tümörler CD58 kaybettiğinde değil, CD58’i koruduklarında da görüldü; bu da bu değişikliğin nadir bir tümör alt türü için sınırlı bir düzeltme olmaktan ziyade CAR T hücre terapilerini geniş çapta geliştirebileceğini düşündürüyor.
Hasta Verilerinden İpuçları
İnsanlardaki alaka düzeyini araştırmak için araştırıcılar CAR T hücreleri veya immün kontrol noktası ilaçları ile tedavi edilen kişilerin gen ifade verilerini inceledi. Çift hedefli bir CAR T terapisi alan diffuse large B‑cell lenfoma hastalarında, infüzyondan önce veya kısa süre sonra CD8 T hücrelerindeki daha düşük DUSP6 seviyeleri daha yüksek tam yanıt oranlarıyla ilişkilendirildi. Anti‑PD‑1 antikorları ile tedavi edilen ayrı bir deri kanseri kohortunda, yanıt vermeyenlerden izole edilen tükenmiş CD8 T hücreleri yanıt verenlerden daha fazla DUSP6 ifade etme eğilimindeydi. Birlikte bu gözlemler DUSP6’in farklı immünoterapiler genelinde T hücresi dayanıklılığının olumsuz bir göstergesi olarak hareket ettiğini ve düzeyinin azaltılmasının sonuçları iyileştirebileceğini öne sürüyor.
Gelecek Kanser Tedavileri İçin Anlamı
Günlük okuyucu için mesaj şudur: bazı tümörler CAR T hücre saldırısından yalnızca tanınmaktan kaçınarak değil, hücrelerin iç motorlarını sabote ederek de kaçıyor. Tümör hücrelerinde CD58 “tutacağı”nın kaybı, CAR T hücrelerinde AP-1 sinyalleşmesini sessizce düşürerek mitokondrilerini boşaltır, toksik yan ürünleri artırır ve erken hücre ölümüne doğru iteler. DUSP6 freni kaldırıldığında, bilim insanları bu kaybolan sinyali geri getirebilir, mitokondri sağlığını onarabilir ve CAR T hücrelerine dirençli tümörlere karşı bile daha fazla dayanıklılık ve öldürme gücü verebilir. Daha fazla güvenlik ve klinik testler gerekli olsa da, DUSP6 yokluğunun canlı kanser ilaçlarını daha güçlü, daha kalıcı ve muhtemelen daha geniş hasta popülasyonları için etkili kılacak ümit verici bir mühendislik stratejisi olarak ortaya çıktığı görülüyor.
Atıf: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Anahtar kelimeler: CAR T hücreleri, CD58, DUSP6, kanser immünoterapisi, T hücresi metabolizması