Clear Sky Science · tr
Kolorektal kanser foto-immunoterapisini güçlendirmek için bimetalik nanobomb aracılı STING yolunun bispesifik T hücresi aracısını artırma potansiyelinin açığa çıkarılması
Bağırsağın Kanserine Karşı Bağışıklık Sistemini Yeniden Harekete Geçirmek
Kolon ve rektum kanserleri yaygındır ve sıklıkla ölümcüldür; bunun bir nedeni tümörlerin bağışıklık sisteminden kaçmayı öğrenmeleridir. Bu çalışma, bir dizi kanserle mücadele yöntemini tek bir küçük “nanobomba” içinde toplayarak vücudun savunmasını uyandırmayı, bağışıklık hücrelerinin tümörü bulmasına yardımcı olmayı ve kanserin yeniden ortaya çıkmasını veya yayılmasını önlemeyi amaçlayan yeni bir stratejiyi araştırıyor.
Günümüzün Bağışıklık İlaçlarının Neden Geliştirilmesi Gerekiyor
Bispesifik T‑hücre aracıları olarak adlandırılan ve vaat eden bir ilaç sınıfı, biyolojik bir çöpçatan gibi çalışır: bir ucu bir T hücresine (önemli bir bağışıklık savaşçısı) tutunur, diğer uç ise tümör hücresindeki bir belirtece bağlanarak onları bir araya getirir ve T hücresinin öldürmesini sağlar. Kan kanserlerinde güçlü olsa da bu ilaçlar kolorektal kanser gibi solid tümörlerde zorlanır. Hızla vücuttan temizlenirler, aynı belirteci paylaşan sağlıklı dokulara saldırabilirler ve tedavinin etkili olması için yeterli bağışıklık hücresi bulunmayan “soğuk” tümörlerle sıkça karşılaşırlar. Bu nedenle doktorlar ve bilim insanları bu ilaçları daha güvenli şekilde teslim etmenin ve soğuk tümörleri etkin, aktive olmuş bağışıklık hücreleriyle dolu “sıcak” tümörlere dönüştürmenin yollarını arıyor.
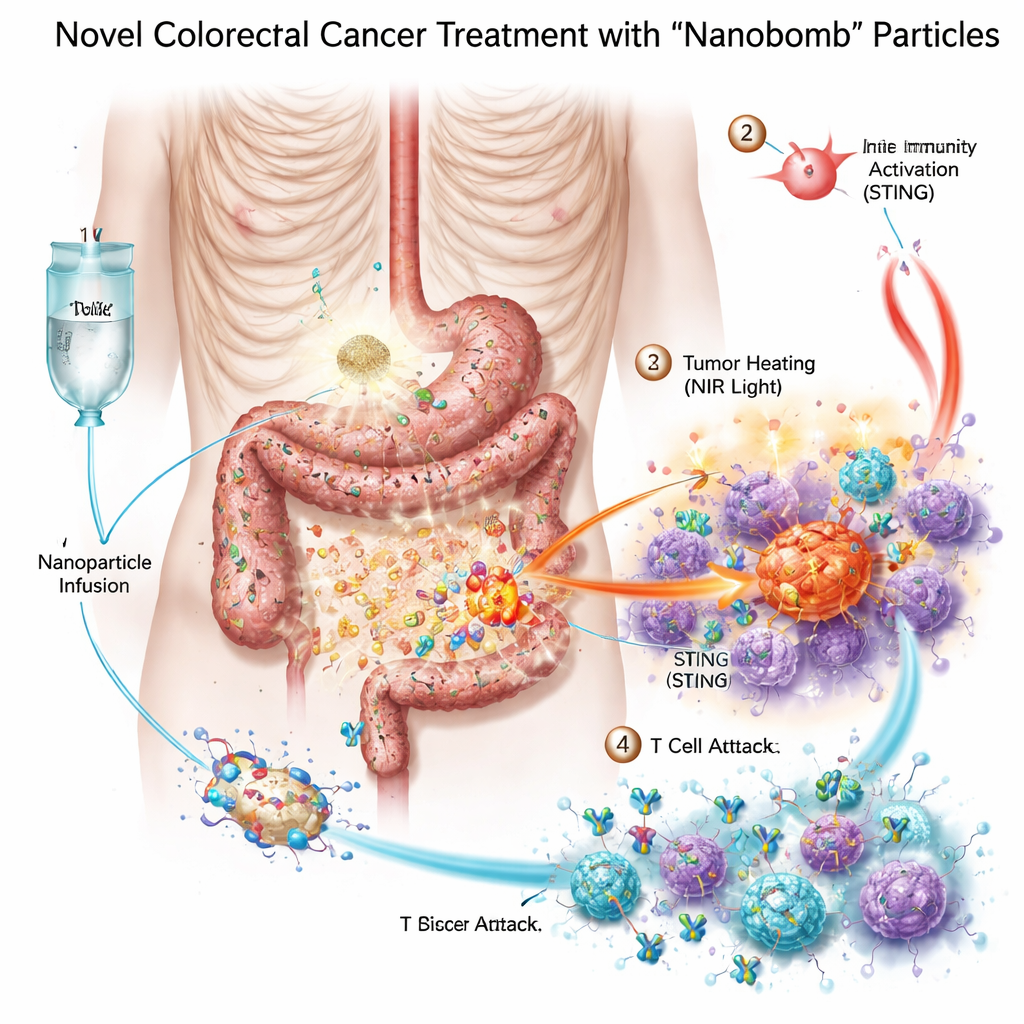
Üç Silahı Tek Bir Küçük “Nanobomba”ya Sığdırmak
Araştırmacılar, MnO2/Co‑DA@BiTE/HPT adıyla bilimsel olarak adlandırılan bimetalik bir nanobomba tasarladı; bu partikül üç tedavi modunu bir araya getiriyor. Öncelikle çekirdek, hücre içi bir alarm sistemi olan STING yolunu aktive edebilen mangan ve kobalt metallerini içeriyor; bu yol vücudun tehlikeyi algılamasına ve bağışıklık hücrelerini çağırmasına yardımcı olur. İkinci olarak, partikülün yüzeyi T hücrelerini kanser hücrelerine bağlayan bir bispesifik T‑hücre aracısı ile kaplanmış. Üçüncü olarak, malzeme yakın‑kızılötesi ışığı emerek hekimlerin tümörü dışarıdan ısıtmasına olanak tanıyan fototermal terapi sağlar. Nanobombaların kolorektal kanser hücrelerine yönelmesini sağlamak için ekip, PD‑L1’i tanıyan kısa bir DNA parçası olan bir aptamer ekledi; PD‑L1 bu tümörlerde sıklıkla bol miktarda bulunur. Bu parçacıklar tümöre ulaştığında, tümör dokusundaki doğal enzimler onları parçalayıp yüklerini tam olarak ihtiyaç duyulan yerde serbest bırakmaya yardımcı olur.
Isıtma, Alarm Verme ve Bağışıklık Ordusunu Çağırma
Laboratuvar kaplarında nanobombalar, tek bileşenlerden çok daha etkili bir şekilde kolorektal kanser hücrelerini öldürdü. Yakın‑kızılötesi ışıkla aydınlatıldıklarında partiküller ısındı, kanser hücrelerini strese soktu ve zarar verdi, ayrıca tümör hücrelerini daha fazla yaralayan yüksek reaktiviteye sahip reaktif oksijen türlerinin oluşumuna katkıda bulundu. Bu stres hücrelerin DNA’sını parçaladı ve tehlike sinyalleri gönderen özellikle görünür bir hücre ölümü biçimine itti. Yakındaki bağışıklık hücreleri, özellikle dendritik hücreler, ölen tümör materyalini yutup serbest kalan mangan ve kobaltın yardımıyla STING yolunu aktive etti. Ardından interferonlar ve T hücrelerini olgunlaştırıp çeken diğer iltihaplandırıcı habercileri ürettiler. Aynı zamanda nanobombanın üzerindeki bispesifik aracısı, T hücrelerini fiziksel olarak PD‑L1 pozitif tümör hücrelerine bağlayarak önceden soğuk olan tümörlerde bile T hücresi aktivasyonunu ve tümör öldürmeyi artırdı.
Tümör Küçülmesinden Kalıcı Bağışıklık Hafızasına
Subkütan kolorektal tümörler, vücudun iki tarafındaki tümörler, akciğer metastazları ve cerrahi sonrası nüks modeli dahil olmak üzere çeşitli fare modellerinde nanobombalar artı ışık tümör büyümesini güçlü bir şekilde yavaşlattı veya neredeyse durdurdu. Tedavi edilen tümörlerde kanser öldüren CD8 T hücreleri daha fazla, normalde bağışıklık tepkilerini baskılayan düzenleyici T hücreleri daha az bulundu. Tümör içindeki ve lenf düğümlerindeki dendritik hücreler olgunlaşma belirtileri gösterdi ve kan testleri bağışıklık uyaran sitokin seviyelerinde artış olduğunu ortaya koydu. Önemli olarak nanobomba tedavisinden sonra tümörlerini temizleyen fareler, kanser tekrar verildiğinde daha iyi korundu ve daha az akciğer metastazı geliştirdi; bu, terapinin yalnızca tek seferlik tümör küçülmesi sağlamaktan öte kalıcı bağışıklık hafızası inşa etmeye yardımcı olduğunu gösteriyor.
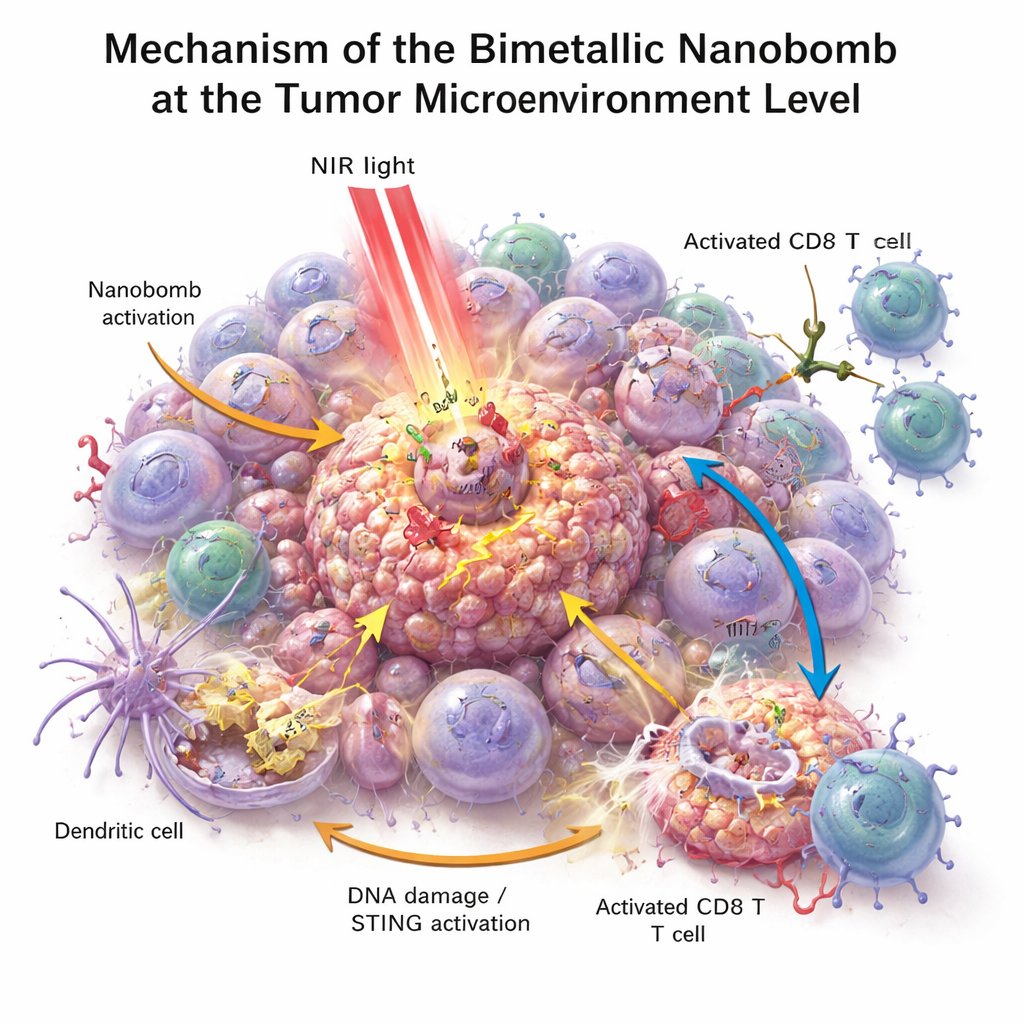
Geleceğin Kanser Bakımı İçin Ne Anlama Gelebilir
Bu çalışma, bir parçacık içinde tümörleri ısıtan, içsel bir tehlike alarmını açan ve T hücrelerini doğrudan kanser hücrelerine yönlendiren “üçlü darbe” nanomedikal bir yaklaşımı tanıtıyor. Farelerde bu yaklaşım yalnızca soğuk kolorektal tümörleri sıcak, iltihaplı hale getirmekle kalmadı, aynı zamanda nüksü ve yayılmayı da önlemeye yardımcı oldu. Teknoloji klinik kullanımdan hâlâ uzak olsa da—ölçeklendirme, uzun vadeli güvenlik ve insanlarda test edilme gibi büyük zorluklar var—bu, akıllı malzemeleri bağışıklık ilaçlarıyla harmanlayarak hastalara daha güçlü ve daha dayanıklı bir antikanser cevap vermeyi hedefleyen gelecekteki tedaviler için bir taslak sunuyor.
Atıf: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Anahtar kelimeler: kolorektal kanser, immünoterapi, nanoparçacıklar, STING yolu, bispesifik T hücresi aracısı