Clear Sky Science · tr
Bireyselleştirilmiş farmakokinetik–farmakodinamik yönlendirmeli tedavi: iPS hücre kaynaklı çoklu organoid platformu ile NF1-mutant meme kanseri
Bu araştırma hastalar için neden önemli
Birçok kanser hastası, bazı kişilerde iyi çalışan fakat bazılarında etkisiz olan ve sıklıkla ağır yan etkilere yol açan ilaçlar alıyor. Bu çalışma, hastanın kendi hücrelerinden laboratuvarda yetiştirilen mini organlar kullanarak vücut dışında kanser tedavilerini test etmenin yeni bir yolunu tanımlıyor. Araştırma, NF1 adlı gendeki değişikliklerin yönlendirdiği ve tedavisi zor bir meme kanseri biçimine odaklanıyor ve bir gen düzeltme stratejisi ile hedefe yönelik bir ilacın birleşiminin daha güvenli, daha etkili ve gerçekten kişiye özel bir tedaviye yol açabileceğini gösteriyor.
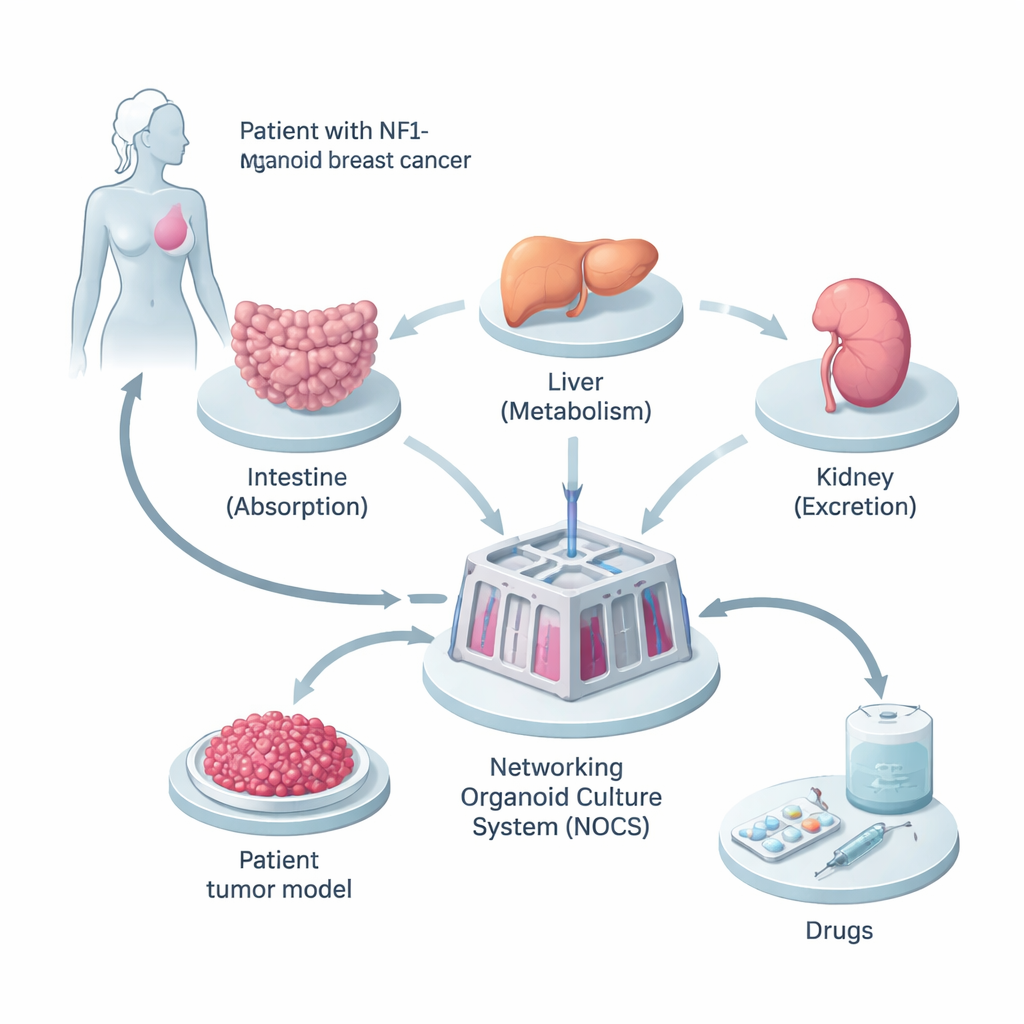
Hastanın vücudunun mini bir versiyonunu oluşturmak
Araştırmacılar, meme kanserinde kalıtsal bir NF1 mutasyonu taşıyan bir kadından alınan doku ile başladılar. Hastanın normal deri benzeri hücrelerini indüklenmiş pluripotent kök hücrelere dönüştürdüler; bu hücreler vücuttaki hemen hemen her hücre tipine dönüşebilir. Bunlardan, ilacın emildiği, işlendiği ve atıldığı başlıca yerler oldukları için ince bağırsak, karaciğer ve böbreğin üç tür mini organını büyüttüler. Paralel olarak, orijinal tümörde bulunan hücre türleri karışımını ve genetik değişiklikleri koruyan 3B tümör “sferoidleri”ni hastanın kanser hücrelerinden oluşturdular.
Canlı bir ilaç-test devresi
Bu mini-organların gerçek bir vücut gibi davranmasını sağlamak için ekip, onları Networking Organoid Culture System (NOCS) adlı sıvı dolu bir cihazda birbirine bağladı. Bu düzende, ortam sıvısı ince bağırsak, karaciğer, böbrek ve tümör bölümleri arasında akar; kan dolaşımını taklit eder. İlaçlar, hap yutmayı ya da enjeksiyon almayı andıran biçimde eklenebilir; sensörler ve pompalar “kanın” ne kadar hızlı aktığını ve ne sıklıkla yenilendiğini kontrol eder. Bu sayede bilim insanları, bir ilacın ne kadarının emildiğini, ne kadar hızlı parçalandığını ve tümör üzerinde ne kadar güçlü etki gösterdiğini—hepsini hasta özgü, insan kaynaklı bir modelde—izleyebildiler.
Exon atlama ile bozuk bir geni düzeltmek
Hastanın tümörü, büyüme yollarını sürekli açık tutan ve birçok standart ilacı etkisiz kılan yıkıcı bir NF1 mutasyonu taşıyordu. Ekip, antisent oligonükleotidler adı verilen kısa genetik materyal parçaları tasarladı; bunlar hücrenin RNA işleme mekanizmasını NF1 geninin hatalı parçası (ekson 2) üzerinde atlama yapmaya zorladı. Günlerce etkin kalan viral bir taşıyıcı kullanarak hastanın kanser hücrelerinde kalıcı bir “ekson atlama” indüklediler. Bu, daha kısa ama fonksiyonel bir NF1 proteini üretip aşırı aktif büyüme sinyallerini azalttı ve tümör hücrelerini tedaviye daha duyarlı hale getirdi.
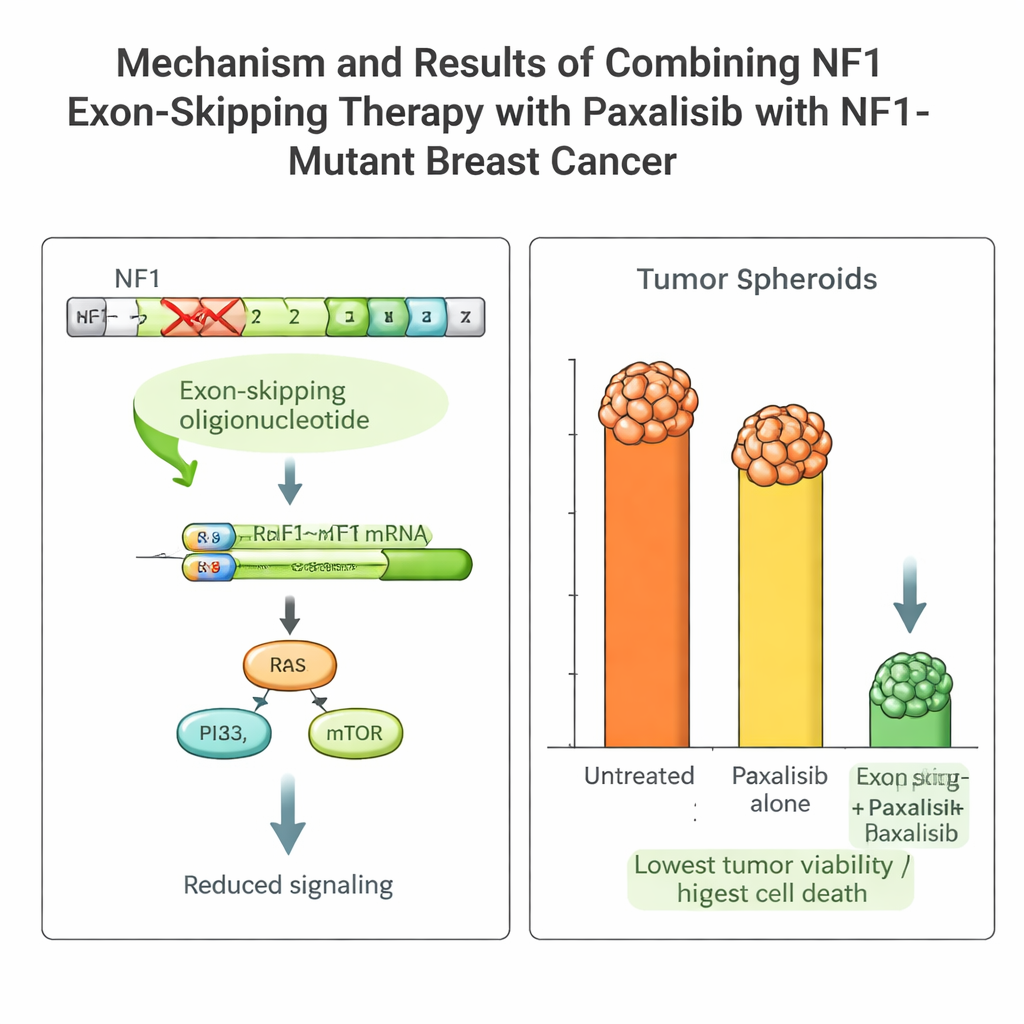
PK/PD rehberliğinde doğru hedefe yönelik ilacı seçmek
Bu platformla donanmış olarak, ekip NF1’in altında yer alan PI3K–mTOR yolunu engelleyen birkaç gelişmiş ilacı karşılaştırdı. Hem farelerde hem de NOCS’te farmakokinetik (vücudun ilacı nasıl işlediği) ve farmakodinamik (ilacın tümör üzerindeki etkisi) ölçümleri yapıldı. Paxalisib adlı bir ilaç öne çıktı: bağırsakta iyi emiliyor, sistemde işe yarar seviyelerde kalıyor ve hayvanlar ile organoid cihazında benzer davranış sergiliyordu. NF1 ekson atlaması ile birlikte kullanıldığında, Paxalisib’in hastanın tümör hücrelerine karşı öldürücü etkisi dramatik biçimde arttı; hem NOCS’te hem de hastanın tümörünü taşıyan farelerde büyümede güçlü azalmalar ve programlı hücre ölümü belirtileri görüldü.
Organlar arasında yarar ve riski dengelemek
İnce bağırsak, karaciğer ve böbrek modelleri aynı devrenin parçası olduğundan, araştırmacılar erken organ hasarı belirtilerini de izleyebildiler. Paxalisib bağırsak ve böbrek modellerinde stres yanıtları ve ince bariyer zayıflamaları ile karaciğerde gerilim işaretleri oluşturdu, ancak test edilen dozda hücre canlılığında belirgin bir kayıp gözlenmedi. Bu tür bir tüm vücut görünümü, insan dokusu kullanarak, tedavi seçeneklerini yalnızca tümörleri ne kadar küçülttüklerine göre değil, aynı zamanda bir ilaç hastaya ulaşmadan önce sağlıklı organları nasıl etkileyebileceğine göre de karşılaştırma imkânı sunuyor.
Gelecekteki kanser bakımına ne anlam ifade edebilir
Basitçe söylemek gerekirse, bu çalışma artık basitleştirilmiş, hasta özgü bir “çip üzerindeki mini vücut” yetiştirmenin ve farklı ilaçların—hatta gen-düzeltici yaklaşımların—nasıl davranacağını ve birbirleriyle nasıl etkileşeceğini test etmenin mümkün olduğunu gösteriyor. Bu NF1-mutant meme kanseri hastası için en uygun strateji, NF1 ekson atlama terapisi ile ağızdan alınan Paxalisib’in kombinasyonu oldu; birlikte kullanıldıklarında tümör büyümesini tek başlarınakinden çok daha fazla yavaşlattılar. Daha fazla geliştirilip daha fazla hastada test edilirse, bu tür platformlar doktorlara her kişinin genleri ve biyolojisine göre uyarlanmış tedavi planları yönünde rehberlik edebilir; başarı şansını artırırken gereksiz toksisiteyi azaltabilir.
Atıf: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Anahtar kelimeler: bireyselleştirilmiş onkoloji, meme kanseri, organoidler, NF1 mutasyonu, hedefe yönelik tedavi