Clear Sky Science · tr
Yumurtalık kanserinde immünoterapinin etkinliğini artırmak için omental metastazlarda lipid kaynaklı immünometabolik yolları kullanmak
Yumurtalık kanseri için karın çevresindeki yağ neden önemli?
Yumurtalık kanseri sıklıkla omentum adı verilen karında yağlı bir doku önlüğüne yayılır. Bu bölge yağ hücreleri ve bağışıklık hücreleri açısından zengindir ve yalnızca pasif bir seyirci olmaktan çok daha fazlasıdır. Burada özetlenen çalışma, bu omental birikimlerde bağışıklık hücrelerinin yağı nasıl kullandığını ve işlediğini göstererek modern immünoterapilerden yalnızca küçük bir hasta grubunun neden yarar gördüğünü açıklamaya yardımcı oluyor. Ayrıca bu tedavileri daha fazla kişide işe yarar hâle getirebilecek yeni ilaç kombinasyonları ve görüntüleme temelli testleri de işaret ediyor.
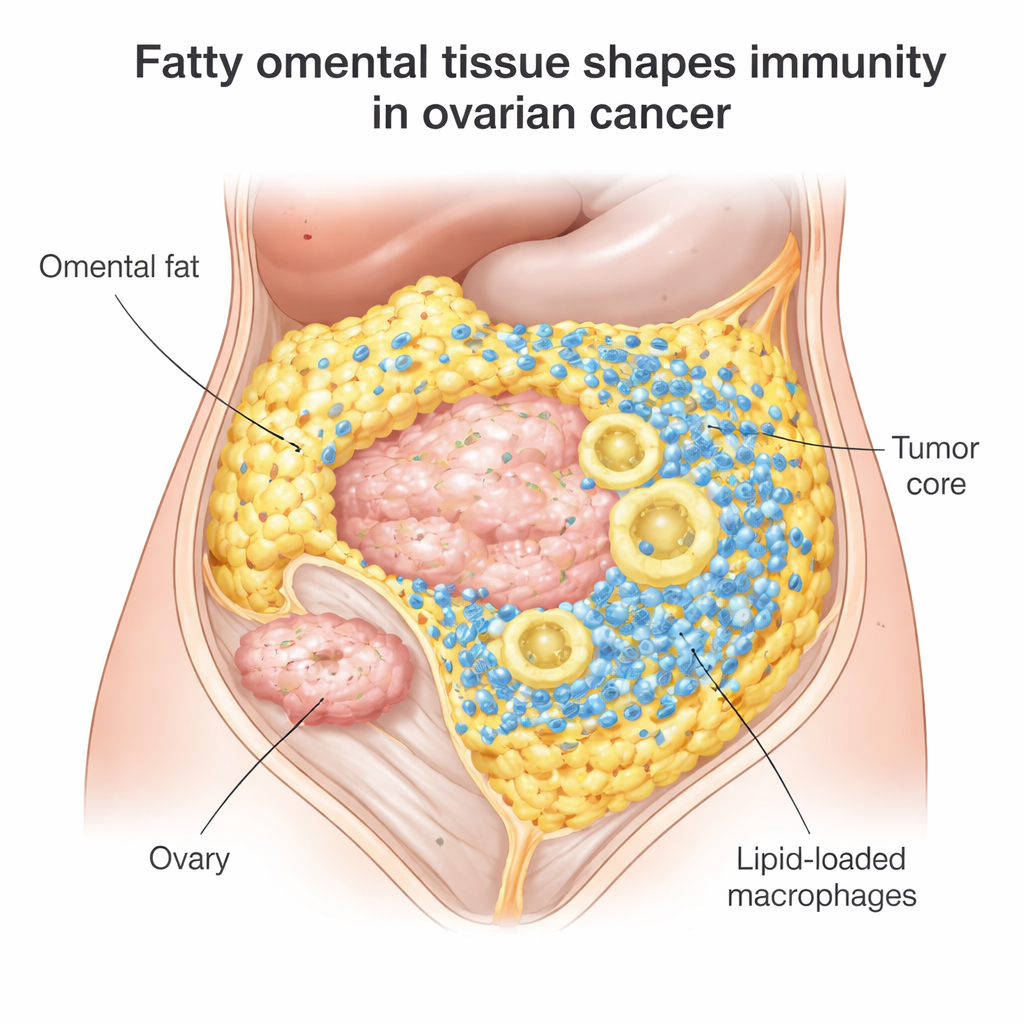
Karın yağında gizli bir savaş alanı
Epiteliyal yumurtalık kanseri olan çoğu kadın başlangıçta cerrahi ve kemoterapiye yanıt verir, ancak %70–80’inde hastalık yeniden ortaya çıkar ve nivolumab veya pembrolizumab gibi immün kontrol nokta ilaçları yalnızca yaklaşık %10–15’inde fayda sağlar. Araştırmacılar, yumurtalık kanserinin yağ hücreleri arasında yayılmaya eğilimli olduğu yaygın bir yer olan omental metastazlara odaklandı. 100’den fazla tümör örneğini incelediklerinde, omental tümörlerin bağışıklık hücreleriyle dolu olduğunu buldular: kanseri hedef alabilen öldürücü T hücreleri ve büyük “temizleyici” hücreler olan makrofajlar. Ama bir sorun vardı. Bu T hücreleri, en çok ihtiyaç duyulan tümör çekirdeğine nüfuz etmek yerine tümör ile yağ arasındaki sınırda kümelenme eğilimindeydi.
Bazı bağışıklık hücrelerini besleyen ama diğerlerini bunaltan yağ
Daha derine inildiğinde, ekibin yağlı bu tümörlerdeki T hücrelerinin yakınlardaki yağ hücrelerinden lipid yani yağ alarak yerel ortama uyum sağladıklarını gösterdi. Bu, onların metabolik olarak "formda" kalmasına benziyor: gen etkinlikleri ve laboratuvar testleri, hastanın kendi tümör hücrelerini tanıyıp öldürebilecek yetenekte olduklarını gösterdi. Aynı zamanda, omentumdaki birçok tümörle ilişkili makrofaj yağ damlacıklarıyla ağır biçimde doluydu. Bu lipid dolu makrofajlar, reaktif oksijen türleriyle bağlantılı kimyasal stresin bir göstergesi olan yüksek oksidatif stres belirtileri gösterdi ve bağışıklığı baskılayan, tümörü destekleyen bir duruma kaydılar. Başka bir deyişle, etkili T hücrelerini besleyebilen aynı yağ açısından zengin ortam, makrofajları zararlı bir moda iterek genel bağışıklık saldırısını zayıflatıyor.
Aşırı beslenmiş makrofajları mevcut ilaçlarla yeniden programlamak
Bilim insanları daha sonra bu stres altındaki makrofajları müttefiklere çevirip çeviremeyeceklerini sordular. Laboratuvarda yetiştirilen taze tümör parçacıklarını kullanarak iki yaklaşımı test ettiler. Birincisi, tümör–yağ sınırında bol bulunan immün sinyal CCL5 için bir reseptör olan CCR5’i engelleyen HIV ilacı maravirocu içeriyordu. Diğeri ise makrofajların yağ asitlerini içeri almasını sağlayan önemli bir “temizleyici” reseptör olan CD36’yı engelledi. Her iki tedavi de makrofaj içindeki yağ yükünü azalttı, oksidatif stres ve zararlı lipid peroksidasyon göstergelerini düşürdü ve dalgalar halinde inflamatuar sinyallerin serbest kalmasını sağladı. Kritik olarak, bunlar öldürücü T hücrelerin çoğalmasına ve yağlı kenardan tümör çekirdeğine geçmesine izin vererek dışarıdan ekstra bağışıklık hücresi eklemeden lokal bağışıklık aktivitesini güçlendirdiler.
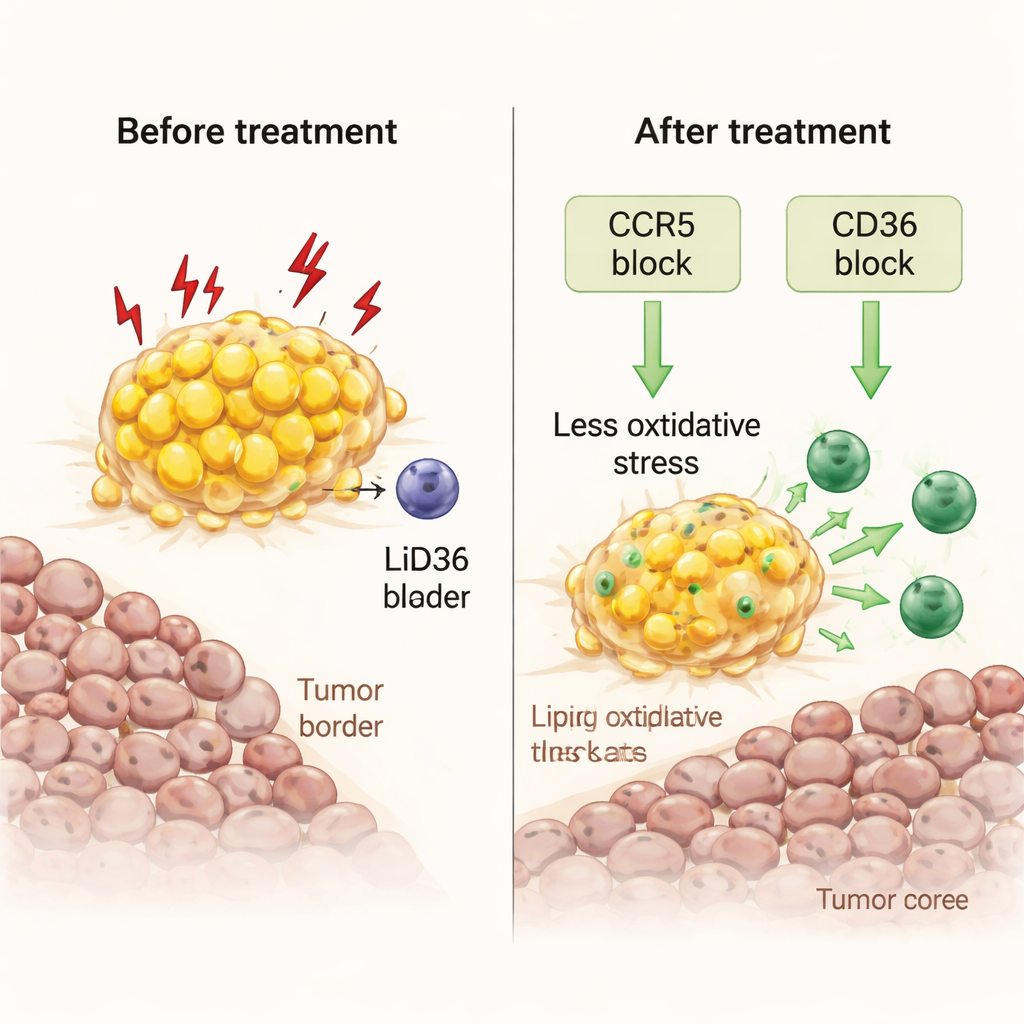
Hücresel yollardan gerçek dünya modellerine ve hastalara
Bu fikirleri daha gerçekçi bir ortamda test etmek için ekip, insan benzeri bir bağışıklık sistemine sahip olacak şekilde insanlaştırılmış fareler kullandı ve yağ açısından zengin dokuya insan meme kanseri yerleştirdi. Maraviroc tedavisi bu hayvanlardaki insan makrofajlarını hasta kaynaklı örnekleri yansıtan şekillerde yeniden programladı: azalmış lipid ve stres imzaları, artan sitokin üretimi ve T hücre ilişkili yollar için daha güçlü destek. Klinik olarak, araştırmacılar kemoterapiye dirençli yumurtalık kanseri için yapılan Japon bir nivolumab denemesini yeniden inceledi. İlacı alan ve yarar gören her hastanın cerrahi örneklerinde omental metastazlar görünüyordu. BT veya MRG görüntüleri ile vücut yağ dağılımının makine öğrenimi analizi birleştirilerek, tümörlerin visceral yağa yakın olma olasılığını invaziv olmayan biçimde işaretleyebilen bir karar ağacı oluşturuldu—ve bir prospektif vakada bu yöntem daha sonra nivolumaba yanıt veren bir hastayı doğru şekilde öngördü.
Gelecekteki tedavi için bunun anlamı ne olabilir?
Uzman olmayan bir kişi için çıkarılacak mesaj şudur: yumurtalık kanserinin vücutta "nerede" büyüdüğü ve yakınındaki yağın bağışıklık hücrelerini nasıl şekillendirdiği, immünoterapinin işe yarayıp yaramayacağını güçlü biçimde etkileyebilir. Yağ açısından zengin omental birikimler, canlı T hücreleri barındırıyor gibi görünürken aynı zamanda saldırıyı bastıran aşırı beslenmiş, stres altındaki makrofajları da barındırıyor. Bu makrofajlardaki lipid yükünü hafifletip oksidatif sıkıntılarını azaltarak—maraviroc gibi CCR5 blokerleri, CD36 hedefli ajanlar veya benzeri stratejiler kullanılarak—kısmi bloke olmuş bir bağışıklık yanıtı tümör üzerinde tam ölçekli bir saldırıya dönüştürülebilir. Aynı zamanda, omental tutulumu görüntüleme temelli ölçümleri, hangi hastaların immün kontrol nokta ilaçlarından en çok yararlanma olasılığında olduğunu seçmede doktorlara yardımcı olabilir ve yumurtalık kanserinin tedavisinde daha kişiselleştirilmiş ve potansiyel olarak daha etkili bir yaklaşım getirebilir.
Atıf: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Anahtar kelimeler: yumurtalık kanseri, omentoal yağ, immünoterapi, tümörle ilişkili makrofajlar, lipid metabolizması