Clear Sky Science · tr
KARDİYOMİOSİTLERDE KLF15 aktivitesinin artırılması: nükleaz-defektif dCas9VPR ile patolojik yeniden programlamayı ve fibrozisi önlemenin yeni bir yaklaşımı
Yetmezlik Gelişen Kalbin Yeniden Programlanması
Kalp yetmezliği milyonlarca insanı etkiler ve genellikle yıllarca yüksek tansiyon veya kapak hastalığı sonrasında yavaşça gelişir. Bu koşullarda kalp kası hücreleri yalnızca daha büyük olmakla kalmaz, aynı zamanda "fetal" bir gen programını etkinleştirir ve kalp yara dokusuyla dolar. Bu çalışma, kalbin kendi gen denetim mekanizmasını DNA’yı kesmeden nazikçe sağlığa doğru geri yönlendirmeyi —kardiyomiyositlerde KLF15 adı verilen koruyucu bir düzenleyiciyi kademeli olarak artırarak— araştırıyor.
Kalp Hücreleri Kimliklerini Kaybettiğinde
Sağlıklı yetişkin bir kalpte, kardiyomiyositler —kalp kası hücreleri— enerji için yağları verimli şekilde yakar ve sabit bir gen aktivitesi düzenini korur. Kronik basınç yüküne maruz bırakılan farelerde tek hücreli RNA dizileme kullanarak araştırmacılar, kalbin normal işlevden genişlemeye ve nihayetinde yetmezliğe geçişinde bireysel kardiyomiyositlerin nasıl değiştiğini haritaladılar. Metabolizma ve büyümeyi dengede tutan KLF15 adlı bir transkripsiyon faktörünün hasta hücrelerde en belirgin aktivite değişimini gösterdiğini buldular. Stres arttıkça KLF15 seviyeleri düştü ve fetal ile strese bağlı genleri baskılama yeteneği zayıfladı. Benzer KLF15 düşüşleri dilate ve hipertrofik kardiyomiyopati hastalarından alınan insan kalplerinde de gözlendi; bu durum, bu bozulmanın türler arasında korunmuş olduğunu gösteriyor.
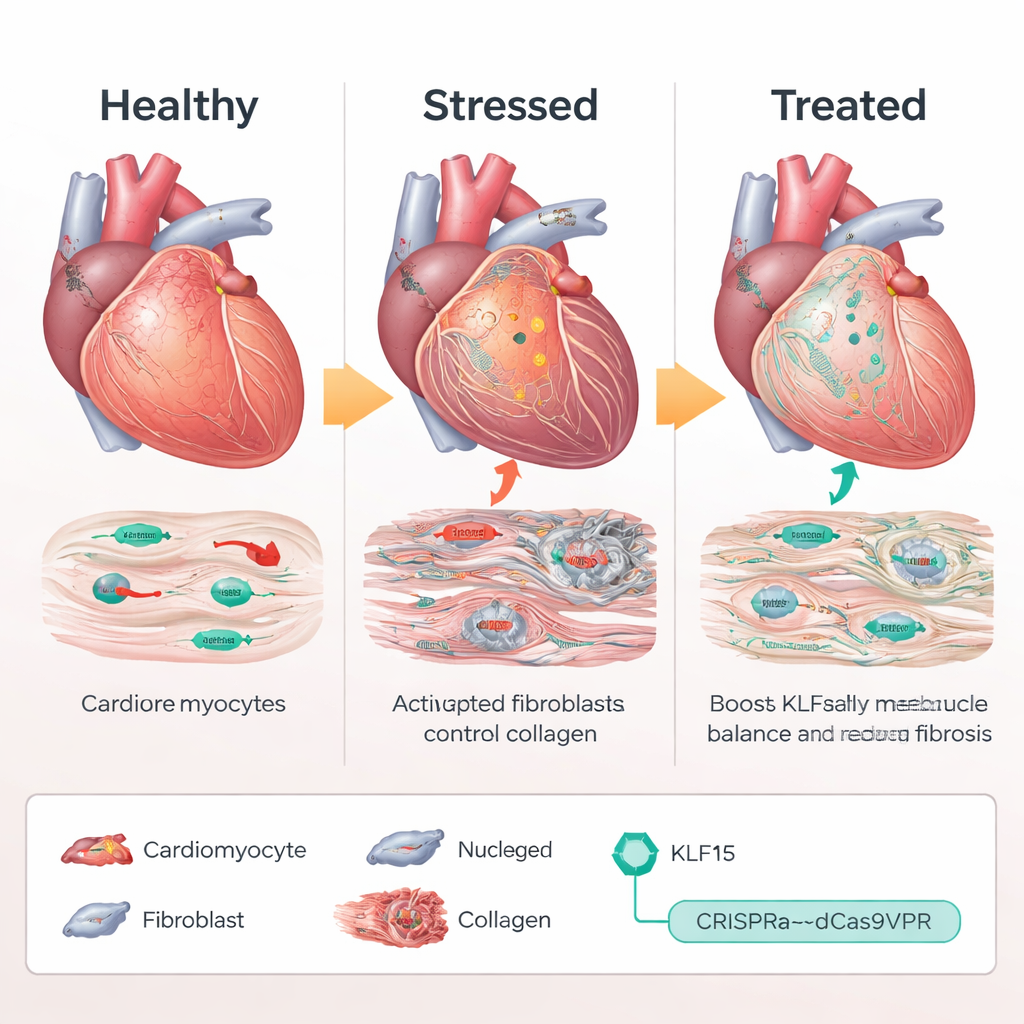
CRISPR’ı Makas Değil, Ses Düğmesi Olarak Kullanmak
KLF15 geninin fazladan bir kopyasını eklemek veya DNA’yı kesmek yerine ekip, doğal Klf15 geninin yakınında bağlanıp onun kendi ifadesini artıran dCas9VPR adında CRISPR tabanlı bir “aktivasyon” sistemi kullandı. Bu CRISPR aktivatorünü yalnızca kardiyomiyositlerde ifade edecek şekilde tasarlanmış farelerde, araştırmacılar Klf15 promotörünü hedeflemek için kılavuz RNA’ları adeno-ilişkili bir virüs (AAV9) ile verdiler. Kronik basınç yükü altında Klf15’i aktive eden kılavuzlar verilen farelerde Klf15 seviyeleri neredeyse normal düzeylerde korundu. Kalp kası hücreleri daha küçük kaldı, pompalama fonksiyonu daha az düştü ve kontrol hayvanlarına kıyasla sağkalım iyileşti. Moleküler düzeyde stres ve fetal genler susturuldu, metabolik ve kalsiyum-handling genleri geri döndü; bu da sağlıksız transkripsiyonel programın büyük ölçüde sıfırlandığını gösteriyor.
Hücreden Hücreye İletişimle Yara Oluşumunu Susturmak
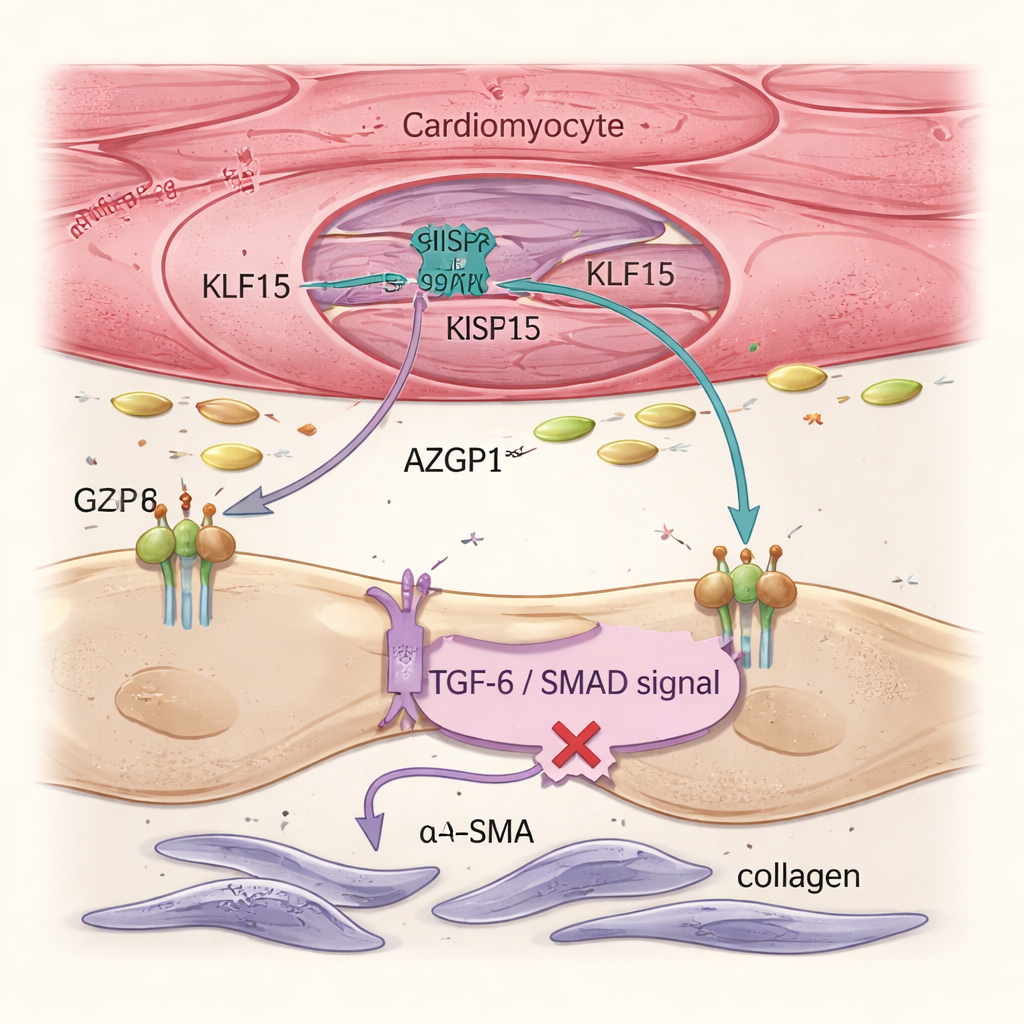
Kalp yetmezliği yalnızca hasta kas hücreleri tarafından değil, aynı zamanda kollajen üreten ve sert skar dokusu oluşturan destek hücreleri olan fibroblastlar tarafından da yönlendirilir. Tek hücre analizleri ve doku görüntülemesi, kardiyomiyositlerde Klf15’in yeniden sağlanmasının fibroblast aktivasyonunu ve genel fibrozisi azalttığını gösterdi; oysa gen terapisi doğrudan fibroblastları hedeflemiyordu. Ekip bu etkiyi AZGP1 adlı salgılanan bir proteine bağladı. Klf15 kardiyomiyositlerde artırıldığında AZGP1 üretimi ve salınımı yükseldi. Hem fare kalplerinde hem de insan kökenli kök hücreden elde edilmiş kalp dokularında daha yüksek AZGP1, fibroblastlarda skarlaşmanın ana sürücüsü olan TGF-β / SMAD yolunu baskıladı ve α-SMA ile POSTN gibi belirteçlerin düzeylerini düşürdü. Önemli olarak, yalnızca kardiyomiyositlerde AZGP1 aşırı eksprese edilmesi kas hücrelerini yeniden programlamadı; bu da KLF15’in öncelikle kardiyomiyositleri doğrudan koruduğunu ve fibroblastları sınırlamak için AZGP1’i bir haberci olarak kullandığını gösteriyor.
İnsan Doku Modelleri Koruyucu Devreyi Doğruluyor
Bu mekanizmaların insan hücrelerinde de geçerli olup olmadığını sınamak için araştırmacılar, üç boyutlu mühendislik ürünü kalp dokularında yetiştirilen indüklenmiş pluripotent kök hücre kaynaklı kardiyomiyositleri kullandılar. Yüksek tansiyonu taklit eden mekanik yük uygulandığında bu dokular KLF15’ini kaybetti, stres ve fetal genleri açtı, sertleşti ve kasılmaları zayıfladı —hastalığın özelliklerini yeniden yarattı. CRISPRa aracılı KLF15 restorasyonu bu düşüşü engelledi, kuvvet üretimini korudu ve gen ifadesini olgun metabolizma ve yapıya doğru geri kaydırdı. Ayrıntılı deneyler, yaygın bilinen pro-fibrotik sinyal TGF-β1’in insan kardiyomiyositlerinde SMAD2/3 yolu aracılığıyla KLF15’i azalttığını gösterdi; bu, kronik stresin uyumsuz yeniden şekillenmeye nasıl yol açtığını açıklamaya yardım eder. Son olarak ekip, tek bir AAV9 vektörüne sığan daha küçük bir Cas9 varyantına dayalı kompakt bir "mini" CRISPRa sistemi mühendislik etti ve bu sistem kardiyomiyosite özgü bir promotörle sürüldü. Yetmez kalp dokusunun hassas kesitlerinde bu vektör KLF15 seviyelerini başarılı şekilde yükseltti ve kültürde günler içinde kasılma performansını iyileştirdi.
Daha Nazik Gen Terapisi için Bir Plan
Uzman olmayanlar için temel mesaj şudur: bu çalışma, kalp kası hücreleri içinde tek bir koruyucu düzenleyiciyi dikkatlice artırmanın hem onların kimliğini stabilize edebileceğini hem de yara oluşumunu sınırlayan sinyaller gönderebileceğini gösteriyor. DNA’yı kesmeyen CRISPR tabanlı bir aktivator kullanarak, yaklaşım yapay bir geni eklemek yerine kalbin kendi genini ince ayarla düzenliyor. Çalışma, mekanik stresi zararlı yeniden şekillenmeyle ilişkilendiren TGF-β → KLF15 → AZGP1 yolunu tanımlıyor ve farelerde, insan hücre modellerinde ve insan kalp doku dilimlerinde KLF15’in yeniden sağlanmasının bu zincirleme reaksiyonu kesebileceğini gösteriyor. Hâlâ preklinik aşamada olmakla birlikte, burada sunulan kompakt, kardiyomiyosite hedeflenen CRISPRa sistemi, genomu yeniden yazmak yerine gen aktivitesini yeniden programlayarak yaygın, genetik olmayan kalp yetmezliği formlarının tedavisi için potansiyel bir yol haritası sunuyor.
Atıf: Schoger, E., Kim, R., Bleckwedel, F. et al. Enhancing KLF15 activity in cardiomyocytes: a novel approach to prevent pathological reprogramming and fibrosis via nuclease-deficient dCas9VPR. Sig Transduct Target Ther 11, 76 (2026). https://doi.org/10.1038/s41392-026-02593-9
Anahtar kelimeler: kalp yetmezliği, KLF15, CRISPR aktivasyonu, kardiyak fibrozis, AZGP1