Clear Sky Science · tr
GPR54, dopa dekarboksilaz aracılığıyla küçük hücre dışı akciğer kanseri gelişimini düzenler
Bu akciğer kanseri öyküsünün önemi
Akciğer kanseri hâlâ en öldürücü kanser türlerinden biridir ve vakaların çoğu küçük hücre dışı akciğer kanseri (KHDAK) adı verilen biçimdedir. Birçok hasta, tümörler mevcut ilaçlara uyum sağladığı veya direnç geliştirdiği için sonunda etkili tedavi seçeneklerini tüketir. Bu çalışma, GPR54 adlı bir reseptör ve dopa dekarboksilaz (DDC) adlı bir enzim etrafında toplanan, akciğer kanseri hücrelerinin içinde daha önce yeterince takdir edilmemiş bir kontrol sistemini ortaya koyuyor. Bu moleküllerin tümörlerin büyümesine ve kendilerini beslemesine nasıl yardımcı olduğunu anlayarak, araştırmacılar KHDAK’yı yavaşlatmanın veya küçültmenin yeni yollarına işaret ediyor.
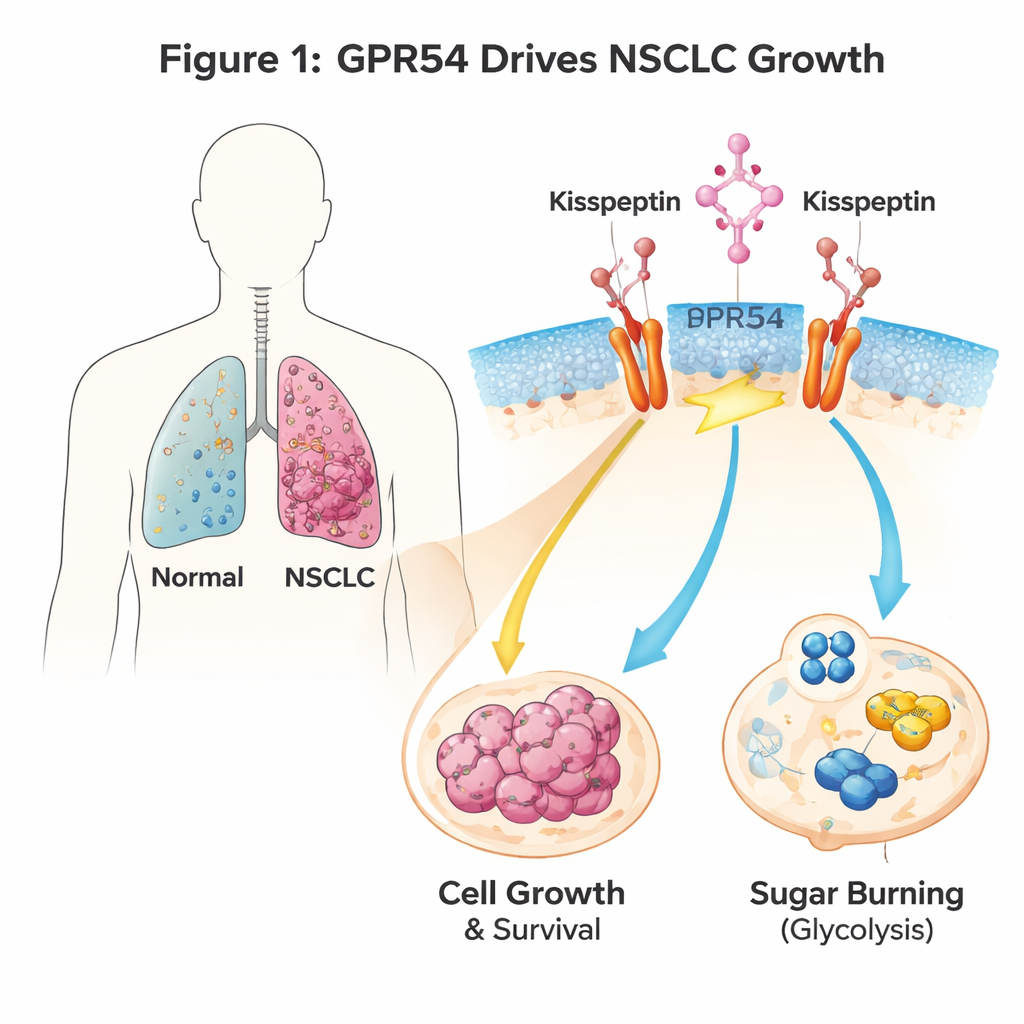
Akciğer kanseri hücrelerindeki bir sinyal anahtarı
GPR54, hücre yüzeyinde yer alan ve kisspeptin adlı doğal bir sinyale yanıt veren bir algılayıcıdır. En çok ergenlik ve üreme süreçlerindeki rolleriyle bilinir, ama birçok kanserde de ortaya çıkar. Yazarlar, Kras adlı kanser yapıcı bir gen akciğer hücrelerinde etkinleştirildiğinde KHDAK gelişen genetik olarak tasarlanmış fareler kullandı. Bu farelerde Gpr54 geni silindiğinde hayvanlar daha uzun yaşadı, daha az ve daha küçük akciğer tümörleri gelişti ve kanser hücreleri belirgin hücre intiharı (apoptoz) belirtileri gösterdi. İnsan KHDAK hücre hatları da aynı öyküyü anlattı: GPR54 düzeyleri azaltıldığında tümör hücreleri daha yavaş büyüdü, daha az koloni oluşturdu ve belirli genetik mutasyonlarından bağımsız olarak daha kolay öldü.
GPR54, tümör hücrelerini nasıl hayatta tutuyor?
Daha derine indiklerinde, araştırmacılar GPR54’ün hangi iç devreleri kullandığını sordular. GPR54’ün hücre içindeki iki büyük büyüme yoluna, AKT ve ERK’e bağlandığını buldular. Her ikisi de kanser hücrelerine bölünme ve ölümden kaçınma talimatı veren yaygın "kablolama merkezleri"dir. GPR54 engellendiğinde veya kaldırıldığında AKT ve ERK aktiviteleri düştü ve hücreler apoptoza daha yatkın hale geldi. Güçlü AKT veya ERK sinyallerinin geri getirilmesi hücreleri kısmen kurtarabildi; bu da GPR54’ün KHDAK hücrelerinin hayatta kalmasına bu büyüme devrelerine dayanarak yardımcı olduğunu doğruluyor.
Kanserin şekeri kullanma biçimini yeniden bağlamak
Kanser hücreleri genellikle besinleri kullanma biçimlerini yeniden programlayıp hızlı şeker yıkımını (glikoliz) büyümeyi desteklemek için tercih eder. Gpr54 eksik olan fare tümörlerinin gen aktivite profillemesi, şeker işleme ve enerji üretimiyle ilişkili birçok genin aşağı düzenlendiğini gösterdi. GPR54’ü etkinleştirmek için kisspeptin ile muamele edilen akciğer kanseri hücrelerinde oksijen kullanımı ve asit üretimi ölçümleri — enerji metabolizması için vekiller — GPR54’ün glikolizi artırdığını ortaya koydu. Gαq/11 anahtarı, PI3K, AKT veya mTOR gibi GPR54 yolunu çeşitli basamaklarda bloke etmek glukoz tüketimini ve laktat üretimini azalttı ve hücreleri apoptoza itti. Basitçe söylemek gerekirse, GPR54 KHDAK hücrelerinin şekeri daha hızlı ve verimli yakmasına yardımcı olarak hızlı büyümelerini destekliyor.
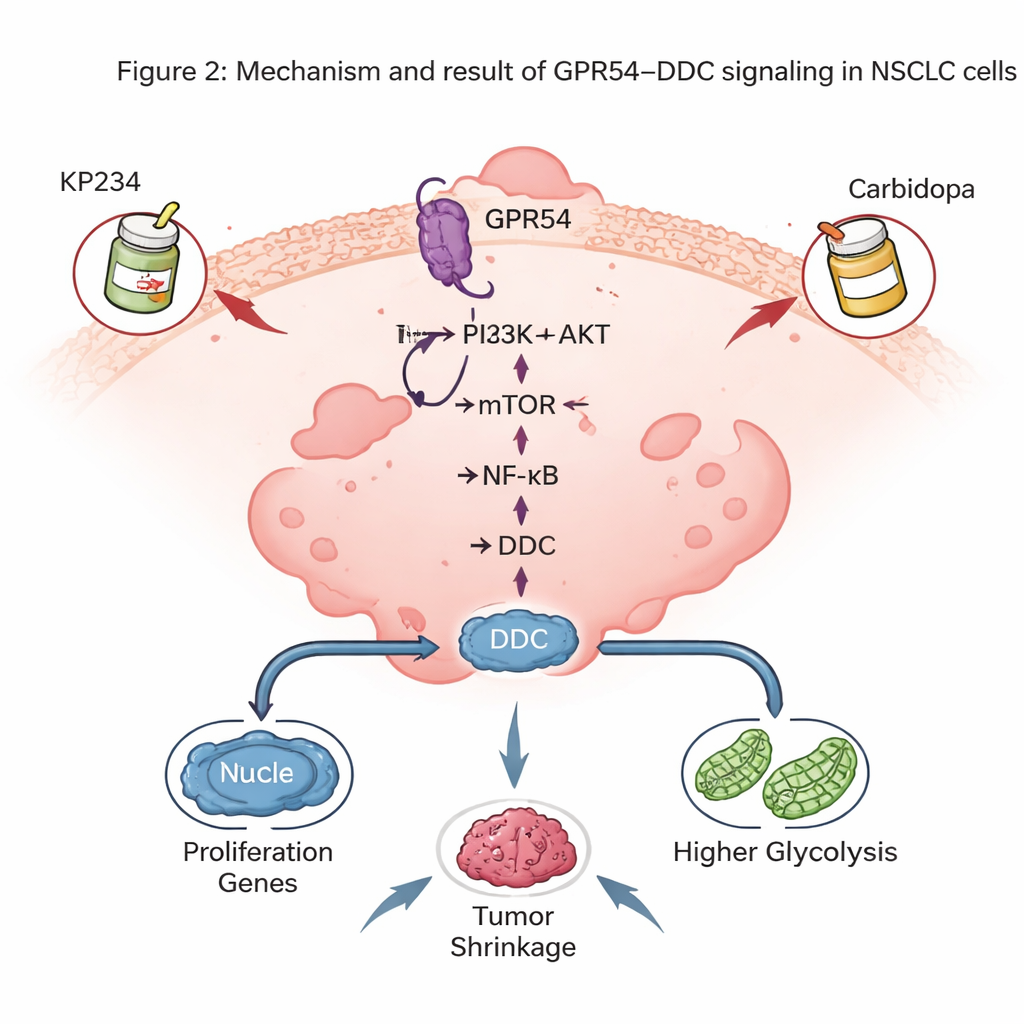
Beyinle ilişkili bir enzimin şaşırtıcı rolü
En çarpıcı keşiflerden biri, GPR54’ün beyin kimyasalları dopamin ve serotonin yapmasıyla en iyi bilinen DDC düzeylerini kontrol etmesiydi. Fare tümörlerinde DDC düzeyleri GPR54 miktarıyla yakından paralel hareket etti: daha az GPR54, daha az DDC demekti. İnsan KHDAK tümörleri ve hücre hatları da normal akciğer hücrelerine göre daha yüksek DDC gösterdi ve daha fazla DDC’ye sahip hastaların sağkalımı daha kötüydü. Akciğer kanseri hücrelerinde DDC azaltıldığında farelerde tümör büyümesi yavaşladı, kültürde hücre bölünmesi azaldı ve daha fazla apoptoz tetiklendi. Moleküler düzeyde DDC, kanser hücresi hayatta kalmasını ve iltihabı teşvik eden ana düzenleyicilerden biri olan NF-κB yolunun aktivitesini sürdürmeye yardımcı oldu ve ayrıca tümör hücrelerinin yüksek glikoliz durumunu destekledi.
Bir ilaç eşleştirme stratejisinin denenmesi
DDC, Parkinson hastalığında karbidopa adlı bir ilaçla hedeflendiği için yazarlar GPR54 blokeri (KP234) ile karbidopayı birleştirmenin KHDAK’ya iki taraftan vurup vuramayacağını araştırdı. Hücre kültüründe ve insan KHDAK hücrelerinin akciğerde büyütüldüğü fare modellerinde, ikili tedavi tek ilaçtan daha fazla tümör büyümesini kesti ve kanser hücresi ölümünü artırdı; hayvanlarda belirgin kilo kaybı gözlenmedi. Bu kombinasyonlar ayrıca mutant RAS genlerine yönelik bazı modern hedefe yönelik ilaçlarla birlikte de umut verici sonuçlar gösterdi; bu da GPR54–DDC sinyalinin mevcut hassas tedavilerin üzerine eklenebileceğini düşündürüyor.
Gelecekteki akciğer kanseri tedavisi için anlamı
Hekim olmayan bir okuyucu için temel mesaj şudur: KHDAK hücreleri, hayatta kalmak ve yakıtı hızlı yakmak için yüzeydeki bir anahtar (GPR54) ile bir metabolik enzim (DDC) arasındaki daha önce yeterince tanınmamış bir ortaklığa dayanır. Bu ortaklığı bozmak tümörleri zayıflatır; deneysel modellerde daha yavaş büyümelerine ve daha kolay ölmesine neden olur. Bu tür stratejiler kliniğe ulaşmadan önce daha çok çalışma gerekmekle birlikte, bu çalışma GPR54 ve DDC’yi agresif KHDAK’yı tanımlamak için potansiyel biyobelirteçler ve standart tedavilerden kaçan hastaların sonuçlarını iyileştirebilecek yeni kombinasyon tedavileri için umut vaat eden hedefler olarak konumlandırıyor.
Atıf: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Anahtar kelimeler: küçük hücre dışı akciğer kanseri, GPR54, dopa dekarboksilaz, kanser metabolizması, hedefe yönelik tedavi