Clear Sky Science · tr
Kanserde reaktif oksijen türleri (ROS): mekânizmadan terapötik çıkarımlara
Yararlı Moleküller Nasıl Tehlikeli Olur
Her hücrenin içinde, reaktif oksijen türleri ya da ROS olarak adlandırılan küçük kimyasal kıvılcımlar normal yaşamın bir parçası olarak sürekli üretilir. Uygun düzeylerde bunlar hücrelerin büyümesine, iletişim kurmasına ve mikroplara karşı savunmasına yardımcı olur. Ancak bu derleme aynı moleküllerin DNA’ya zarar verebileceğini, hücresel devreleri bozabileceğini ve kanserin büyümesini, yayılmasını ve tedaviye direnç kazanmasını tetikleyebileceğini açıklar. ROS’un bu “çifte yaşamını” anlamak, bilim insanlarının zararlı oksidatif stresi yatıştıran veya tümör hücrelerini öldürmek için kasıtlı olarak bunu aşan yeni kanser terapileri tasarlamasına yardımcı oluyor.
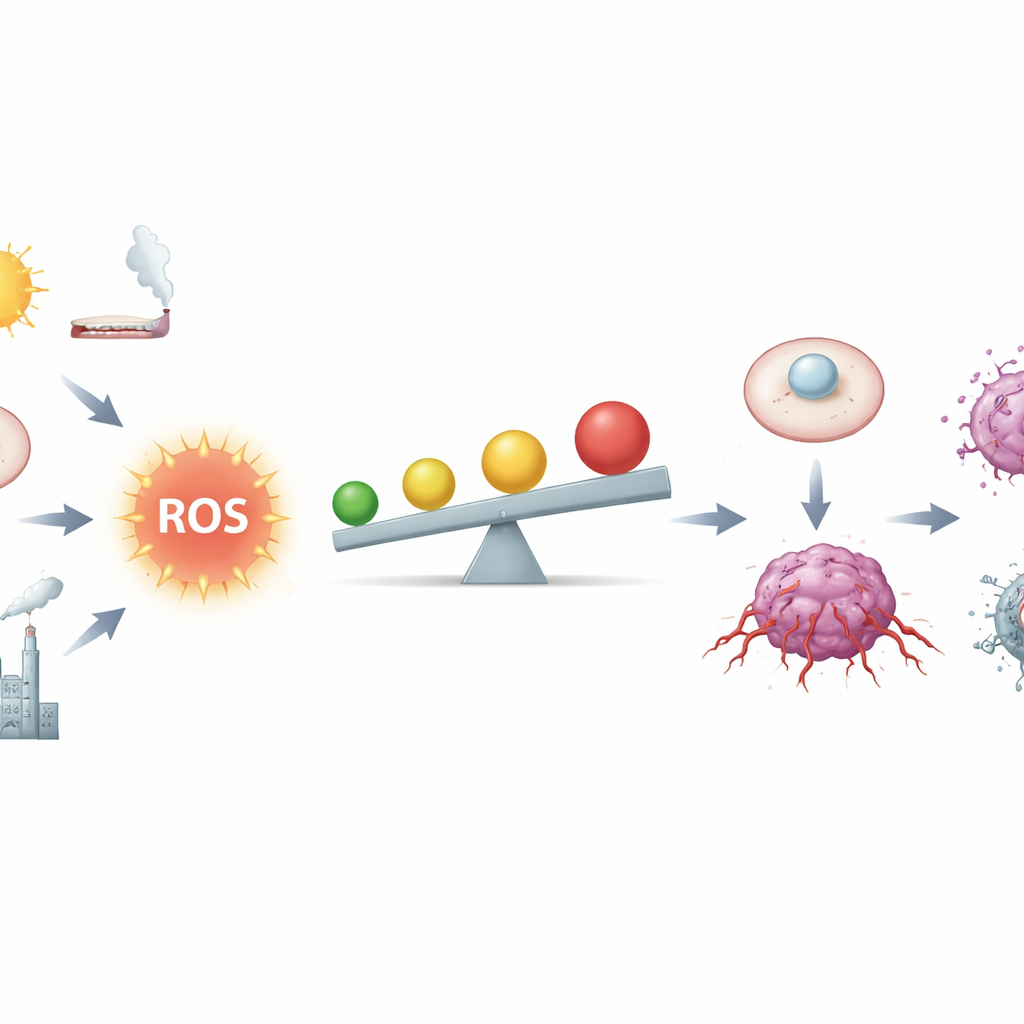
Yakıt ile Ateş Arasındaki İnce Çizgi
Yazarlar ROS’u solunum ve metabolizmanın kimyasal yan ürünleri olarak tanımlar, ama aynı zamanda güçlü haberci moleküllerdir. Sağlıklı dokularda düşük miktarlardaki ROS hücre döngüsünü kontrol etmeye, hasarı onarmaya ve bağışıklığı ince ayarlamaya yardımcı olur. Hücreler bu sinyalleri, glutatyon gibi moleküller ve Nrf2 adı verilen bir ana anahtar tarafından kontrol edilen enzimler de dahil olmak üzere ayrıntılı bir antioksidan ağı kullanarak dengede tutar. Ancak kanser hücreleri tehlike bölgesine daha yakındır: hatalı genler, aşırı çalışan mitokondriler, kronik inflamasyon, tütün dumanı, radyasyon ve bazı metaller ROS’u yükseltir. Orta-yüksek düzeylerde ROS DNA’yı tıraşlayabilir, kromozomları kararsızlaştırabilir ve büyüme ile hayatta kalma devrelerini kronik olarak “açık” hale getirerek normal bir hücrenin kanser hücresine dönüşmesini kolaylaştırır.
Oksidatif Stresin Tümör Davranışını Nasıl Şekillendirdiği
Bir tümör oluştuktan sonra ROS biyolojisini şekillendirmeye devam eder. Orta düzey oksidatif stres, hücrelerin bölünmesini, yeni kan damarları oluşturmasını, yakın dokuyu istila etmesini ve kemoterapiye dayanmasını teşvik eden birçok büyüme yolunu aktive eder. ROS kanser hücrelerinin şekeri, yağları ve amino asitleri kullanma biçimini yeniden programlayabilir; böylece yakıtı ekstra antioksidan gücü ve yeni hücreler için yapı taşları üreten yollara yönlendirir. Ayrıca hücrenin kader kararlarını etkiler: yoğunluk ve bağlama bağlı olarak ROS, dengeyi hayatta kalma sinyalleri lehine veya klasik apoptoz gibi programlı hücre ölümü ile ferroptoz, nekroptoz ve kuproptoş gibi daha yeni ölüm biçimlerinden birine doğru çevirebilir. Bu durum ROS’u hem tümör ilerlemesinin suç ortakları hem de tümörün kendi kendini yok etmesi için potansiyel tetikleyiciler yapar.
Bağışıklığı ve İlaç Yanıtını Yeniden Kabaklama
Derleme, ROS’un yalnızca kanser hücreleri içinde hareket etmediğini — tümörün çevresini yeniden şekillendirdiğini — vurgular. Yüksek oksidatif stres, kanserle savaşan T hücrelerini ve doğal öldürücü hücreleri tükenmeye veya ölmeye zorlayabilir, aynı zamanda tümörü saldırılardan koruyan baskılayıcı hücreleri destekleyebilir. ROS ayrıca tümörlerin “beni öldürme” sinyallerini, örneğin kontrol noktası proteinlerini yukarı çekmesine yardımcı olarak immünoterapinin etkilerini körleştirebilir. Aynı zamanda orta düzey ROS, ilaç-çıkış pompalarını ve stres yanıtlarını artırarak ilaç direncini tetikleyebilir; bu da kanser hücrelerinin kemoterapiyi dışarı atmasına veya verdiği hasarı onarmasına izin verir. Ancak diğer koşullar altında ROS’u kritik bir eşiğin ötesine itmek bu savunmaları parçalayabilir ve tümörleri tedaviye yeniden duyarlı hale getirebilir.
Redoks Zayıflığını Tedavi Stratejisine Çevirmek
Kanser hücreleri ROS’u kullanma ile onlardan zehirlenme arasında bir ipte yürüdükleri için yazarlar ROS dengesini terapötik bir kaldıraç olarak görür. Bir strateji, özellikle önleme amacıyla veya tedavi sırasında sağlıklı dokuyu korumak için zarar verici ROS’u azaltmak ya da antioksidanları güçlendirmektir. Diğer strateji tümörlerde bunun tersini yapmaktır: antioksidan sistemleri engellemek veya ROS üretimini artırmak, böylece kanser hücreleri ölümcül eşiği aşana kadar ROS’u yükseltmek; bu yaklaşım radyasyon, hedefe yönelik ilaçlar veya immünoterapi ile birleştirildiğinde özellikle etkili olabilir. Üçüncü bir yaklaşım ise ROS düzeylerini değiştirmeden, tümörlerin dayandığı ROS’a duyarlı anahtarları — sinyal proteinlerini, metabolik enzimleri veya ölüm yollarını — bloke etmektir. Bu fikirlerin hepsinde kişiselleştirme teması vardır: farklı kanserler farklı “redoks imzalar” taşır, bu yüzden gelecekteki tedaviler her hasta için doğru redoks hedefli tedaviyi seçmek üzere oksidatif hasar, antioksidan kapasite ve ROS ilişkili genlerin kan veya doku testlerini gerektirebilir.
Hastalar İçin Ne Anlama Geliyor
Basitçe söylemek gerekirse, bu makale ROS’un tamamen kötü ya da tamamen iyi olmadığını; hücrelerin ve kanserlerin kullandığı güçlü araçlar olduğunu savunur. Kanser hücreleri sağlıklı hücrelere göre oksidatif stresin eşik noktasına daha yakın çalışmaya meyillidir ve bu durum terapötik bir pencere yaratabilir. Ancak antioksidanlar ve pro-oksidanların doz, zamanlama ve tümör türüne bağlı olarak hem fayda hem zarar verebilmesi nedeniyle takviye ya da ROS’u artıran ilaçların genel kullanımı risklidir. Yazarlar geleceğin her tümörün redoks durumunu okuyacak dikkatle tasarlanmış tedaviler ve tanılar olduğunu ve ardından ROS’u ve antioksidan sistemleri ya normal dokuları korumak için yeterince aşağı çekecek ya da kanser hücrelerini kırılma noktalarının ötesine itmek için yeterince yukarı kaldıracak şekilde düzenleyeceklerini sonucuna varıyorlar.
Atıf: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Anahtar kelimeler: reaktif oksijen türleri, oksidatif stres, kanser metabolizması, redoks terapisi, tümör mikroçevresi