Clear Sky Science · tr
Ekzogen Epstein–Barr virüsü nükleer antijeni 1, immünoterapiye karşı ADAR1 kaynaklı tümör direnci oluşturur
Yaygın bir virüs kanser tedavisi için neden önemli?
Çok sayıda kanser artık vücudun kendi bağışıklık sistemini serbest bırakan immünoterapi ilaçlarıyla tedavi ediliyor. Yine de hastaların çoğu bundan fayda görmüyor; çünkü tümörleri bağışıklık saldırısından kaçmayı öğreniyor. Bu çalışma, çok yaygın bir virüs olan Epstein–Barr virüsünün (EBV) tümörlerin bağışıklık savunmalarını nasıl kapattığını ve bu güçlü ilaçlara karşı nasıl direnç oluşturduğunu—ve tasarım temelli yeni bir molekül tipinin bu savunmaları nasıl yeniden etkinleştirebileceğini—açıklıyor.
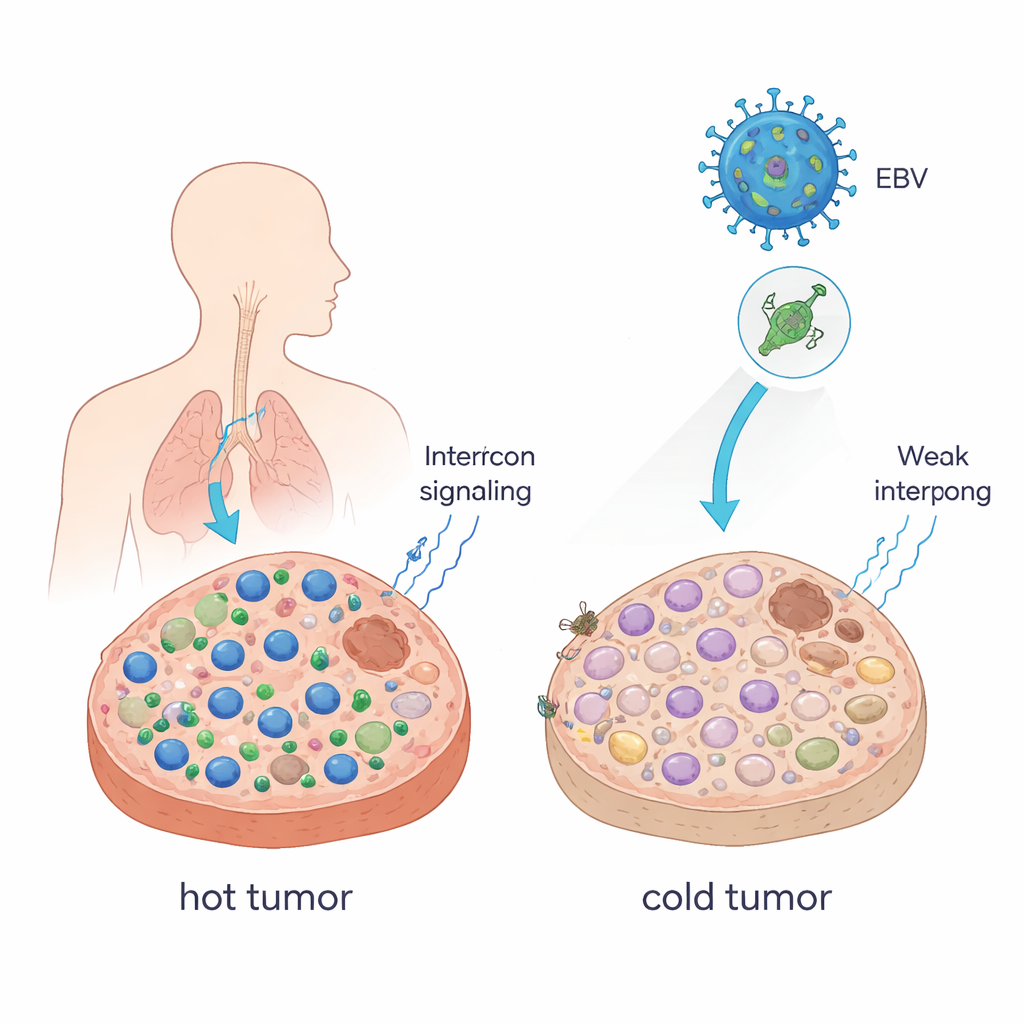
Sıcak tümörleri soğuk hale getirmek
Hekimler genellikle içinde kanseri öldüren T hücrelerinin bol olduğu tümörleri "sıcak", bu hücrelerin az olduğu tümörleri ise "soğuk" olarak tanımlar. Sıcak tümörler genellikle anti–PD-1 antikorları gibi immün kontrol noktası blokajı (ICB) ilaçlarına iyi yanıt verir; soğuk tümörler ise çoğunlukla yanıt vermez. Yazarlar tek bir EBV proteininin, EBNA1 olarak adlandırılan proteinin, tümörleri daha soğuk ve daha saklanmacı bir duruma itebileceğini gösterdi. Fare tümör hücrelerine EBNA1 üretmelerini zorladıklarında ve bunları sağlam bağışıklık sistemine sahip farelerde büyüttüklerinde, tümörler daha büyük oldu, daha az CD8+ T hücresi ve doğal öldürücü hücre içerdi ve bağışıklık baskılayıcı makrofajlar arttı. Bağışıklık hücrelerini harekete geçirmeye yardımcı kilit haberciler olan interferon sinyalleri de güçlü biçimde azaldı. EBV ile sıkı ilişki gösteren nazofaringeal karsinom hasta örneklerinde EBNA1 ifade eden tümörler de benzer şekilde normal dokuya göre daha az CD8+ T hücresi gösterdi.
Viral bir kestirme: hücrenin RNA-denetim mekanizmasına giriş
EBNA1’in tümör ortamını nasıl yeniden şekillendirdiğini anlamak için araştırmacılar onunla fiziksel etkileşim yapan insan proteinlerini aradı. m6A işaretlerini okuyan ve haberci RNA’ların stabilitesini veya çevirisini artırabilen IGF2BP3 adlı bir proteine odaklandılar. EBNA1, EBV-pozitif kanser hücreleri dahil olmak üzere birkaç hücre tipinde IGF2BP3’e sıkı bağlandı. Hasta tümörlerinden alınan veriler, yüksek IGF2BP3 düzeylerinin interferon ilişkili gen aktivitesinin zayıf olması ve daha düşük CD8+ T hücresi infiltrasyonu ile birlikte olduğunu gösterdi; bu da viral-konak ortaklığının antitümör bağışıklığını zayıflatabileceğini işaret ediyor.
Tehlike sinyallerini susturan bir RNA editörünü güçlendirmek
Daha derin analizler bu etkileşimin kilit bir hedefini ortaya koydu: belirli “A” harflerini “I”ye çevirerek çift sarmallı RNA’yı düzenleyen ADAR1 enzimi. Bu düzenleme, hücre içindeki viral benzeri RNA’yı iç sensörlere daha az tehlikeli gösterebilir ve interferon yanıtlarını azaltabilir. Yazarlar EBNA1, IGF2BP3 ve EIF4G1 adlı bir çeviri faktörünün ADAR1 mRNA’sı üzerinde üç parçalı bir kompleks oluşturduğunu buldu. Bu kompleks m6A etiketlemesini artırıyor, çeviri mekanizmasını işe alıyor ve ADAR1 RNA seviyelerini yükseltmeden ADAR1 protein üretimini seçici biçimde artırıyor. Sonuç olarak tümör hücreleri, özellikle interferon ilişkili genlerin yakınında bulunan tekrarlı genetik elementlerde daha fazla RNA düzenlemesi yapıyor. Bu düzenlemeler, normalde MDA5 ve PKR gibi sensörleri uyarması gereken düzenlenmemiş çift sarmallı RNA havuzunu azaltarak interferon üretimini köreltiyor ve tümörlerin bağışıklık saldırısından saklanmasına yardımcı oluyor.
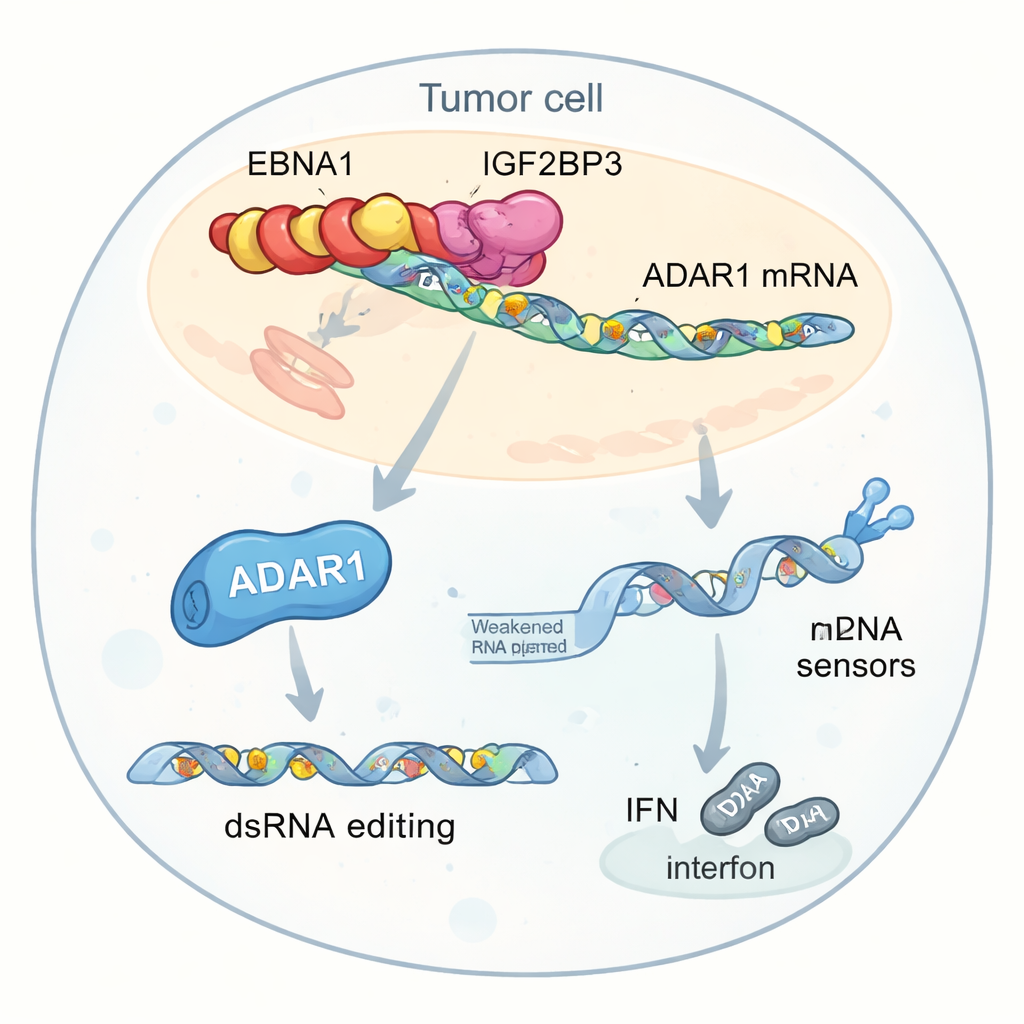
Daha az interferon, zayıf immünoterapi
Laboratuvarda EBNA1 ifade eden tümör hücreleri T hücreleri ve anti–PD-1 antikorlarıyla karşılaştırıldığında, kontrol hücrelerine göre öldürülmesi daha zordu ve daha az interferon salgıladılar. Doğrudan interferonla muamele edildiklerinde bile EBNA1 taşıyan hücreler daha az hassastı ve iç RNA sensörleri daha zayıf aktifleştirildi. ADAR1 düzeylerini azaltmak bu etkileri kısmen tersine çevirdi, sensör aktivitesini ve interferon sinyalini geri getirdi. Genetik ve dizileme deneyleri EBNA1 ifade eden hücrelerin belirli RNA bölgelerinde, özellikle interferon uyarımından sonra, daha fazla A-to-I düzenleme olayı gösterdiğini doğruladı; bu da viral destekleyici ADAR1 artışının aksi halde güçlü bağışıklık tepkilerini tetikleyecek tehlike sinyallerini nötralize etmeye yardımcı olduğu fikrini güçlendiriyor.
Bağışıklık saldırısını yeniden uyandıran bir tasarımcı bozucu
Ekip daha sonra tümörlerden EBNA1’i uzaklaştırmanın immünoterapiye karşı hassasiyeti geri getirebileceğini sordu. EBNA1’i hücrenin kendi atık sistemine işaretleyerek yıkan bir PROTAC molekülü, EP-1215, tasarladılar. Düşük dozlarda EP-1215 EBNA1’i etkin biçimde parçaladı ve ADAR1 protein düzeylerini azalttı. Fare deneylerinde EP-1215 tek başına EBNA1-pozitif tümörler üzerinde sınırlı etki gösterdi ve anti–PD-1 tek başına da zayıftı. Ancak iki tedavi birleştirildiğinde tümörler keskin biçimde küçüldü, CD8+ T hücresi infiltrasyonu arttı ve interferon üreten T hücreleri çoğaldı. İnsan bağışıklık hücrelerine ve EBV ilişkili tümörlere sahip insanlaştırılmış fare modellerinde de kombinasyon tek başına tedavileri geride bıraktı ve bariz karaciğer veya böbrek toksisitesi saptanmadı.
Gelecek kanser bakımına etkisi
Uzman olmayanlar için çıkarım şu: yaygın bir virüs kanser hücrelerini sessizce yeniden programlayarak hücre içi alarm sistemlerini susturabilir ve aksi takdirde bağışıklık hücrelerini çekecek ve etkinleştirecek kimyasal sinyalleri kapatabilir. EBNA1 bunu bir konak RNA okuyucusu (IGF2BP3) ve bir çeviri faktörü (EIF4G1) ele geçirip RNA editörü ADAR1’in aşırı üretimini sağlayarak yapıyor; ADAR1 de bağışıklık sensörlerinin tanımak üzere kurulduğu RNA yapılarını düzenleyip ortadan kaldırıyor. EP-1215 gibi hedefe yönelik bir PROTAC ile EBNA1’in parçalanması, bu tehlike sinyallerini geri getirebildi ve dirençli tümörleri mevcut kontrol nokta ilaçlarına yeniden duyarlı hale getirdi. Benzer stratejiler insanlarda güvenli ve etkili bulunursa, EBNA1 gibi viral yardımcıları hedeflemek, soğuk EBV-bağlantılı tümörleri sıcak hedeflere çevirmenin yeni bir yolu olabilir; böylece modern immünoterapiler nihayet etkinlik gösterebilir.
Atıf: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Anahtar kelimeler: Epstein-Barr virüsü, immünoterapi direnci, ADAR1, RNA düzenleme, nazofaringeal karsinom