Clear Sky Science · tr
PKC-eta, Hippo–YAP sinyal yolunu düzenleyerek meme kanseri metastazını teşvik ediyor
Bu araştırma neden önemli
Üçlü‑negatif meme kanseri (TNBC), erken yayıldığı ve hedefe yönelik tedavilerinin eksik olduğu için en tehlikeli meme kanseri türlerinden biridir. Bu çalışma, PKC‑eta (PKCη) adı verilen kanser hücreleri içindeki belirli bir enzimin, tümörlerin kopup vücutta yolculuk ederek yeni tümörler oluşturmasına yardımcı olan bir anahtar gibi davrandığını ortaya koyuyor. Bu anahtarın nasıl çalıştığını anlayarak araştırmacılar, onu kapatabilen küçük doğal bir peptidi de tanımlıyor; bu da agresif hastalık için potansiyel yeni bir tedavi yoluna işaret ediyor. 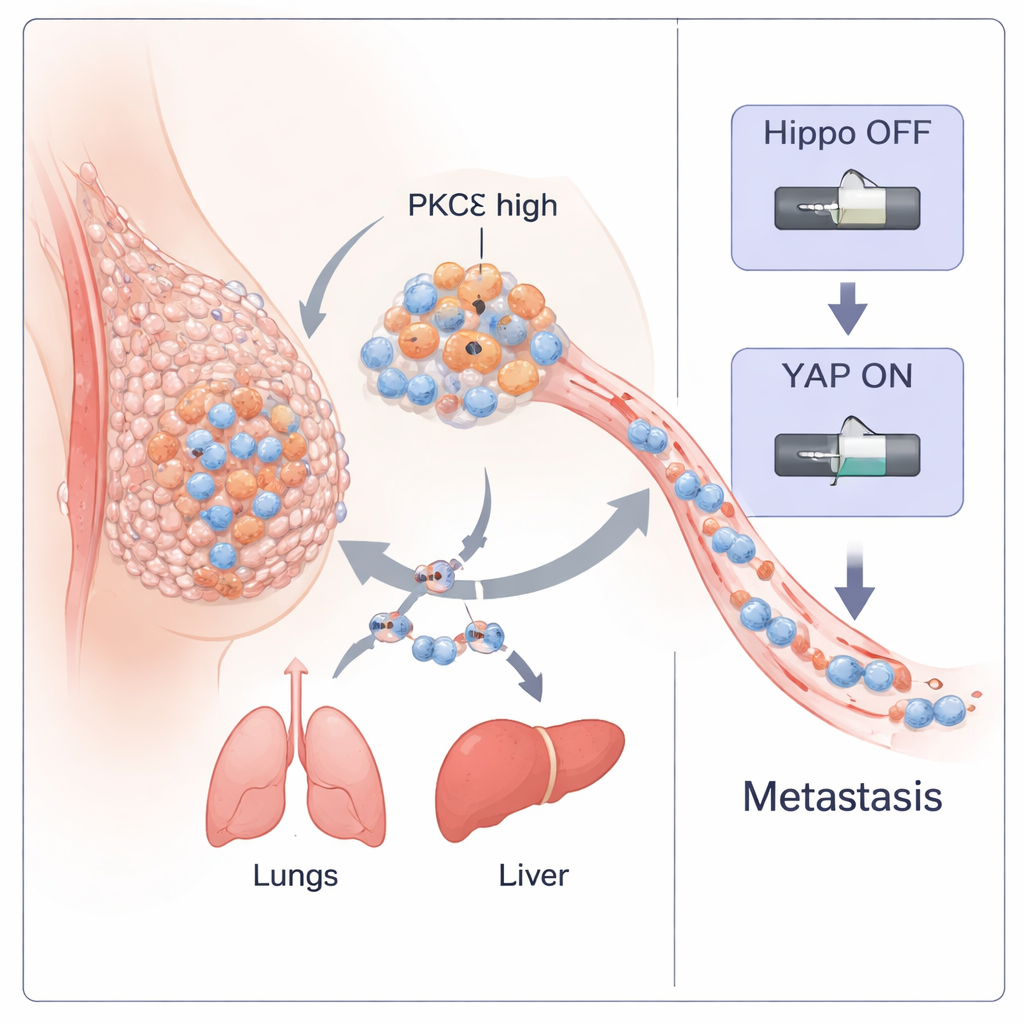
Agresif meme tümörlerinde gizli bir sürücü
Ekip, büyük meme kanseri hasta veri kümelerini taramakla başladı. PKCη’yi kodlayan genin (PRKCH) “claudin‑low” olarak bilinen ve TNBC ile güçlü örtüşme gösteren, kök hücre benzeri ve yüksek hareket kabiliyetine sahip hücrelerce zengin bir tümör alt tipinde özellikle yüksek olduğunu buldular. Birden çok hasta kohortunda, yüksek PRKCH gösteren tümörler epitel–mesenkimal geçiş (EMT) imzaları sergiledi—bir zamanlar düzenli olan hücrelerin bağlantılarını gevşetip şekil değiştirerek daha invazif hâle geldiği bir süreç. PRKCH düzeyleri ayrıca metastatik örneklerde birincil primer tümörlere göre daha yüksekti ve insan TNBC dokularının protein boyamaları, yüksek dereceli ileri evre kanserlerde daha aktif, perinükleer PKCη gösterdi. Birlikte, bu bulgular PKCη’nin tümör agresifliği ve yayılımıyla yakından ilişkili olduğunu öne sürdü.
Laboratuvardan fareye: PKCη’nin yayılanı beslediğini göstermek
Neden‑sonuç ilişkisini sınamak için araştırmacılar, iki yüksek metastatik TNBC hücre hattından, biri fare (4T1) ve biri insan (MDA‑MB‑231) olanlardan PKCη’yi CRISPR gen düzenleme ile kaldırdılar. PKCη olmadan hücreler daha “epitelyal” bir duruma kaydı: E‑kadherin ve EpCAM gibi adezyon proteinleri arttı, vimentin ve N‑kadherin dahil klasik mesenkimal belirteçler azaldı. Bu PKCη‑eksik hücreler daha az ve daha küçük koloniler oluşturdu, göç ve invazyon yetenekleri düştü, yerinden ayrıldıklarında hücre ölmesine karşı daha hassas oldu ve CD44high/CD24low ve ALDH‑pozitif hücre sayısı ile küre oluşturma kapasitesi gibi kanser kök hücresi özelliklerinde keskin bir azalma gösterdi. Farelere enjekte edildiğinde, PKCη eksik hücreler daha küçük primer tümörler ve akciğer, karaciğer, beyin ve diğer organlara çok daha az metastaz üretti; fareler ayrıca daha uzun yaşadı. PKCη’nin geri verilmesi bu değişiklikleri tersine çevirdi ve enzimin TNBC ilerlemesini ve yayılmasını aktif olarak desteklediğini doğruladı.
PKCη, bir büyüme kontrol yolunu nasıl ele geçiriyor
Çalışma sonra PKCη’nin bu prometastatik gücü nasıl uyguladığını detaylandırdı. Hasta verileri, PKCη düzeylerinin, Hippo yolunun kontrol ettiği güçlü bir gen‑anahtarı olan YAP ile eşzamanlı olarak yükselip düştüğünü gösterdi—Hippo yolu normalde büyümeyi sınırlayan bir hücresel “fren” görevi görür. PRKCH veya YAP1’in yüksek düzeyleri daha kötü hasta sonuçlarını öngördü ve her ikisinin de birlikte yüksek olması uzak metastaz‑özgür sağkalım ile özellikle kötü ilişkilendirildi. TNBC hücrelerinde PKCη’nin kaldırılması toplam YAP düzeyini düşürdü ve YAP’ı çekirdekten sitoplazmaya kaydırdı; burada inaktif hâlde kalır. Biyokimyasal deneyler, PKCη’nin YAP ile fiziksel olarak bağlandığını ve özellikle Ser128 pozisyonuna bir fosfat grubu eklediğini gösterdi. Bu modifikasyon YAP’ı stabilize eder ve çekirdeğe girip EMT, kök hücre özellikleri ve metastazı yöneten genleri açmasına yardımcı olur. PKCη yok olduğunda, YAP bunun yerine Ser127 ve Ser397 gibi farklı konumlarda işaretlenir; bu işaretler YAP’ın 14‑3‑3 proteinlerine bağlanmasına, sitoplazmada hapsolmasına ve nihayetinde degradasyonuna yol açar. PKCη ayrıca AKT enziminin doğal frenleyicisi olan PTEN’i artırır; böylece AKT aktivitesini düşük tutar ve aksi takdirde YAP’ı inaktive edecek üst akış Hippo kinazlarını baskılar. Bu yolla PKCη hem doğrudan YAP’ı aktive eder hem de dolaylı olarak Hippo “frenini” kapalı tutar. 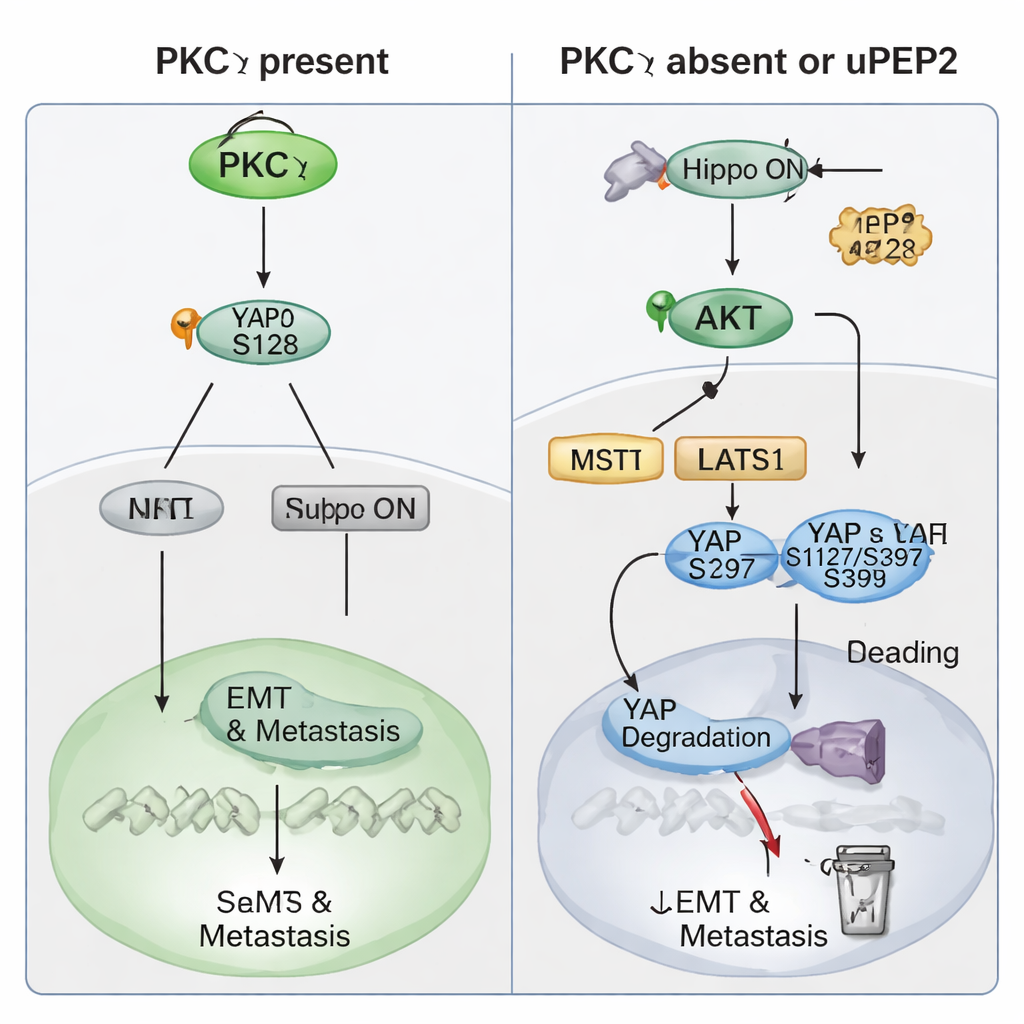
Kansere yönelik anahtarı etkisizleştiren küçük bir peptid
İlginç biçimde, PKCη geni kısa bir upstream açık okuma çerçevesi (uORF) taşır ve bu uORF uPEP2 adlı bir mikropeptidi kodlar. Önceki çalışmalar uPEP2’nin PKCη ve ilişkili enzimlere bağlanıp onları inhibe edebileceğini göstermişti. Burada, sentetik uPEP2 ile TNBC hücrelerinin tedavisi PKCη gen koparmaya benzer etkiler oluşturdu: göç, invazyon ve kök hücre‑benzeri davranışlar azaldı, EMT belirteçleri daha az agresif bir profile kaydı ve YAP düzeyleri düşerken onun “kapalı” fosforilasyon işaretleri arttı. Fare tümörlerinde uPEP2, primer tümörlerde PKCη ve YAP’ı azalttı, YAP inaktivasyonunu artırdı ve karaciğer ile akciğerde daha az mikrometastaz ile ilişkilendirildi. Mekanistik olarak uPEP2, PKCη’nin degradasyonunu teşvik ederek Hippo yolunu yeniden açar ve YAP’ı sitoplazmik tutulmaya ve parçalanmaya yönlendirir.
Gelecekteki tedaviler için bunun anlamı
Hekim olmayan bir okuyucu için temel mesaj şudur: Araştırmacılar, en agresif meme kanserlerinin doğal bir büyüme‑kontrol sistemini devre dışı bırakarak ve YAP “gaz pedalını” aktif hale getirerek gevşemesine, hareket etmesine ve uzak organlara yerleşmesine yardımcı olan kilit bir bağlantı noktası olarak PKCη’yi tanımladı. PKCη’yi ortadan kaldırarak veya küçük doğal peptid uPEP2 ile onu degradasyona uğratarak Hippo güvenlik frenini geri getirebildiler, YAP’ı susturdular ve preklinik modellerde metastazı büyük ölçüde azalttılar. Bu çalışma hâlâ deneysel aşamada olup hücre hatları ve immün yetmezlikli farelerde gerçekleştirilmiş olsa da, PKCη ve onun YAP ile etkileşimini yeni TNBC tedavileri için umut verici hedefler olarak ön plana çıkarıyor ve uPEP2‑benzeri ilaçların bir gün bu zor tedavisi olan kanserin yayılmasını önlemeye veya sınırlamaya yardımcı olabileceğini öne sürüyor.
Atıf: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Anahtar kelimeler: üçlü negatif meme kanseri, PKC-eta, Hippo-YAP yolu, epitel-mesenkimal geçiş, kanser metastazı