Clear Sky Science · tr
Osteoartrit: moleküler patogenez ve potansiyel tedavi seçenekleri
Günlük Eklem Ağrısı Bütün Vücudun Öyküsü Haline Geldiğinde
Azalan diz ağrıları veya sert parmaklar genellikle yaşlanmanın kaçınılmaz bir parçası olarak geçiştirilir. Oysa osteoartrit — dünya genelinde en yaygın eklem hastalığı — yalnızca "aşınma" değildir. Bu derleme makale, ağrılı eklemlerin içinde gerçekte neler olduğunu, yanlış çalışan ağrı sinirlerinden aşırı yüklenen hücresel makineliğe kadar açığa çıkarıyor ve basit ağrı kesicilerin ötesine geçen yeni tedavi kuşaklarını inceliyor.
Ağır Kişisel Maliyetleri Olan Yaygın Bir Hastalık
Osteoartrit küresel nüfusun yaklaşık %8’ini etkiler; yüz milyonlarca insan kronik ağrı ve azalmış hareket kabiliyeti ile yaşamaktadır. Hastalık daha sık kadınlarda, 55 yaş üstünde ve fazla kilolu olanlarda ya da işleri veya sporları gereği eklemlere tekrarlayan ağır yük binen kişilerde görülür. Bugünün standart bakım yaklaşımları — egzersiz, kilo verme, korseler, anti-inflamatuar ilaçlar, eklem içi enjeksiyonlar ve şiddetli durumlarda eklem protezi — semptomları hafifletebilir ama nadiren hastalığın ilerlemesini durdurur. Bu ihtiyaç ile mevcut tedaviler arasındaki boşluk, bilim insanlarını osteoartritin nasıl başladığını ve neden bu kadar çok acı verdiğini daha derinlemesine araştırmaya yöneltti.
Eklem Neden Ağrır: Kablolar, Kimyasallar ve Sinyaller
Osteoartritte ağrı yalnızca röntgenle açıklanamaz: az hasarı olan bazı kişiler şiddetli ağrı çekerken, ciddi değişiklikleri olan diğerleri az ağrı bildirir. Makale, ağrıyı diz ekleminden omurilik boyunca beyne kadar izler. Eklemdeki sinir uçları — özellikle ince Aδ ve C lifleri — interlökinler ve tümör nekroz faktörü de dahil olmak üzere iltihaplı kimyasalların ve ayrıca sinir büyüme faktörünün iç içe geçtiği bir ortamda yıkanır. Bu maddeler, sinir uçlarındaki sodyum ve kalsiyumu geçiren özel kanalları açar veya etkinleştirir, böylece sinirlerin daha kolay ve daha sık ateşlenmesine neden olur. Zamanla omurilik ve beyindeki ağrı yolları aşırı duyarlı hale gelebilir; normal hareket veya hafif soğuk bile şiddetli ve yanıcı bir his yaratabilir.
Eklem Hücrelerinin İçindeki Gizli İş Yükü
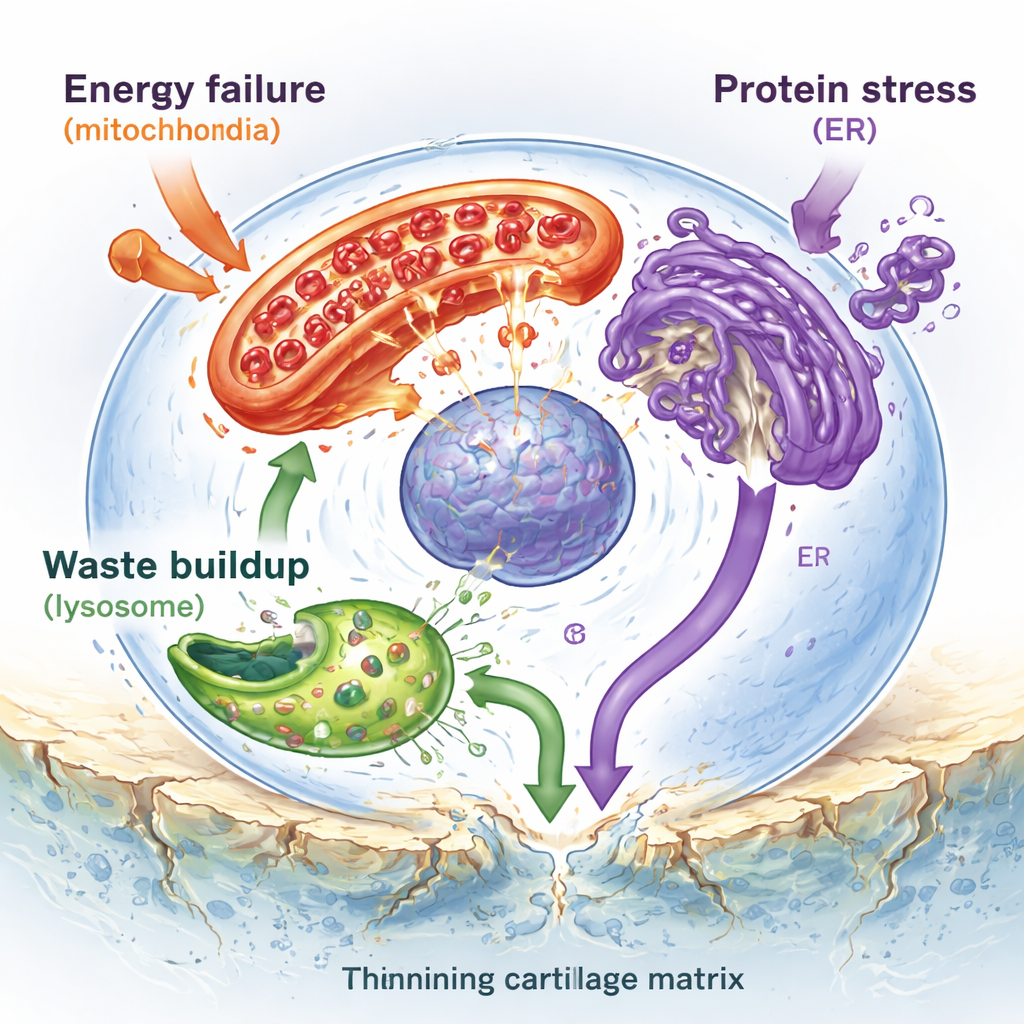
Kıkırdağın derinliklerinde, tek yerleşik hücreler olan kondrositler, kemiklerin kaymasını sağlayan pürüzsüz, esnek bir matriksi sürdürmeye çalışır. Yazarlar bu hücrelerin birden fazla cepheden kuşatma altında olduğunu gösteriyor. Hücrenin küçük enerji santralleri olan mitokondriler hasar görür ve daha az verimli hale gelir; çok az enerji üretip DNA ve proteinlere zarar veren aşırı reaktif oksijen türleri açığa çıkarırlar. Hücrenin geri dönüşüm merkezleri olan lizozomlar sert mineral kristallerle aşırı yüklenir; membranları zayıflar ve böylece yıkıcı enzimler hücre içine sızarak hücre ölümünü tetikler. Yeni proteinlerin katlandığı membran ağı olan endoplazmik retikulum, yanlış katlanmış moleküllerle tıkanır ve kronik bir "stres yanıtı" başlatır; bu süreç sonunda hücreleri öz-yıkıma iter. Bu stres altındaki organeller birlikte iltihabı besler ve kıkırdak kaybı ile kalsifikasyonunu hızlandırır.
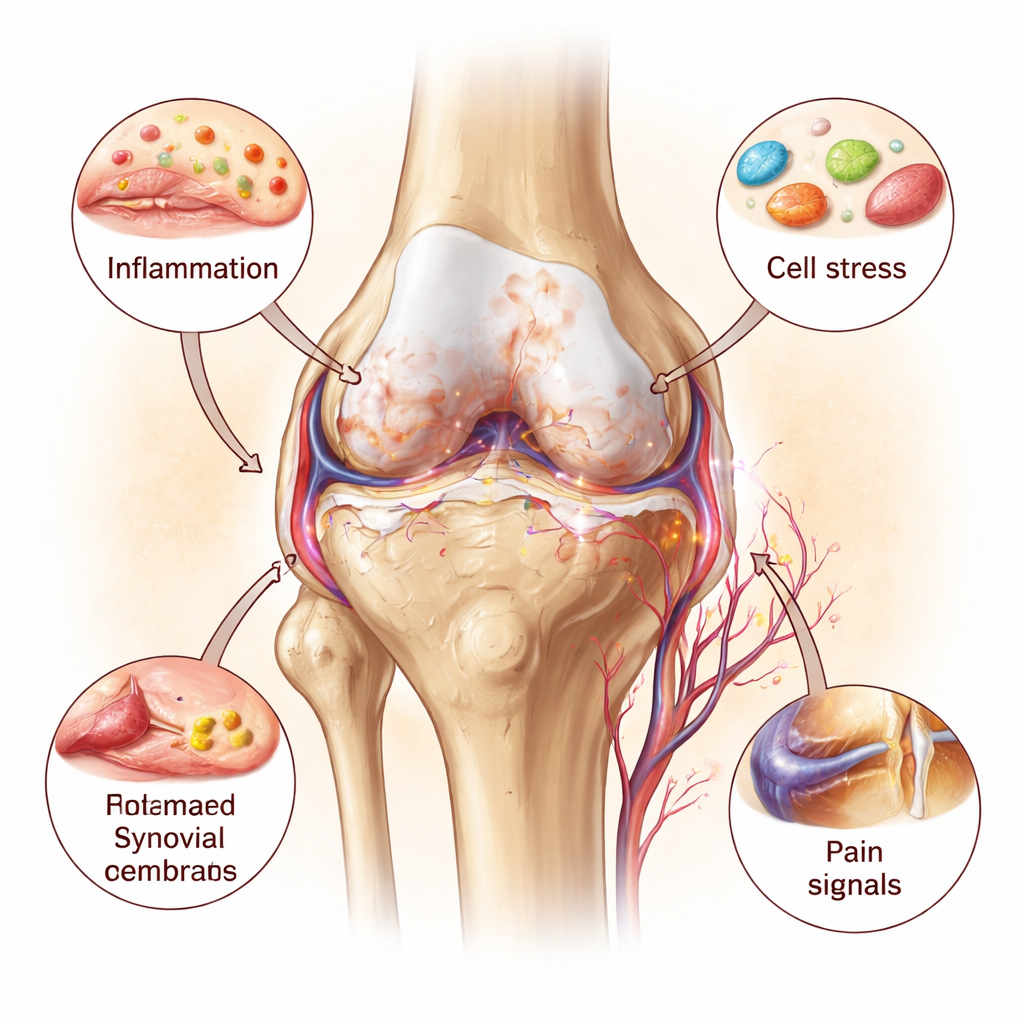
İltihap: Ateşe Yakıt
İnflamatuar haberci moleküller bu sürecin hoparlörleridir. Özellikle üçü — interlökin‑1, interlökin‑6 ve tümör nekroz faktör‑alfa — organel hasarı ile birlikte kötü döngü oluşturur. Bu moleküller kondrositleri kıkırdağı parçalayan enzimleri üretmeye ve eklem yüzeyi altındaki anormal kemik büyümesini teşvik etmeye sürükler. Aynı zamanda yaralanmış mitokondriler ve sızan lizozomlar kendi acil durum sinyallerini salarak eklem içindeki bağışıklık sensörlerini daha da aktive eder. Kan damarları ve ağrı lifleri normalde sessiz ve sinirsiz olan kıkırdak bölgelerine büyür, ağrı hassasiyetini artırır. Bu tüm-eklem bakışı, osteoartriti pasif, mekanik bir kıkırdak aşınması değil; yavaş ilerleyen ama kendini güçlendiren bir inflamatuar hastalık olarak tarif eder.
Yeni Tedavi Fikirleri: İyon Kanallarından Hücresel Güç Merkezlerine
Bu mekanistik haritayla donanan araştırmacılar yeni ilaçları ve taşıma sistemlerini test ediyor. Ağrı tarafında, deneysel ilaçlar TRPV1 (kapsaisin reseptörü), TRPA1, TRPM3/8 gibi kanalları veya belirli sodyum kanallarını (Nav1.7 ve Nav1.8) bloke ediyor ya da nazikçe desensitize ediyor; ayrıca sinirlerin aşırı hassaslaşmasını engellemek için sinir büyüme faktörünü nötralize ediyorlar. Hastalık-modifiye edici tarafta, hedefe yönelik antikorlar önemli inflamatuar sitokinleri azaltmayı amaçlarken; küçük moleküller ve "senolitik" ajanlar daha sağlıklı hücresel davranışı geri kazandırmaya çalışıyor. Özellikle heyecan verici bir sınır organel‑yönelimli tedavidir: mitokondri temizliğini (mitofaji) uyaran, lizozomal asidite ve membranları stabilize eden veya endoplazmik retikulum stresini hafifleten bileşikler. İlaçları kesin olarak ihtiyaç duyulan yere taşıyacak şekilde kıkırdak hücrelerine ve hatta belirli organellere yönelen sofistike nanopartiküller, lipozomlar ve tasarlanmış ekzomlar geliştiriliyor.
Osteoartritle Yaşayan İnsanlar İçin Bu Ne Anlama Geliyor
Makale, osteoartritin düzensiz hücre metabolizması, kronik düşük dereceli inflamasyon ve uyumsuz ağrı devreleri içeren karmaşık bir biyolojik bozukluk olarak görülmesi ve tedavi edilmesi gerektiği sonucuna varıyor. Önerilen birçok ilaç ve taşıma sistemi hâlâ erken laboratuvar veya hayvan test aşamasında olsa da, bunlar tedavinin çok modlu ve kişiselleştirilmiş olacağı bir gelecek vaat ediyor: aşırı aktif sinirleri yatıştırarak ağrıyı hafifletirken aynı zamanda eklemin kendi hücrelerini ve iç makinelerini korumak veya gençleştirmek. Hastalar için bu, yalnızca hareketi daha az ağrılı hale getiren değil, aynı zamanda bugün sıklıkla kaçınılmaz kabul edilen yapısal hasarı yavaşlatan veya mümkünse tersine çeviren terapilere ulaşmak anlamına gelebilir.
Atıf: Zhang, Y., Han, Y., Sun, Y. et al. Osteoarthritis: molecular pathogenesis and potential therapeutic options. Sig Transduct Target Ther 11, 81 (2026). https://doi.org/10.1038/s41392-025-02556-6
Anahtar kelimeler: osteoartrit, eklem ağrısı, kıkırdak, iltihap, mitokondri